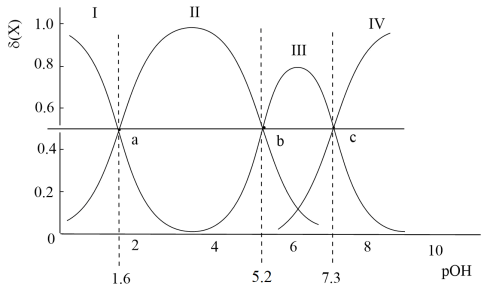
常温下,将一定量稀硫酸逐滴滴入高铁酸钠(Na2FeO4)溶液中,溶液中含铁微粒FeO 、HFeO
、HFeO 、H3FeO
、H3FeO 的物质的量分数δ(X)随pOH变化如图。下列说法正确的是
的物质的量分数δ(X)随pOH变化如图。下列说法正确的是
 、HFeO
、HFeO 、H3FeO
、H3FeO 的物质的量分数δ(X)随pOH变化如图。下列说法正确的是
的物质的量分数δ(X)随pOH变化如图。下列说法正确的是
| A.Ⅲ代表H2FeO4的变化曲线 |
| B.a、b、c三点水的电离程度相等 |
C.25℃时,FeO +3H2O +3H2O H3FeO H3FeO +3OH-的平衡常数K=10-12.1 +3OH-的平衡常数K=10-12.1 |
D.b点处:c(Na+)+c(H+)+c(H3FeO )=c(OH-)+2c(FeO )=c(OH-)+2c(FeO )+3c(HFeO )+3c(HFeO ) ) |
更新时间:2021-05-28 13:42:18
|
相似题推荐
多选题
|
较难
(0.4)
名校
【推荐1】已知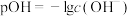 。初始温度25℃时,向
。初始温度25℃时,向 氨水中滴加
氨水中滴加 的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。下列说法正确的是
的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。下列说法正确的是

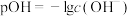 。初始温度25℃时,向
。初始温度25℃时,向 氨水中滴加
氨水中滴加 的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。下列说法正确的是
的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。下列说法正确的是
A.a、b、c三点对应 的水解平衡常数: 的水解平衡常数: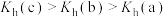 |
B.a点溶液中水电离产生的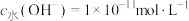 |
C.图中x=7,b点溶液中,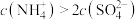 |
D.若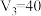 ,则c点对应溶液中 ,则c点对应溶液中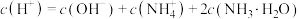 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】室温下,向10mL浓度均为0.1mol/L的CuCl2、FeCl2和ZnCl2溶液中分别滴加等浓度的Na2S溶液,滴加过程中pc[pc=-lgc(M2+),M2+为Cu2+或Fe2+或Zn2+]与Na2S溶液体积的关系如图所示。已知:Ksp(CuS)<Ksp(ZnS),Ksp(FeS)=6.25×10-18,lg25=1.4。下列说法正确的是
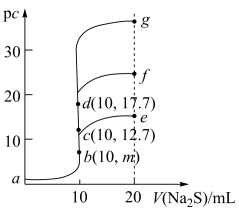

| A.m=8.6 |
| B.a点的CuCl2溶液中:2c(Cu2+)>c(Cl−)+c(OH−) |
| C.a→d→g的过程中,水的电离程度经历由大到小后又增大的过程 |
| D.将足量晶体ZnCl2加入0.1mol/L的Na2S溶液中,c(Zn2+)最大可达到10−24.4mol·L−1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐3】室温时,向 100mL 0.1mol·L-1 NH4HSO4溶液中滴加 0.1mol·L-1NaOH 溶液,溶液 pH随 NaOH 溶液体积的变化如图所示。下列说法正确的是
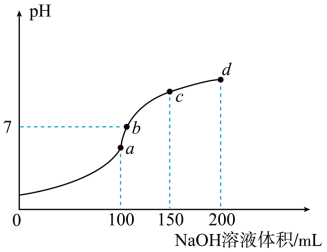

| A.图中 a、b、c、d 四个点,水的电离程度最大的是 d 点 |
B.a 点处存在 c(NH )+c(NH3·H2O)=0.1mol·L-1 )+c(NH3·H2O)=0.1mol·L-1 |
C.b 点处存在 c(Na+)>c(SO )>c(NH )>c(NH )>c(OH-)=c(H+) )>c(OH-)=c(H+) |
| D.由 b 到 c 发生反应的离子方程式为 NH4++OH-=NH3·H2O |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】缓冲溶液由浓度较大的弱酸及相应的盐溶液组成,其溶液能够保持稳定的pH,溶液pH的计算公式为pH= -lgKa +lg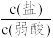 。现有25°C浓度均为1mol·L-1的CH3COOH和CH3COONa缓冲溶液[已知25°C时,Ka(CH3COOH) =1.75 ×10-5mol·L-1]。下列说法正确的是
。现有25°C浓度均为1mol·L-1的CH3COOH和CH3COONa缓冲溶液[已知25°C时,Ka(CH3COOH) =1.75 ×10-5mol·L-1]。下列说法正确的是
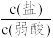 。现有25°C浓度均为1mol·L-1的CH3COOH和CH3COONa缓冲溶液[已知25°C时,Ka(CH3COOH) =1.75 ×10-5mol·L-1]。下列说法正确的是
。现有25°C浓度均为1mol·L-1的CH3COOH和CH3COONa缓冲溶液[已知25°C时,Ka(CH3COOH) =1.75 ×10-5mol·L-1]。下列说法正确的是| A.决定该缓冲溶液pH的主要因素是CH3COOH的Ka |
B.将该缓冲溶液稀释一倍,溶液中c(H+ )减小为原来的 |
| C.向该缓冲溶液中加入几滴NaOH溶液,溶液pH几乎不变 |
| D.该缓冲溶液中: c( CH3COO-) -c( CH3COOH) <c(H+) -c(OH- ) |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】H2C2O4为二元弱酸。25 ℃时,向0.100 mol·L−1 Na2C2O4溶液中缓缓通入HCl气体(忽略溶液体积的变化)。下列指定溶液中微粒的物质的量浓度关系正确的是
| A.0.100 mol·L−1 Na2C2O4溶液中:c(C2O42−)>c(HC2O4−)>c(OH−)>c(H+) |
| B.pH=7的溶液中:c(Cl-)=c(HC2O4−)+2c(H2C2O4) |
| C.c(Cl-)=0.100 mol·L−1溶液中:c(OH−)‒c(H+)=c(H2C2O4)‒c(C2O42−) |
| D.c(HC2O4−)=c(C2O42−)的酸性溶液中:c(Cl-)+c(HC2O4−)<0.100 mol·L−1+c(H2C2O4) |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐3】邻苯二甲酸(用H2A表示)为二元弱酸,常温下,Ka1=1.1×10-3,Ka2=3.9×10-6,室温下用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 H2A溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是
| A.滴加20 mL NaOH溶液时:c(OH-)>c(H+)+c(H2A )-2c(A2-) |
| B.pH=7的溶液:c(Na+)<0.050 00 mol·L-1+c(A2-) -c(H2A) |
| C.滴定过程中可能会出现:c(Na+)>c(HA-)=c(A2-)>c(OH-)>c(H+) |
| D.滴加40 mL NaOH溶液时:2c(Na+)=c(H2A)+c(A2-)+c(HA-) |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐1】常温下,向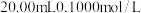 的
的 溶液中滴加
溶液中滴加 的
的 溶液,溶液中,
溶液,溶液中,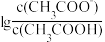 随pH的变化关系如图所示(取
随pH的变化关系如图所示(取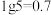 )。
)。
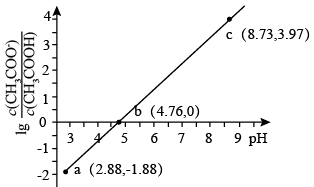
下列说法正确的是
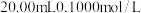 的
的 溶液中滴加
溶液中滴加 的
的 溶液,溶液中,
溶液,溶液中,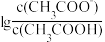 随pH的变化关系如图所示(取
随pH的变化关系如图所示(取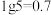 )。
)。
下列说法正确的是
A.常温下, 的电离常数为 的电离常数为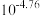 |
B.当溶液的 时,消耗 时,消耗 溶液 溶液 |
| C.溶液中水的电离程度大小:a>b>c |
D.c点溶液中: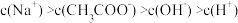 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
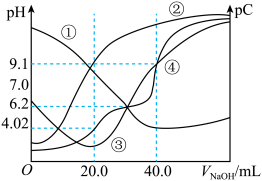
【推荐2】常温下,向 的
的 溶液中滴加
溶液中滴加 溶液,各微粒浓度和滴定曲线关系如图
溶液,各微粒浓度和滴定曲线关系如图 ,下列说法正确的是
,下列说法正确的是
 的
的 溶液中滴加
溶液中滴加 溶液,各微粒浓度和滴定曲线关系如图
溶液,各微粒浓度和滴定曲线关系如图 ,下列说法正确的是
,下列说法正确的是
A.曲线③代表 ,曲线④代表滴定曲线 ,曲线④代表滴定曲线 |
B.常温下 电离常数 电离常数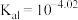 |
C.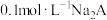 溶液 溶液 约为9.6 约为9.6 |
D. 溶液中: 溶液中: |
您最近一年使用:0次

 )或-1g[c(H+)/c(HC2O
)或-1g[c(H+)/c(HC2O )关系如图所示,下列说法错误的是
)关系如图所示,下列说法错误的是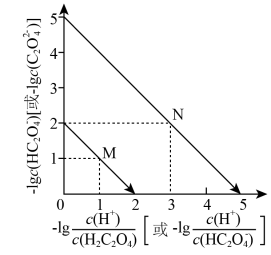
 和
和 的关系
的关系 随pH的升高而减小
随pH的升高而减小

