下列叙述不正确的是
| A.反应CaSO4(g) = CaO (g)+ SO3(g) △H>0 在高温下能自发进行 |
| B.平衡正向移动,反应物的转化率一定增大 |
| C.升高温度,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快 |
| D.当碰撞的分子具有足够的能量和适当的取向时,才能发生化学反应 |
更新时间:2021-07-15 21:39:26
|
相似题推荐
【推荐1】 与
与 的反应分两步完成,其能量曲线如下图所示。
的反应分两步完成,其能量曲线如下图所示。
反应①: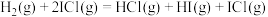
反应②:
下列有关说法不正确 的是

 与
与 的反应分两步完成,其能量曲线如下图所示。
的反应分两步完成,其能量曲线如下图所示。反应①:
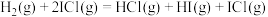
反应②:

下列有关说法

| A.反应①、②均是反应物总能量高于生成物总能量 |
| B.反应①、②均是反应物的总键能大于生成物的总键能 |
C.  |
| D.温度升高,活化分子百分数增大,反应碰撞概率增大,反应速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不 正确的是
A.已知反应2NO2(g) N2O4(g)在低温下可自发进行,则△H>0 N2O4(g)在低温下可自发进行,则△H>0 |
| B.夏天冰箱保鲜食品的原理是降低温度,减小化学反应速率 |
| C.当锌粒和稀硫酸反应制氢气时,往溶液中加少量醋酸钠固体会减缓反应 |
| D.当锌粒和盐酸反应制氢气时,往溶液中滴加少量CuSO4溶液可加快反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】硫代硫酸钠溶液与稀硫酸可发生反应:Na2S2O3 + H2SO4=Na2SO4 + SO2↑ + S↓ + H2O,某同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
设计实验如下
下列说法正确的是
设计实验如下
| 实验编号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
| ① | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ② | 25 | 5 | 0.2 | 5 | 0.1 | 10 |
| ③ | 25 | 5 | 0.1 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.2 | 5 | 0.1 | 10 |
| ⑤ | 50 | 8 | 0.1 | 5 | 0.1 | V1 |
下列说法正确的是
| A.实验①和实验④中最先出现浑浊的是实验① |
| B.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和实验④ |
| C.选择实验①和实验③,测定混合液变浑浊的时间,可探究硫酸浓度对化学反应速率的影响 |
| D.选择实验④和实验⑤,可探究Na2S2O3 的浓度对反应速率的影响,则V1=10mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关说法中正确的是
| A.影响化学反应速率的主要因素为浓度、温度、压强和催化剂 |
| B.能加快Fe与稀H2SO4反应产生H2的速率的措施可以是将稀硫酸改为98%的浓硫酸 |
C.恒温恒容时向已达平衡的2SO3(g) 2SO2(g)+O2(g)体系中充入SO3,SO3转化率将升高 2SO2(g)+O2(g)体系中充入SO3,SO3转化率将升高 |
D.压缩已达平衡的2NO2(g) N2O4(g)体系的体积,再达平衡时气体颜色比原平衡的深 N2O4(g)体系的体积,再达平衡时气体颜色比原平衡的深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于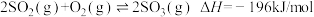 ,下列说法正确的是
,下列说法正确的是
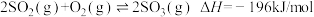 ,下列说法正确的是
,下列说法正确的是A.若反应达到平衡状态,升高温度,体系中 的含量上升 的含量上升 |
| B.若反应达到平衡状态,减小压强,正反应速率加快,逆反应速率减慢,平衡逆向移动 |
C.若反应达到平衡状态,充入 ,若容器容积恒定,则正逆反应速率不变,平衡不移动 ,若容器容积恒定,则正逆反应速率不变,平衡不移动 |
D.若反应达到平衡状态,充入 ,若容器压强恒定,则正逆反应速率均减小,平衡逆向移动 ,若容器压强恒定,则正逆反应速率均减小,平衡逆向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中,正确的是
A. 转化变为 转化变为 时,熵减小 时,熵减小 |
| B.使用催化剂能使非自发反应转化成自发反应 |
C.室温下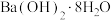 晶体与 晶体与 晶体的反应是非自发反应 晶体的反应是非自发反应 |
D.某反应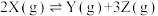 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国科研团队研究 电催化合成氨反应[
电催化合成氨反应[ △H<0]时,发现不同电解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法不正确的是
△H<0]时,发现不同电解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法不正确的是
 电催化合成氨反应[
电催化合成氨反应[ △H<0]时,发现不同电解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法不正确的是
△H<0]时,发现不同电解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法不正确的是
| A.反应放热是合成氨反应自发进行的主要助力 |
B.选用 作电解质的反应速率比选用 作电解质的反应速率比选用 的快 的快 |
C. 先吸附于催化剂表面再参加合成氨反应 先吸附于催化剂表面再参加合成氨反应 |
| D.形成Li-S键合作用时,合成氨反应的△H的绝对值较小 |
您最近一年使用:0次

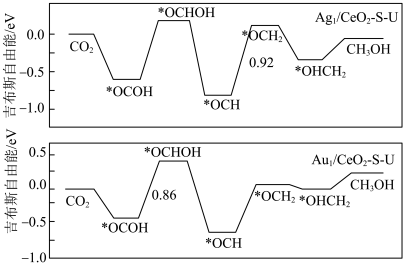
 负载的不同过渡金属催化剂上产物活性和选择性的不同进行了探究。测定
负载的不同过渡金属催化剂上产物活性和选择性的不同进行了探究。测定 在不同催化剂上发生还原反应生成
在不同催化剂上发生还原反应生成 的自由能如图所示,数字标注的为吉布斯自由能变化值。
的自由能如图所示,数字标注的为吉布斯自由能变化值。