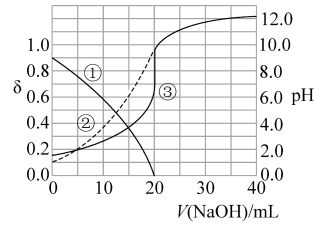
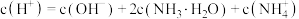次磷酸(H3PO2)是一种精细磷化工产品。常温下,某实验小组以酚酞为指示剂,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的次磷酸(H3PO2)溶液。溶液pH、所有含磷微粒的分布系数δ随滴加NaOH溶液体积V(NaOH)的变化关系如图所示[比如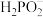 的分布系数:
的分布系数: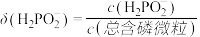 ],下列叙述正确的是
],下列叙述正确的是
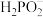 的分布系数:
的分布系数: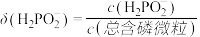 ],下列叙述正确的是
],下列叙述正确的是
A.曲线①代表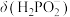 ,曲线②代表 ,曲线②代表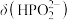 |
| B.NaH2PO2是酸式盐,其水溶液显碱性 |
C.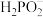 水解常数Kh≈1.0×10-9 水解常数Kh≈1.0×10-9 |
D.当滴定至中性时,溶液中存在: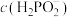 +c(H3PO2)>c(Na+) +c(H3PO2)>c(Na+) |
更新时间:2021-07-20 10:14:25
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】甘氨酸( )是人体必需氨基酸之一,在25℃时,向
)是人体必需氨基酸之一,在25℃时,向 甘氨酸水溶液中通入HCl或加入NaOH固体,当量随溶液pH变化曲线如图所示。已知:
甘氨酸水溶液中通入HCl或加入NaOH固体,当量随溶液pH变化曲线如图所示。已知: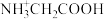 、
、 和
和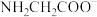 三种形式存在,且有如下平衡:
三种形式存在,且有如下平衡:
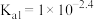 ,
,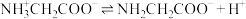
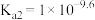 。
。
②在某pH下,溶液中甘氨酸主要以 存在,调pH值使甘氨酸整体所带的正、负电荷数目相等,此时的pH称为该氨基酸的等电点(pI)。
存在,调pH值使甘氨酸整体所带的正、负电荷数目相等,此时的pH称为该氨基酸的等电点(pI)。
下列说法正确的是
 )是人体必需氨基酸之一,在25℃时,向
)是人体必需氨基酸之一,在25℃时,向 甘氨酸水溶液中通入HCl或加入NaOH固体,当量随溶液pH变化曲线如图所示。已知:
甘氨酸水溶液中通入HCl或加入NaOH固体,当量随溶液pH变化曲线如图所示。已知: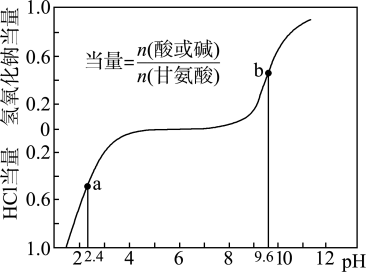
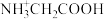 、
、 和
和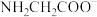 三种形式存在,且有如下平衡:
三种形式存在,且有如下平衡:
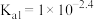 ,
,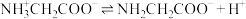
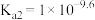 。
。②在某pH下,溶液中甘氨酸主要以
 存在,调pH值使甘氨酸整体所带的正、负电荷数目相等,此时的pH称为该氨基酸的等电点(pI)。
存在,调pH值使甘氨酸整体所带的正、负电荷数目相等,此时的pH称为该氨基酸的等电点(pI)。下列说法正确的是
A.甘氨酸的 |
B. |
C.b点NaOH当量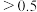 |
D.a点溶液中,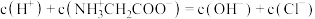 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下用0.01mol·L-1NaOH溶液滴定10mL0.01mol·L-1H2R溶液,所得溶液的pH与离子浓度变化的关系如图所示。下列说法错误的是
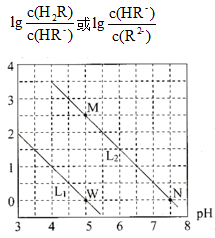

A.曲线L1表示pH与lg 的变化关系 的变化关系 |
| B.常温下H2R的第二步电离平衡常数Ka2的数量级为10-8 |
| C.水的电离程度:M>N |
| D.0.01mol·L-1H2R溶液的pH约为3.5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
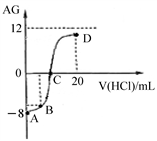
【推荐1】若用AG表示溶液的酸度,其表达式为:AG=lg[ ]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
 ]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
| A.该滴定过程可选择酚酞作为指示剂 |
| B.若B点加入的盐酸溶液体积为5 mL,所得溶液中:c(M+) + 2c(H+) = c(MOH) + 2c(OH−) |
| C.滴定过程中从A点到D点溶液中水的电离程度:A<B<C<D |
| D.C点时加入盐酸溶液的体积等于10 mL |
您最近一年使用:0次
单选题
|
较难
(0.4)
真题
名校
【推荐2】某温度下,向一定体积 0.1mol/L 醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH (pOH = -lg[OH-])与pH的变化关系如图所示,则
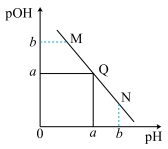

| A.M点所示溶液导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO-)>c(Na+) |
| C.M点和N点所示溶液中水的电离程度可能相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,向20 mL某浓度的硫酸溶液中滴入0.1 mol•L−1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图。下列分析不正确的是
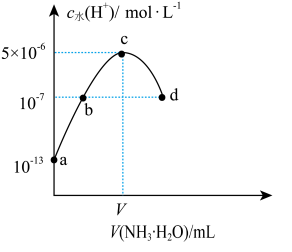

| A.V=20 |
B.b点所示溶液中:c( )>c( )>c( )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
C.d点所示溶液中:c( )+c(OH-)=2c( )+c(OH-)=2c( )+c(H+) )+c(H+) |
| D.NH3·H2O电离常数K≈1×10-5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】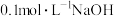 溶液与盐酸酸化的
溶液与盐酸酸化的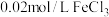 溶液滴定时t-pH曲线如图所示(已知
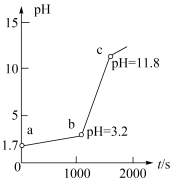
溶液滴定时t-pH曲线如图所示(已知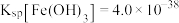 ,
, )。下列说法正确的是
)。下列说法正确的是
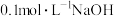 溶液与盐酸酸化的
溶液与盐酸酸化的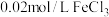 溶液滴定时t-pH曲线如图所示(已知
溶液滴定时t-pH曲线如图所示(已知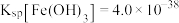 ,
, )。下列说法正确的是
)。下列说法正确的是
A.如图为 溶液滴定 溶液滴定 溶液的t-pH曲线 溶液的t-pH曲线 |
B.由曲线上a点 ,可计算室温下 ,可计算室温下 的水解常数 的水解常数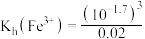 |
C.曲线上b点表示 恰好沉淀完全 恰好沉淀完全 |
D.c点存在关系: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下向20mL0.10mol/LCH3COOH溶液中滴加0.10mol/ L NaOH溶液时,混合溶液的pH与相关微粒的浓度关系如图所示。已知:pKa=-lgKa。下列说法不正确的是
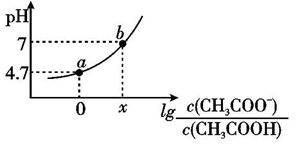

A.CH3COOH溶液中存在如下平衡:CH3COOH H++CH3COO- H++CH3COO- |
| B.b点,加入NaOH溶液的体积小于20mL |
| C.将等物质的量的CH3COOH和CH3 COONa一起溶于蒸馏水中,得到对应a点的溶液 |
| D.常温下,CH3COOH的电离常数为Ka,则pKa=4.7 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】取0.2 mol / L HX溶液与0.2 mol / L NaOH溶液等体积混合(忽略混合后溶液体积变化),测得混合溶液的pH = 8,则下列说法正确的是
| A.混合溶液中由水电离出的c (OH-)小于0.2 mol / LHX溶液中由水电离出的c(H+) |
| B.c (Na+) =" c" (X-) + c (HX) =" 0.2" mol / L |
| C.c (Na+) — c (X-) = 9.9×10-7mol /L |
| D.c (OH-) — c (HX) = c(H+) = 10-8 mol / L |
您最近一年使用:0次

 溶液滴定二元弱酸
溶液滴定二元弱酸 溶液,图中直线①表示溶液中
溶液,图中直线①表示溶液中 和
和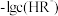 的关系,直线②表示
的关系,直线②表示 和
和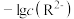 的关系。下列说法错误的是
的关系。下列说法错误的是
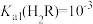
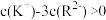
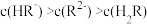 ,则pH范围为
,则pH范围为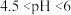
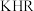 的溶液中:
的溶液中: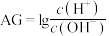 ,室温下用0.1
,室温下用0.1 的HCl溶液滴定10.00mL 0.1
的HCl溶液滴定10.00mL 0.1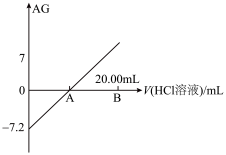

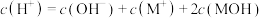
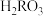 溶液中,混合溶液中
溶液中,混合溶液中 或
或 与pH的关系如图所示。下列叙述正确的是
与pH的关系如图所示。下列叙述正确的是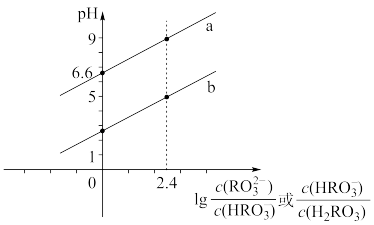
 的数量级为
的数量级为
 时,酸碱恰好完全反应
时,酸碱恰好完全反应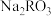 溶液和
溶液和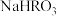 溶液混合后,溶液中
溶液混合后,溶液中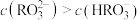
 的稀硫酸逐滴滴入
的稀硫酸逐滴滴入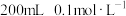 的稀氨水中,下列说法错误的是
的稀氨水中,下列说法错误的是 时,
时,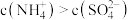
 时溶液呈碱性,则
时溶液呈碱性,则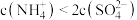
 时,
时,