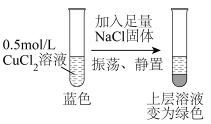
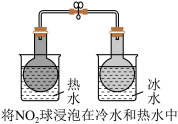
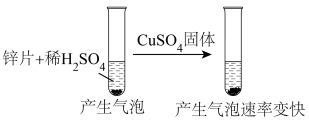
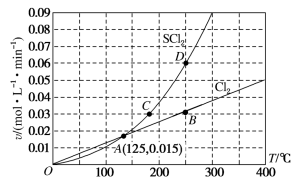
一定压强下,向10L密闭容器中充入1molS2Cl2和1molCl2,发生反应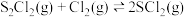 。Cl2与SCl2的消耗速率(
。Cl2与SCl2的消耗速率( )与温度(T)的关系如图,以下说法正确的是
)与温度(T)的关系如图,以下说法正确的是
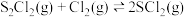 。Cl2与SCl2的消耗速率(
。Cl2与SCl2的消耗速率( )与温度(T)的关系如图,以下说法正确的是
)与温度(T)的关系如图,以下说法正确的是
| A.该反应是吸热反应 |
| B.A、B、C、D四点对应状态下,达到平衡状态的为B点、D点 |
| C.一定温度下,在密闭容器中达到平衡后缩小容器体积,重新达到平衡后,S2Cl2的平衡转化率减小 |
| D.达到平衡后再加热,平衡向正反应方向移动 |
更新时间:2021-10-14 17:08:14
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,将 和
和 充入
充入 密闭容器中发生反应:
密闭容器中发生反应: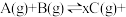
 ,在
,在 时达到平衡。在
时达到平衡。在 、
、 时分别改变反应的一个条件,测得容器中
时分别改变反应的一个条件,测得容器中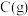 的浓度随时间变化情况如图所示。
的浓度随时间变化情况如图所示。
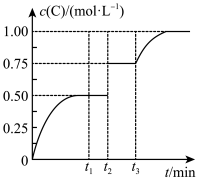
下列有关说法正确的是
 和
和 充入
充入 密闭容器中发生反应:
密闭容器中发生反应: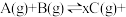
 ,在
,在 时达到平衡。在
时达到平衡。在 、
、 时分别改变反应的一个条件,测得容器中
时分别改变反应的一个条件,测得容器中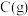 的浓度随时间变化情况如图所示。
的浓度随时间变化情况如图所示。
下列有关说法正确的是
A. |
B.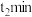 时改变的条件是使用催化剂 时改变的条件是使用催化剂 |
C. 时改变的条件是只增大生成物C的浓度 时改变的条件是只增大生成物C的浓度 |
D. 、 、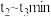 阶段反应的平衡常数均为4 阶段反应的平衡常数均为4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对机动车尾气中的NO进行处理,可以保护环境,减少污染。研究表明使用乙醇汽油并不能减少NO的排放量。某研究小组在实验室对机动车尾气以耐高温试剂Ag-ZSW-5催化,测得NO转化为N2的转化率随反应温度的变化如图所示。下列有关说法正确的是


| A.NO直接分解为N2的反应为吸热反应 |
| B.增大压强,可提高NO还原为N2的平衡转化率 |
| C.使用催化剂,可提高NO还原为N2的平衡转化率 |
| D.汽缸中吸入足量空气使汽油完全燃烧,可以减少尾气中的NO排放 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】合成尿素[CO(NH2)2]是利用CO2的途径之一。将NH3和CO2按照2∶1的比例通入到恒容反应容器中,通过下列反应合成尿素。
反应Ⅰ:2NH3(g)+CO2(g) NH2COONH4(l) △H=-159.5 kJ/mol
NH2COONH4(l) △H=-159.5 kJ/mol
反应Ⅱ:NH2COONH4(l) CO(NH2)2(1)+H2O(l) △H =72.5 kJ/mol
CO(NH2)2(1)+H2O(l) △H =72.5 kJ/mol
下列说法正确的是
反应Ⅰ:2NH3(g)+CO2(g)
 NH2COONH4(l) △H=-159.5 kJ/mol
NH2COONH4(l) △H=-159.5 kJ/mol反应Ⅱ:NH2COONH4(l)
 CO(NH2)2(1)+H2O(l) △H =72.5 kJ/mol
CO(NH2)2(1)+H2O(l) △H =72.5 kJ/mol下列说法正确的是
| A.高温有利于反应Ⅰ自发进行 |
| B.NH3的体积分数不再改变,不能说明反应I达到了平衡状态 |
| C.将2molNH3和1molCO2充入反应I的平衡体系中,再次达到平衡时,c(NH3)增大 |
| D.增大压强,对于尿素的合成没有影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一密闭容器中,发生某反应,反应达到平衡后,该反应的平衡常数表达式为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.仅升高温度, 的浓度增大,则该反应的 的浓度增大,则该反应的 |
B.增大体积减小压强, 的物质的量浓度减小 的物质的量浓度减小 |
| C.当混合气体的质量不再改变时,该反应达到平衡 |
D.该反应的化学方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ΔH<0,若反应物的起始物质的量相同,下列关于该反应的示意图不正确的是
4NO(g)+6H2O(g) ΔH<0,若反应物的起始物质的量相同,下列关于该反应的示意图不正确的是
 4NO(g)+6H2O(g) ΔH<0,若反应物的起始物质的量相同,下列关于该反应的示意图不正确的是
4NO(g)+6H2O(g) ΔH<0,若反应物的起始物质的量相同,下列关于该反应的示意图不正确的是A.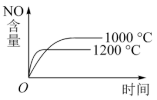 | B.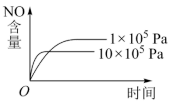 |
C.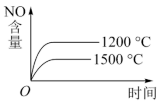 | D.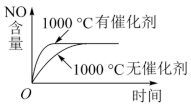 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知升高温度时,速率常数(k)总是增大,因此绝大多数的化学反应速率增大。但是2NO(g)+O2(g) 2NO2(g)的速率却随着温度升高而减小,已知该反应历程分两步:I.2NO(g)
2NO2(g)的速率却随着温度升高而减小,已知该反应历程分两步:I.2NO(g) N2O2(g)(快)ΔH1<0,v1正=k1正c2(NO)、v1逆=k1逆c(N2O2);II.N2O2(g)+O2(g)
N2O2(g)(快)ΔH1<0,v1正=k1正c2(NO)、v1逆=k1逆c(N2O2);II.N2O2(g)+O2(g) 2NO2(g)(慢) ΔH2<0,v2正=k2正c(N2O2)c(O2)、v2逆=k2逆c2(NO2),试分析升高温度该反应速率减小的原因是
2NO2(g)(慢) ΔH2<0,v2正=k2正c(N2O2)c(O2)、v2逆=k2逆c2(NO2),试分析升高温度该反应速率减小的原因是
 2NO2(g)的速率却随着温度升高而减小,已知该反应历程分两步:I.2NO(g)
2NO2(g)的速率却随着温度升高而减小,已知该反应历程分两步:I.2NO(g) N2O2(g)(快)ΔH1<0,v1正=k1正c2(NO)、v1逆=k1逆c(N2O2);II.N2O2(g)+O2(g)
N2O2(g)(快)ΔH1<0,v1正=k1正c2(NO)、v1逆=k1逆c(N2O2);II.N2O2(g)+O2(g) 2NO2(g)(慢) ΔH2<0,v2正=k2正c(N2O2)c(O2)、v2逆=k2逆c2(NO2),试分析升高温度该反应速率减小的原因是
2NO2(g)(慢) ΔH2<0,v2正=k2正c(N2O2)c(O2)、v2逆=k2逆c2(NO2),试分析升高温度该反应速率减小的原因是| A.k2正增大,c(N2O2)增大 | B.k2正减小,c(N2O2)减小 |
| C.k2正增大,c(N2O2)减小 | D.k2正减小,c(N2O2)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下,向容积为5L的恒容密闭容器中充入4molP和8molQ,发生反应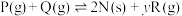
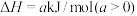 。反应过程中测得气体P的物质的量浓度变化如图所示。已知反应进行到8min时达到平衡状态,若平衡后升高温度,混合气体的平均相对分子质量将增大(y为正整数),下列说法正确的是
。反应过程中测得气体P的物质的量浓度变化如图所示。已知反应进行到8min时达到平衡状态,若平衡后升高温度,混合气体的平均相对分子质量将增大(y为正整数),下列说法正确的是
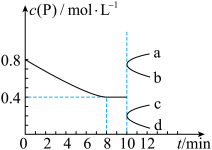
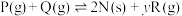
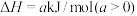 。反应过程中测得气体P的物质的量浓度变化如图所示。已知反应进行到8min时达到平衡状态,若平衡后升高温度,混合气体的平均相对分子质量将增大(y为正整数),下列说法正确的是
。反应过程中测得气体P的物质的量浓度变化如图所示。已知反应进行到8min时达到平衡状态,若平衡后升高温度,混合气体的平均相对分子质量将增大(y为正整数),下列说法正确的是
| A.该反应中,化学计量数y=3 |
B.8min时,该反应的平衡常数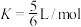 |
| C.反应达到平衡后,向该容器中加入适量P达到新平衡后,平衡常数增大 |
| D.10min时,仅将容器容积缩小至原来的两倍,则气体P的物质的量浓度的变化曲线为d |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定量混合物在密闭容器中发生反应:mA(g)+nB(g) pC(g)达平衡后,将气体体积缩小到原来的1/2,当达到新的平衡时,B物质的浓度为原来的1.9倍,若压缩过程中保持温度不变,则下列说法正确的是
pC(g)达平衡后,将气体体积缩小到原来的1/2,当达到新的平衡时,B物质的浓度为原来的1.9倍,若压缩过程中保持温度不变,则下列说法正确的是
 pC(g)达平衡后,将气体体积缩小到原来的1/2,当达到新的平衡时,B物质的浓度为原来的1.9倍,若压缩过程中保持温度不变,则下列说法正确的是
pC(g)达平衡后,将气体体积缩小到原来的1/2,当达到新的平衡时,B物质的浓度为原来的1.9倍,若压缩过程中保持温度不变,则下列说法正确的是| A.m+n<p | B.平衡向逆反应方向移动 | C.A的转化率降低 | D.C的体积分数增大 |
您最近一年使用:0次


 在容积可变的容器中进行,不能说明该反应已达到平衡状态的是
在容积可变的容器中进行,不能说明该反应已达到平衡状态的是