某科研课题小组研究利用含H+、Na+、Zn2+、Mn2+、Fe2+、Fe3+、SO 的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
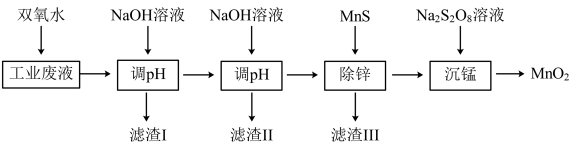
回答下列问题:
(1)加入双氧水的目的是___ 。
(2)第一次调pH使Fe3+完全沉淀,写出反应的离子方程___ 。
(3)第二次调pH前,科研小组成员分析此时的溶液,得到常温下相关数据如表(表中金属离子沉淀完全时,其浓度为1×10-5mol·L-1)。
为防止Mn2+同时沉淀造成产品不纯,最终选择将溶液的pH控制为7,则此时溶液中Zn2+的沉淀率为___ ,利用滤渣Ⅱ制备高纯的ZnO时,必然含有极其微量的___ (以化学式表示)。
(4)已知常温下,Ksp(MnS)=3.0×10-14,Ksp(ZnS)=1.5×10-24,在除锌时发生沉淀转化反应为:MnS(s)+Zn2+(aq) ZnS(s)+Mn2+(aq),其平衡常数K=
ZnS(s)+Mn2+(aq),其平衡常数K=___ 。(填数值)
(5)沉锰反应在酸性条件下完成,写出该反应的离子方程式___ 。
 的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
回答下列问题:
(1)加入双氧水的目的是
(2)第一次调pH使Fe3+完全沉淀,写出反应的离子方程
(3)第二次调pH前,科研小组成员分析此时的溶液,得到常温下相关数据如表(表中金属离子沉淀完全时,其浓度为1×10-5mol·L-1)。
| 浓度/(mol·L-1) | 氢氧化物的Ksp | 开始沉淀的pH | 沉淀完全的pH | |
| Zn2+ | 0.12 | 1.2×10-17 | 6.0 | 8.1 |
| Mn2+ | 0.10 | 4.0×10-14 | 7.8 | 9.8 |
(4)已知常温下,Ksp(MnS)=3.0×10-14,Ksp(ZnS)=1.5×10-24,在除锌时发生沉淀转化反应为:MnS(s)+Zn2+(aq)
 ZnS(s)+Mn2+(aq),其平衡常数K=
ZnS(s)+Mn2+(aq),其平衡常数K=(5)沉锰反应在酸性条件下完成,写出该反应的离子方程式
更新时间:2021-10-15 13:20:10
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氯气是一种重要的化工原材料,常用于制备盐酸、漂白液、农药和药品等。某小组为了制备源白液(主要成分 ),并探究氯气的主要性质,设计了如下实验装置。并查阅到下列资料:“
),并探究氯气的主要性质,设计了如下实验装置。并查阅到下列资料:“ 与水的反应是放热反应。在加热条件下
与水的反应是放热反应。在加热条件下 与碱液发生:
与碱液发生: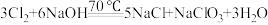
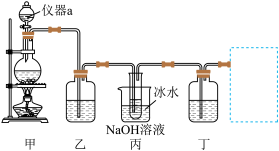
(1)仪器a的名称是___________ ,写出装置甲中发生的化学反应方程式___________ 。
(2)装置乙的作用是提纯 ,装有的试剂是
,装有的试剂是___________ ,装置乙不能省去,原因是___________ 。
(3)丙中冰水浴的作用是___________ 。
(4)欲验证 与水反应所得的溶液既有酸性、又有漂白性,装置丁盛放的试剂是
与水反应所得的溶液既有酸性、又有漂白性,装置丁盛放的试剂是___________ ,现象是___________ 。
(5)在虚线框中可以使用下列的装置是___________
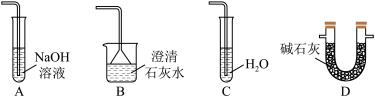
(6)常温下,在 溶液中滴加浓盐酸,也可以制备
溶液中滴加浓盐酸,也可以制备 ,该氧化还原反应中包含下列几种微粒:
,该氧化还原反应中包含下列几种微粒: ,写出上述的化学反应方程式并配平
,写出上述的化学反应方程式并配平___________ 。在该反应中,表现酸性和还原性的 质量比是
质量比是___________ 。
 ),并探究氯气的主要性质,设计了如下实验装置。并查阅到下列资料:“
),并探究氯气的主要性质,设计了如下实验装置。并查阅到下列资料:“ 与水的反应是放热反应。在加热条件下
与水的反应是放热反应。在加热条件下 与碱液发生:
与碱液发生: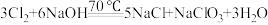

(1)仪器a的名称是
(2)装置乙的作用是提纯
 ,装有的试剂是
,装有的试剂是(3)丙中冰水浴的作用是
(4)欲验证
 与水反应所得的溶液既有酸性、又有漂白性,装置丁盛放的试剂是
与水反应所得的溶液既有酸性、又有漂白性,装置丁盛放的试剂是(5)在虚线框中可以使用下列的装置是

(6)常温下,在
 溶液中滴加浓盐酸,也可以制备
溶液中滴加浓盐酸,也可以制备 ,该氧化还原反应中包含下列几种微粒:
,该氧化还原反应中包含下列几种微粒: ,写出上述的化学反应方程式并配平
,写出上述的化学反应方程式并配平 质量比是
质量比是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为生产自来水的消毒剂。回答下列问题:
I.ClO2的制备,生产流程如下图所示:
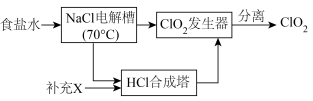
(1)用于电解的食盐水需先除去其中的 等杂质。向粗盐水中依次中加入过量的
等杂质。向粗盐水中依次中加入过量的___________ (填化学式)溶液、过量的 溶液和过量的
溶液和过量的___________ (填化学式)溶液,过滤后向滤液中加入盐酸至溶液呈中性。
(2)将经过净化后的食盐水加入电解槽中,70℃左右电解得到 和一种气体,则
和一种气体,则 合成塔中还需要补充的物质X为
合成塔中还需要补充的物质X为___________ (填化学式)。
(3)ClO2发生器中发生的反应为: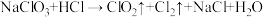 (反应未配平)。
(反应未配平)。
① 在该反应中表现的性质是
在该反应中表现的性质是___________ 。
②配平该反应的化学方程式,并用单线桥法标出电子转移的数目 ___________ 。
II.探究ClO2的某些性质,装置如下图所示:
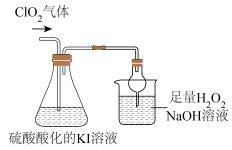
已知:①ClO2是极易溶于水的气体:②I2遇淀粉溶液变为蓝色
(4)反应结束后,往锥形瓶内滴加淀粉溶液,溶液变为蓝色,写出ClO2通入锥形瓶中反应的离子方程式___________ 。
(5)上图装置中,球形干燥管的作用是___________ 。烧杯内液体用于吸收未反应的CO2,若反应的氧化产物是 ,且氧化剂与还原剂的个数之比是
,且氧化剂与还原剂的个数之比是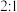 ,则还原产物是
,则还原产物是___________ (填化学式)。
I.ClO2的制备,生产流程如下图所示:

(1)用于电解的食盐水需先除去其中的
 等杂质。向粗盐水中依次中加入过量的
等杂质。向粗盐水中依次中加入过量的 溶液和过量的
溶液和过量的(2)将经过净化后的食盐水加入电解槽中,70℃左右电解得到
 和一种气体,则
和一种气体,则 合成塔中还需要补充的物质X为
合成塔中还需要补充的物质X为(3)ClO2发生器中发生的反应为:
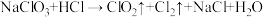 (反应未配平)。
(反应未配平)。①
 在该反应中表现的性质是
在该反应中表现的性质是②配平该反应的化学方程式,
II.探究ClO2的某些性质,装置如下图所示:

已知:①ClO2是极易溶于水的气体:②I2遇淀粉溶液变为蓝色
(4)反应结束后,往锥形瓶内滴加淀粉溶液,溶液变为蓝色,写出ClO2通入锥形瓶中反应的离子方程式
(5)上图装置中,球形干燥管的作用是
 ,且氧化剂与还原剂的个数之比是
,且氧化剂与还原剂的个数之比是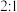 ,则还原产物是
,则还原产物是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氮化锂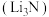 是一种重要的化工试剂,在空气中易潮解。实验室制备
是一种重要的化工试剂,在空气中易潮解。实验室制备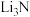 的原理是
的原理是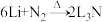 。某实验小组拟设计实验制备
。某实验小组拟设计实验制备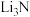 并探究其性质。(装置可重复使用)
并探究其性质。(装置可重复使用)
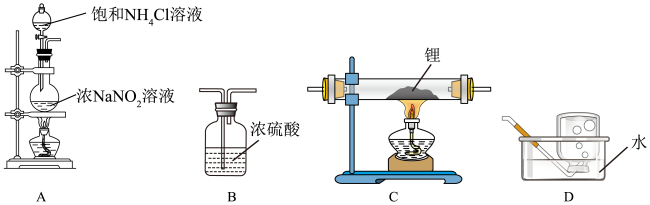
回答下列问题:
(1)装饱和 溶液的仪器是
溶液的仪器是______________ (填名称)。
(2)B装置的作用是______________ 。
(3)气流从左至右,装置的连接顺序为
______________ 。
(4)实验时,先点燃______________ (填“A处”或“C处”)酒精灯。
(5)A装置中制备 的反应的化学方程式为
的反应的化学方程式为______________ 。
(6)如果氮化锂产品中混有 ,可能的原因是
,可能的原因是______________ 。
(7)取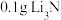 粗产品于试管中,向试管中滴加蒸馏水,有气体产生,同时溶液呈碱性。
粗产品于试管中,向试管中滴加蒸馏水,有气体产生,同时溶液呈碱性。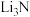 与水反应的化学方程式为
与水反应的化学方程式为______________ 。
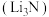 是一种重要的化工试剂,在空气中易潮解。实验室制备
是一种重要的化工试剂,在空气中易潮解。实验室制备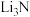 的原理是
的原理是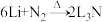 。某实验小组拟设计实验制备
。某实验小组拟设计实验制备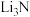 并探究其性质。(装置可重复使用)
并探究其性质。(装置可重复使用)
回答下列问题:
(1)装饱和
 溶液的仪器是
溶液的仪器是(2)B装置的作用是
(3)气流从左至右,装置的连接顺序为

(4)实验时,先点燃
(5)A装置中制备
 的反应的化学方程式为
的反应的化学方程式为(6)如果氮化锂产品中混有
 ,可能的原因是
,可能的原因是(7)取
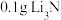 粗产品于试管中,向试管中滴加蒸馏水,有气体产生,同时溶液呈碱性。
粗产品于试管中,向试管中滴加蒸馏水,有气体产生,同时溶液呈碱性。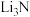 与水反应的化学方程式为
与水反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】请完成下列填空:
(1)还原剂肼( )与氧化剂
)与氧化剂 混合极易发生反应,生成气态水和氮气。已知:①使
混合极易发生反应,生成气态水和氮气。已知:①使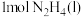 和
和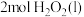 转化为
转化为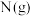 、
、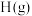 、
、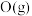 需要吸收
需要吸收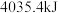 热量,破坏
热量,破坏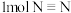 键需吸收
键需吸收 热量;②
热量;②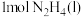 与
与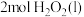 完全反应生成气态水和氮气的能量变化如图所示:
完全反应生成气态水和氮气的能量变化如图所示:

①该反应的热化学方程式为___________ 。
②断开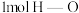 键吸收的热量为
键吸收的热量为___________  。
。
(2)25℃时,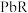 (
( 为
为 或
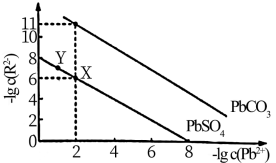
或 )的沉淀溶解平衡关系如图所示。
)的沉淀溶解平衡关系如图所示。
①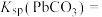
___________ 。
②向X点对应的饱和溶液中加入少量 固体,
固体,___________ (填“能”或“不能”)转化为Y点对应的溶液。
③当 和
和 沉淀共存时,溶液中
沉淀共存时,溶液中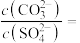
___________ 。
(1)还原剂肼(
 )与氧化剂
)与氧化剂 混合极易发生反应,生成气态水和氮气。已知:①使
混合极易发生反应,生成气态水和氮气。已知:①使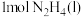 和
和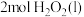 转化为
转化为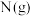 、
、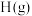 、
、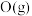 需要吸收
需要吸收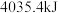 热量,破坏
热量,破坏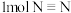 键需吸收
键需吸收 热量;②
热量;②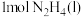 与
与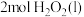 完全反应生成气态水和氮气的能量变化如图所示:
完全反应生成气态水和氮气的能量变化如图所示:
①该反应的热化学方程式为
②断开
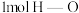 键吸收的热量为
键吸收的热量为 。
。(2)25℃时,
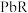 (
( 为
为 或
或 )的沉淀溶解平衡关系如图所示。
)的沉淀溶解平衡关系如图所示。
①
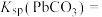
②向X点对应的饱和溶液中加入少量
 固体,
固体,③当
 和
和 沉淀共存时,溶液中
沉淀共存时,溶液中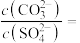
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)可逆反应FeO(s)+CO(g) Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
①写出该反应平衡常数的表达式________ 。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量________ ;充入氦气,混合气体的密度________ (填“增大”“减小”或“不变”)。
(2)常温下,浓度均为0.1mol·L-1的下列六种溶液的pH如下表:
①根据表中数据判断,浓度均为0.01mol·L-1的下列四种物质的溶液中,酸性最强的是________ (填编号)。
A.HCNB.HClOC.H2CO3D.CH3COOH
②据上表数据,请你判断下列反应不能成立的是________ (填编号)。
A.CH3COOH+Na2CO3===NaHCO3+CH3COONa
B.CH3COOH+NaCN===CH3COONa+HCN
C.CO2+H2O+2NaClO===Na2CO3+2HClO
(3)泡沫灭火剂中装有Al2(SO4)3溶液、NaHCO3溶液及起泡剂,写出使用时发生反应的离子方程式_______________________________________________________
(4)写出难溶电解质的溶度积表达式,Mg(OH)2:____________ ;在Mg(OH)2悬浊液中加入MgCl2固体,平衡________ 移动(填“正向”“逆向”或“不”),Ksp________ (填“增大”“减小”或“不变”)。
(5)1g固体炭与水蒸气反应生成CO气体和H2气体,需吸收akJ热量,此反应的热化学方程式为____________________________________
 Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:| T/K | 938 | 1100 |
| K | 0.68 | 0.40 |
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量
(2)常温下,浓度均为0.1mol·L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCNB.HClOC.H2CO3D.CH3COOH
②据上表数据,请你判断下列反应不能成立的是
A.CH3COOH+Na2CO3===NaHCO3+CH3COONa
B.CH3COOH+NaCN===CH3COONa+HCN
C.CO2+H2O+2NaClO===Na2CO3+2HClO
(3)泡沫灭火剂中装有Al2(SO4)3溶液、NaHCO3溶液及起泡剂,写出使用时发生反应的离子方程式
(4)写出难溶电解质的溶度积表达式,Mg(OH)2:
(5)1g固体炭与水蒸气反应生成CO气体和H2气体,需吸收akJ热量,此反应的热化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】工业上以锂辉石(Li2O·A12O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:

已知:①Li2O·Al2O3·4SiO2+H2SO4(浓) =Li2SO4+Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示。
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是____________________________________________________________________ 。
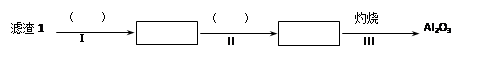
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。
向滤液1中加入石灰乳的作用是(运用化学平衡移动原理解释)__________________________________________________ 。
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是________________________________________________________ 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
① a中,阳极的电极反应式是_____________________________ 。
②b中,生成Li2CO3反应的化学方程式是__________________________________ 。

已知:①Li2O·Al2O3·4SiO2+H2SO4(浓) =Li2SO4+Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示。
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是
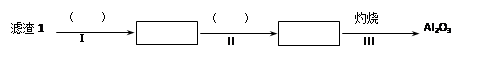
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。
向滤液1中加入石灰乳的作用是(运用化学平衡移动原理解释)
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
① a中,阳极的电极反应式是
②b中,生成Li2CO3反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为 和
和 还有少量
还有少量 、FeO、CaO、
、FeO、CaO、 和
和 等)为原料制备硼酸(
等)为原料制备硼酸( )的工艺流程如图所示:
)的工艺流程如图所示:
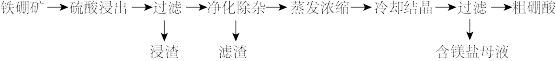
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表(室温下):
回答下列问题:
(1)“硫酸浸出”时,常将铁硼矿粉碎,其目的是___________ 。
(2)“净化除杂”时:
①首先需通入过量的 ,其目的是
,其目的是___________ 。
②其次调节溶液的pH约为5,“滤渣”的主要成分为___________ (填化学式)。
③室温下,依据表中提供的数据求出
___________ 。
(3)室温下, 为一元弱酸,可用于中和溅在皮肤上的NaOH溶液,
为一元弱酸,可用于中和溅在皮肤上的NaOH溶液, 的
的 的pH约为
的pH约为___________ (已知:室温下, ,lg2≈0.3,lg3≈0.5)。
,lg2≈0.3,lg3≈0.5)。
 和
和 还有少量
还有少量 、FeO、CaO、
、FeO、CaO、 和
和 等)为原料制备硼酸(
等)为原料制备硼酸( )的工艺流程如图所示:
)的工艺流程如图所示: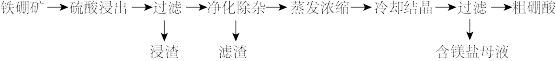
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表(室温下):
| 金属离子 |  |  |  |  |  |
开始沉淀(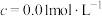 )的pH )的pH | 2.2 | 3.7 | 9.5 | 12.3 | 6.3 |
沉淀完全( )的pH )的pH | 3.2 | 4.7 | 11.0 | 13.8 | 8.3 |
(1)“硫酸浸出”时,常将铁硼矿粉碎,其目的是
(2)“净化除杂”时:
①首先需通入过量的
 ,其目的是
,其目的是②其次调节溶液的pH约为5,“滤渣”的主要成分为
③室温下,依据表中提供的数据求出

(3)室温下,
 为一元弱酸,可用于中和溅在皮肤上的NaOH溶液,
为一元弱酸,可用于中和溅在皮肤上的NaOH溶液, 的
的 的pH约为
的pH约为 ,lg2≈0.3,lg3≈0.5)。
,lg2≈0.3,lg3≈0.5)。
您最近一年使用:0次
【推荐2】用锑砷烟灰(主要成分为Sb2O3、As2O3,含Pb、Ag、Cu等元素)制取焦锑酸钠[NaSb(OH)6]和砷酸钠(Na3AsO4),不仅治理了砷害污染,还可综合回收其它有价金属。其工艺流程如图所示:
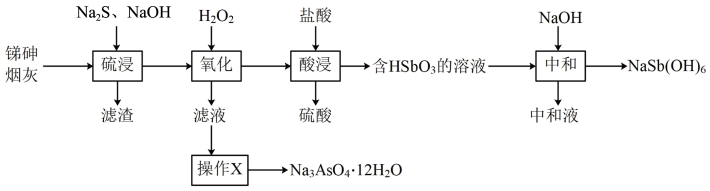
已知:
①Ag、Cu、Fe的氧化物不溶于Na2S溶液
②硫浸后,锑砷以Na3SbS3、Na3AsS3存在;
③NaSb(OH)6易溶于热水,难溶于冷水,不溶于乙醇。
回答下列问题:
(1)“硫浸”时,Sb2O3溶解的离子方程式为___ 。
(2)用NaNO3和NaOH浸取锑砷烟灰也可得到Na3SbO4,其缺陷是__ 。
(3)“氧化”时所用H2O2的电子式为___ ,反应温度不宜太高的原因是___ 。
(4)“中和”时,生成NaSb(OH)6的化学方程式为___ ,操作X为__ 、过滤、洗涤、干燥。
(5)As2O3对应的酸为H3AsO3,测得某工业酸性废液中含H3AsO3和Fe2+,其浓度如表:
已知:Ksp(FeAsO3)>Ksp(FeAsO4)=5.70×10-21,H3AsO3的还原性比Fe2+强。
根据题目信息,则可采用__ 方法除去该废水中的砷,除去砷后的废液中c(AsO )=
)=__ mol·L-1(不考虑反应过程中溶液体积的微小变化)

已知:
①Ag、Cu、Fe的氧化物不溶于Na2S溶液
②硫浸后,锑砷以Na3SbS3、Na3AsS3存在;
③NaSb(OH)6易溶于热水,难溶于冷水,不溶于乙醇。
回答下列问题:
(1)“硫浸”时,Sb2O3溶解的离子方程式为
(2)用NaNO3和NaOH浸取锑砷烟灰也可得到Na3SbO4,其缺陷是
(3)“氧化”时所用H2O2的电子式为
(4)“中和”时,生成NaSb(OH)6的化学方程式为
(5)As2O3对应的酸为H3AsO3,测得某工业酸性废液中含H3AsO3和Fe2+,其浓度如表:
| 物质 | H3AsO3 | Fe2+ |
| 浓度/g·L-1 | 0.378 | 0.840 |
根据题目信息,则可采用
 )=
)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝(Al)、钼(Mo)、镍(Ni)等元素的氧化物,一种回收利用工艺的部分流程如下:
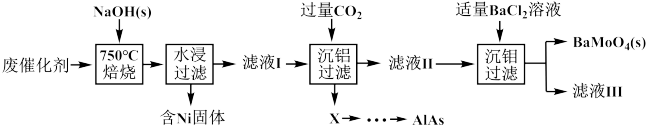
已知:25℃时,H2CO3的Ka1=4.5 × 10-7,Ka2=4.7 × 10-11;Ksp(BaMoO4)=3.5 × 10-8;Ksp(BaCO3)=2.6 × 10-9;该工艺中,pH>6.0时,溶液中Mo元素以MoO 的形态存在。
的形态存在。
(1)“焙烧”中,有Na2MoO4生成,其中Mo元素的化合价为___________ 。
(2)“沉铝”中,生成的沉淀X为___________ 。
(3)“沉钼”中,pH为7.0。
①生成BaMoO4的离子方程式为___________ 。
②若条件控制不当,BaCO3也会沉淀。为避免BaMoO4中混入BaCO3沉淀,溶液中c( ):c(MoO
):c(MoO )=
)=___________ (列出算式)时,应停止加入BaCl2溶液。
(4)①滤液III中,主要存在的钠盐有NaCl和Y,Y为___________ 。
②往滤液III中添加适量NaCl固体后,通入足量___________ (填化学式)气体,再通入足量CO2,可析出Y

已知:25℃时,H2CO3的Ka1=4.5 × 10-7,Ka2=4.7 × 10-11;Ksp(BaMoO4)=3.5 × 10-8;Ksp(BaCO3)=2.6 × 10-9;该工艺中,pH>6.0时,溶液中Mo元素以MoO
 的形态存在。
的形态存在。(1)“焙烧”中,有Na2MoO4生成,其中Mo元素的化合价为
(2)“沉铝”中,生成的沉淀X为
(3)“沉钼”中,pH为7.0。
①生成BaMoO4的离子方程式为
②若条件控制不当,BaCO3也会沉淀。为避免BaMoO4中混入BaCO3沉淀,溶液中c(
 ):c(MoO
):c(MoO )=
)=(4)①滤液III中,主要存在的钠盐有NaCl和Y,Y为
②往滤液III中添加适量NaCl固体后,通入足量
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下所示:(已知:硫不溶于水,微溶于酒精,易溶于二硫化碳、四氯化碳和苯。)
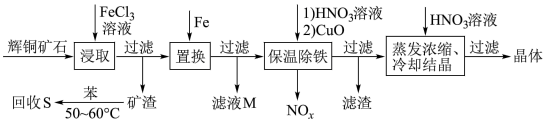
(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:____________ 。
(2)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是_____________________ 。
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为_________________ 。向“滤液M”中加入(或通入)____ (填字母),可得到另一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾
(4)“保温除铁”过程中,加入CuO的目的是__________________ ;“蒸发浓缩、冷却结晶”过程中,加入HNO3调节溶液的pH,其理由是___________ 。
(5)洗涤硝酸铜晶体的洗涤剂可以使用下列物质中的______________ 。
a.酒精 b.热水 c.饱和硝酸铜溶液

(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:
(2)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为
a.铁 b.氯气 c.高锰酸钾
(4)“保温除铁”过程中,加入CuO的目的是
(5)洗涤硝酸铜晶体的洗涤剂可以使用下列物质中的
a.酒精 b.热水 c.饱和硝酸铜溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】MnSO4·H2O可用作分析试剂、媒染剂、添加剂、药用辅料等。一种以软锰矿(主要成分为MnO2,还有CaO、Al2O3、SiO2等杂质)为原料制备MnSO4·H2O的工艺流程如图所示。
②该工艺条件下,有关金属离子沉淀的pH范围如下表所示。
回答下列问题:
(1)“酸浸”时,MnO2被Fe2+还原,写出基态Fe2+的价电子轨道表示式___________ 。
(2)“酸浸”得到的滤渣1需要进行二次酸浸,然后将浸出液合并。二次酸浸的目的是___________ 。
(3)“氧化”时,试剂A可以是___________ (填写试剂化学式)。
(4)“除铁铝”时,应调节溶液pH的范围是___________ 。
(5)“除钙”时,加入MnF2,发生反应的离子方程式是___________ 。在25℃时该反应的平衡常数K=___________ 。
(6)硫酸锰在不同温度下的溶解度S和一定温度内析出晶体的组成如图所示。“一系列操作”包括将所得滤液控制温度在80~90℃之间蒸发结晶、___________ 、___________ 、真空干燥,最后得到MnSO4·H2O。___________ (写出一种)。
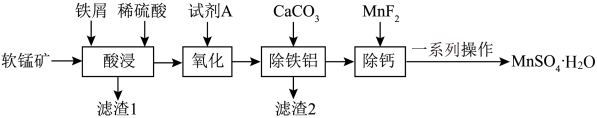
②该工艺条件下,有关金属离子沉淀的pH范围如下表所示。
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
| 开始沉淀的pH | 1.9 | 7.0 | 3.4 | 8.1 |
| 沉淀完全的pH | 3.2 | 9.0 | 4.7(>9.8时开始溶解) | 10.1 |
(1)“酸浸”时,MnO2被Fe2+还原,写出基态Fe2+的价电子轨道表示式
(2)“酸浸”得到的滤渣1需要进行二次酸浸,然后将浸出液合并。二次酸浸的目的是
(3)“氧化”时,试剂A可以是
(4)“除铁铝”时,应调节溶液pH的范围是
(5)“除钙”时,加入MnF2,发生反应的离子方程式是
(6)硫酸锰在不同温度下的溶解度S和一定温度内析出晶体的组成如图所示。“一系列操作”包括将所得滤液控制温度在80~90℃之间蒸发结晶、

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(1)合成塔中发生反应的化学方程式为_______ 。
(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨_______ 的性质。
(3)氧化炉中,NH3转化为NO的化学方程式为_______ 。标准状况下,5.6LNH3被氧化为NO时转移电子的物质的量为_______ 。
(4)吸收塔中出来的尾气可用Na2CO3溶液吸收,主要反应为:
a.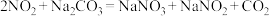
b.
①吸收后的溶液经浓缩、结晶、过滤,得到 晶体。该晶体中的主要杂质是
晶体。该晶体中的主要杂质是_______ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
②根据反应b,每产生22.4L(标准状况下) 吸收液质量将增加
吸收液质量将增加_______ g。
(5)以合成氨为基础的化肥工业对粮食增长的贡献率占50%左右,但人类如果过度施用化肥,对环境造成影响是_______ (任答1点);为了维持自然界中氮的平衡,除了合理施用化肥外,人类还可以采取措施是_______ (任答1点)。

(1)合成塔中发生反应的化学方程式为
(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨
(3)氧化炉中,NH3转化为NO的化学方程式为
(4)吸收塔中出来的尾气可用Na2CO3溶液吸收,主要反应为:
a.
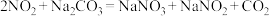
b.

①吸收后的溶液经浓缩、结晶、过滤,得到
 晶体。该晶体中的主要杂质是
晶体。该晶体中的主要杂质是②根据反应b,每产生22.4L(标准状况下)
 吸收液质量将增加
吸收液质量将增加(5)以合成氨为基础的化肥工业对粮食增长的贡献率占50%左右,但人类如果过度施用化肥,对环境造成影响是
您最近一年使用:0次



