甲烷重整时涉及以下两个反应:
①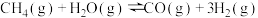

②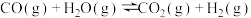

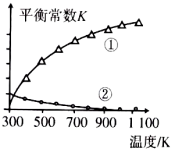
它们的平衡常数随温度的变化如图所示,下列说法正确的是
①
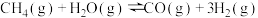

②

它们的平衡常数随温度的变化如图所示,下列说法正确的是

| A.反应①、②都是放热反应 |
| B.两曲线交点表示此时①、②两反应平衡常数相等 |
C.相同温度下,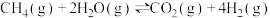 的平衡常数为 的平衡常数为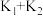 |
D.相同条件下,增大反应①中水蒸气的浓度, 的转化率增大 的转化率增大 |
更新时间:2021-10-20 13:33:43
|
相似题推荐
【推荐1】已知:氧化锂(Li2O)晶体形成过程中的能量变化如图所示,下列说法正确的是
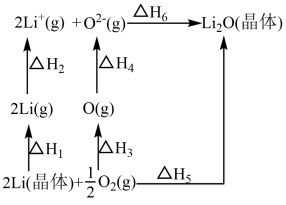

| A.∆H1<0,∆H2>0 |
| B.-∆H5+∆H1+∆H2+∆H3+∆H4+∆H6=0 |
| C.∆H3<0,∆H4<0 |
| D.氧化锂的晶格能=∆H6 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
【推荐2】S(单斜)和S(正交)是硫的两种同素异形体。已知:
①S(单斜,s)+O2(g)=SO2(g) △H1=-297.16 kJ·mol-1
②S(正交,s)+O2(g)=SO2(g) △H2=-296.83 kJ·mol-1
③S(单斜,s)=S(正交,s) △H3
下列说法正确的是
①S(单斜,s)+O2(g)=SO2(g) △H1=-297.16 kJ·mol-1
②S(正交,s)+O2(g)=SO2(g) △H2=-296.83 kJ·mol-1
③S(单斜,s)=S(正交,s) △H3
下列说法正确的是
| A.△H3=+0.33 kJ·mol-1 |
| B.单斜硫转化为正交硫的反应是放热反应 |
| C.正交硫比单斜硫稳定 |
| D.①式表示断裂1 mol O2中的共价键所吸收的能量比形成1 mol SO2中的共价键所放出的能量少297.16 kJ |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室模拟工业处理含铬废水,操作及现象如图1,反应过程中铬元素的化合价变化如图2下列说法不正确的是
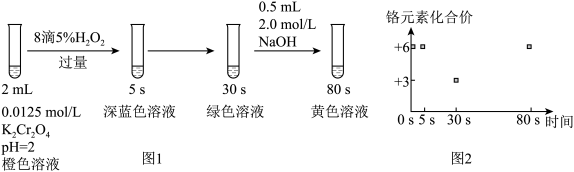
已知:深蓝色溶液中生成了CrO5。

已知:深蓝色溶液中生成了CrO5。
A.实验开始至5s, 发生了氧化还原反应 发生了氧化还原反应 |
B.实验开始至30s,溶液中生成Cr3+的总反应离子方程式为: +3H2O2+8H+=2Cr3++7H2O+3O2↑ +3H2O2+8H+=2Cr3++7H2O+3O2↑ |
| C.30s至80s的过程,不一定是氧气氧化了Cr3+ |
D.80s时,溶液中又生成了 ,颜色相比于开始时浅,是水稀释所致 ,颜色相比于开始时浅,是水稀释所致 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
【推荐2】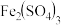 溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓盐酸黄色加深(b)。已知:
溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓盐酸黄色加深(b)。已知: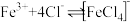 (黄色);浓度较小时
(黄色);浓度较小时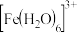 (用
(用 表示)几乎无色。取溶液进行如下实验,对现象的分析不正确的是
表示)几乎无色。取溶液进行如下实验,对现象的分析不正确的是
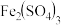 溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓盐酸黄色加深(b)。已知:
溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓盐酸黄色加深(b)。已知: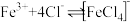 (黄色);浓度较小时
(黄色);浓度较小时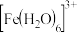 (用
(用 表示)几乎无色。取溶液进行如下实验,对现象的分析不正确的是
表示)几乎无色。取溶液进行如下实验,对现象的分析不正确的是A.测得溶液a的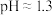 ,证明 ,证明 发生了水解 发生了水解 |
B.将溶液a加热,颜色加深,说明升温能促进 水解 水解 |
C.加入浓盐酸, 与 与 对 对 浓度大小的影响是一致的 浓度大小的影响是一致的 |
D.向b中加入 后,黄色褪去,说明 后,黄色褪去,说明 能抑制 能抑制 水解 水解 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐3】 “减少碳排放,实现碳中和”是当今世界的热门话题。某课题组利用CO2和H2在催化剂的作用下合成甲醇,主要发生如下三个反应:
I. CO2(g)+3H2(g)→CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
II.CO2(g)+H2(g)→CO(g)+H2O(g) ΔH2=+40.9kJ·mol-1
III.……
下列措施中,能提高CO2转化率的是___________。
I. CO2(g)+3H2(g)→CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
II.CO2(g)+H2(g)→CO(g)+H2O(g) ΔH2=+40.9kJ·mol-1
III.……
下列措施中,能提高CO2转化率的是___________。
| A.在原料气中加入适量H2O(g) |
| B.从体系中不断分离出甲醇 |
| C.循环利用原料气 |
| D.使用高效催化剂 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】已知反应N2O4(g)  2NO2(g) ΔH>0的平衡体系中,物质的总质量(m总)与总物质的量(n总)之比M(M=
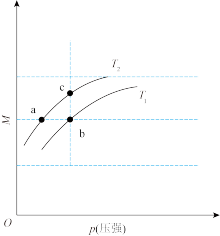
2NO2(g) ΔH>0的平衡体系中,物质的总质量(m总)与总物质的量(n总)之比M(M= 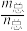 )在不同温度下随压强的变化曲线如图所示。下列说法正确的是
)在不同温度下随压强的变化曲线如图所示。下列说法正确的是
 2NO2(g) ΔH>0的平衡体系中,物质的总质量(m总)与总物质的量(n总)之比M(M=
2NO2(g) ΔH>0的平衡体系中,物质的总质量(m总)与总物质的量(n总)之比M(M= 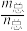 )在不同温度下随压强的变化曲线如图所示。下列说法正确的是
)在不同温度下随压强的变化曲线如图所示。下列说法正确的是
| A.温度:T1>T2 |
| B.平衡常数:K(a)=K(b)<K(c) |
| C.反应速率:vb<va |
| D.当M=69 g·mol-1时,n(NO2)∶n(N2O4)=1∶1 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
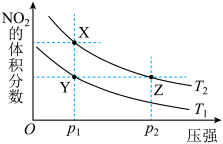
【推荐2】反应
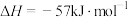 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是

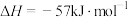 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是
A. | B.X、Y两点的反应速率:X>Y |
| C.X、Z两点气体的颜色:X比Z浅 | D.X、Z两点气体的平均相对分子质量:X>Z |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是( )
| A.平衡常数变化,化学平衡不一定发生移动 |
| B.化学平衡发生移动,平衡常数一定改变 |
| C.化学平衡常数只受温度的影响,温度升高,化学平衡常数的变化取决于该反应的反应热 |
| D.对于一个可逆反应,化学计量数不同,化学平衡常数表达式及数值也不同 |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐2】已知:2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g) ∆H,原料初始组成n(CO2):n(H2)=1:3,反应达到平衡时,体系压强为p,四种组分的物质的量分数x随温度T的变化如图。对于气相反应,用某组分(B)的分压(pB)代替物质的量浓度(cB)表示平衡常数KP,分压=总压×物质的量分数。下列说法不正确的是
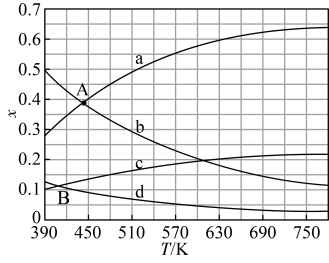

| A.反应的∆H>0 |
| B.曲线c代表的是C2H4 |
| C.为了提高反应速率,可以选择合适的催化剂 |
D.根据A点(440K,0.39)求得该温度时反应的平衡常数Kp=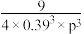 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
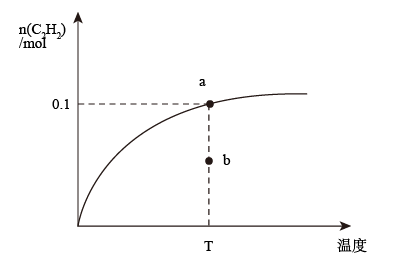
【推荐3】温度为T时,向2.00L恒容密闭容器中充入1.00molCH4,发生反应:2CH4(g) C2H2(g)+3H2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
C2H2(g)+3H2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
改变温度,测得不同温度下达平衡时C2H2的物质的量的变化曲线如图。下列说法正确的是
 C2H2(g)+3H2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
C2H2(g)+3H2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:| t/s | 0 | 5 | 15 | 25 | 35 |
| n(CH4)/mol | 1.00 | 0.84 | 0.81 | 0.80 | 0.80 |

| A.温度T时,前5sH2平均速率为0.048mol/(L·s) |
| B.温度T时,b点v(正)>v(逆) |
| C.该反应的平衡常数随温度升高逐渐减小 |
| D.温度T时,若向2.00L恒容密闭充入2.00molC2H2和6.00molH2,达到平衡时,C2H2转化率大于80% |
您最近一年使用:0次

 、
、 的氧化性依次减弱
的氧化性依次减弱 CH3CH2OH(g)+3H2O(g)需在300℃进行可推测该反应是吸热反应
CH3CH2OH(g)+3H2O(g)需在300℃进行可推测该反应是吸热反应

