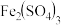 溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓盐酸黄色加深(b)。已知:
溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓盐酸黄色加深(b)。已知: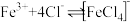 (黄色);浓度较小时
(黄色);浓度较小时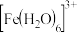 (用
(用 表示)几乎无色。取溶液进行如下实验,对现象的分析不正确的是
表示)几乎无色。取溶液进行如下实验,对现象的分析不正确的是A.测得溶液a的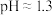 ,证明 ,证明 发生了水解 发生了水解 |
B.将溶液a加热,颜色加深,说明升温能促进 水解 水解 |
C.加入浓盐酸, 与 与 对 对 浓度大小的影响是一致的 浓度大小的影响是一致的 |
D.向b中加入 后,黄色褪去,说明 后,黄色褪去,说明 能抑制 能抑制 水解 水解 |
更新时间:2022-07-11 21:45:04
|
相似题推荐
多选题
|
较易
(0.85)
【推荐1】萨巴蒂尔反应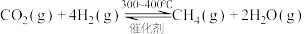 ,与水的电解联合使用是一种重要的载人航天器中氧气再生的方法。下列说法不正确的是
,与水的电解联合使用是一种重要的载人航天器中氧气再生的方法。下列说法不正确的是
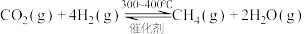 ,与水的电解联合使用是一种重要的载人航天器中氧气再生的方法。下列说法不正确的是
,与水的电解联合使用是一种重要的载人航天器中氧气再生的方法。下列说法不正确的是A.上述反应 >0 >0 |
B.增大 , , 的平衡转化率升高 的平衡转化率升高 |
C.上述反应平衡常数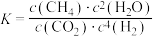 |
D.萨巴蒂尔反应产生的 可作航天器燃料 可作航天器燃料 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
【推荐2】各可逆反应达平衡后,改变反应条件,其变化趋势正确的是
A.I2(g)+H2(g)  2HI(g)(恒温) 2HI(g)(恒温) 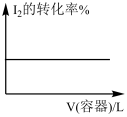 |
B.CH3COOH H++CH3COO- H++CH3COO-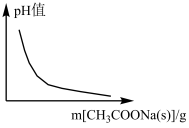 |
C.FeCl3+3KSCN Fe(SCN)3+3KCl Fe(SCN)3+3KCl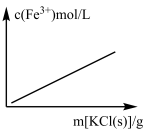 |
D.CH3OCH3(g)+3H2O(g)  6H2(g)+2CO(g)-Q 6H2(g)+2CO(g)-Q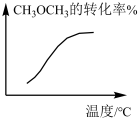 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】下列事实能说明氨水是弱电解质的是:
| A.氨水与氯化铝溶液反应产生氢氧化铝沉淀 |
| B.用氨水做导电实验,灯泡很暗 |
| C.0.1mol/L的氨水的pH<13 |
| D.氯化铵溶液的pH<7 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐2】已知反应BeCl2+Na2BeO2+2H2O →2NaCl+2Be(OH)2↓ 能进行完全。以下推断中正确的是
| A.BeCl2溶液pH<7,将其蒸干、灼烧后可得残留物BeCl2 |
| B.Na2BeO2溶液pH>7,将其蒸干、灼烧后可得残留物Na2BeO2 |
| C.Be(OH)2即能溶于盐酸,又能溶于NaOH溶液 |
| D.BeCl2水溶液的导电性强,BeCl2一定是离子化合物 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
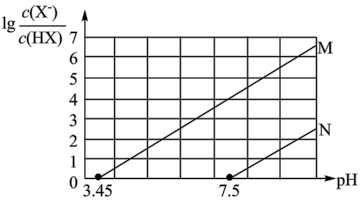
【推荐1】常温下,向 的NaA溶液中通入HF(g),溶液中
的NaA溶液中通入HF(g),溶液中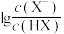 (X代表A或F)的值和pH的关系如图所示,已知酸性:
(X代表A或F)的值和pH的关系如图所示,已知酸性: ,忽略溶液体积的变化,下列叙述错误的是
,忽略溶液体积的变化,下列叙述错误的是
 的NaA溶液中通入HF(g),溶液中
的NaA溶液中通入HF(g),溶液中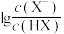 (X代表A或F)的值和pH的关系如图所示,已知酸性:
(X代表A或F)的值和pH的关系如图所示,已知酸性: ,忽略溶液体积的变化,下列叙述错误的是
,忽略溶液体积的变化,下列叙述错误的是
A.HA的电离常数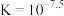 |
B.当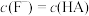 时,混合溶液 时,混合溶液 |
C.通入0.01molHF时,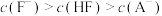 |
| D.随着HF的通入,溶液导电性先增大后减小 |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐2】常温下,将等浓度的NaOH溶液分别滴加到等pH、等体积的HA、HB两种弱酸溶液中,溶液的pH与粒子浓度比值的对数关系如图所示。下列叙述错误的是
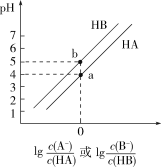

| A.酸性:HA<HB |
| B.a点时,溶液中由水电离出的c(OH-)约为1×10−10 mol∙L−1 |
| C.向HB溶液中滴加NaOH溶液至pH=7时:c(B-)>c(HB) |
| D.b点时,c(Na+)>c(B-)=c(HB)>c(H+)>c(OH-) |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】在一定条件下,Na2CO3溶液存在水解平衡:CO +H2O
+H2O HCO
HCO +OH-。下列说法正确的是( )
+OH-。下列说法正确的是( )
 +H2O
+H2O HCO
HCO +OH-。下列说法正确的是( )
+OH-。下列说法正确的是( )| A.稀释溶液,各物质浓度均减小,平衡不移动 |
| B.通入CO2,平衡向正反应方向移动 |
C.升高温度,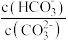 减小 减小 |
| D.加入NaOH固体,溶液pH增大 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】在Al3++3H2O Al(OH)3+3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH增大,应采取的措施是
Al(OH)3+3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH增大,应采取的措施是
 Al(OH)3+3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH增大,应采取的措施是
Al(OH)3+3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH增大,应采取的措施是| A.加热 | B.通入HCl |
| C.加入适量Na2CO3(s) | D.加入NaCl溶液 |
您最近一年使用:0次



 溶液中存在
溶液中存在 平衡。下列说法不正确的是
平衡。下列说法不正确的是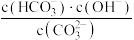 增大
增大 ,溶液
,溶液 减小
减小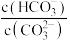 增大
增大


