室温时,向40 mL 0.05 mol· L-1NaHX溶液中逐滴滴入0.1 mol· L-1NaOH溶液,pH水为由水电离产生的氢离子浓度的负对数。pH水与所加NaOH溶液的体积关系如下图所示。下列说法错误的是
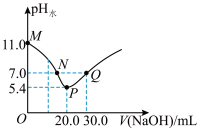

| A.M点溶液中,c(Na+ )>c(HX- )>c(H+ )>c(X2-) |
| B.N点和Q点溶液由水电离产生的氢离子浓度相同,溶液都呈中性 |
C.图中N点至P点对应的溶液中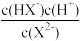 始终减小 始终减小 |
| D.P点对应的溶液pH水<7,呈碱性 |
19-20高三·河北衡水·阶段练习 查看更多[3]
河北省衡水市河北衡水中学2021届高三第一次联合考试(全国卷2)化学试题湖北省仙桃中学、天门中学(B班)2021-2022学年高二上学期期中考试化学试题(已下线)专题25 水的电离和溶液的酸碱性(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练
更新时间:2021-10-30 17:10:29
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.直接加热蒸干FeCl3溶液,可得FeCl3固体 |
| B.加入催化剂可加快反应速率,并提高反应物的转化率 |
| C.pH值相同的CH3COOH溶液和NH4Cl溶液中,水的电离程度相同 |
| D.可用Na2CO3溶液处理水垢中的CaSO4,转化为易于除去的CaCO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
A.c(H+)=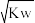 的溶液一定呈中性 的溶液一定呈中性 |
| B.将水加热,Kw增大,pH不变,仍呈中性 |
| C.向水中加入少量氢氧化钠固体,溶液的c(OH-)增大,平衡逆向移动,Kw减小 |
| D.向0.01 mol·L-1醋酸溶液中加水,溶液中水电离产生的c(H+)将减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知水的电离方程式:H2O H++OH-,下列叙述中正确的是
H++OH-,下列叙述中正确的是
 H++OH-,下列叙述中正确的是
H++OH-,下列叙述中正确的是| A.升高温度,KW增大,pH不变 |
| B.向水中滴入氨水,水电离平衡逆向移动,c(OH-)降低 |
| C.室温下向水中加入少量稀硫酸,c(H+)增大,KW不变 |
| D.向水中加入少量固体CH3COONa,水电离平衡逆向移动,c(H+)降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】298 K时,在20.0 mL0.10 mol·L-1氨水中滴入0.10 mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol·L-1氨水的电离度为1%,下列有关叙述正确的是
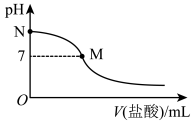

| A.该滴定过程应该选择酚酞作为指示剂 |
| B.M点对应的盐酸体积小于20.0 mL |
C.M点处的溶液中c( )=c(Cl-)=c(H+)=c(OH-) )=c(Cl-)=c(H+)=c(OH-) |
| D.N点处的溶液中pH=12 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关溶液的说法正确的是
| A.向10mLpH=3的醋酸溶液中加入10mLpH=l1的NaOH溶液,混合液的pH=7 |
| B.实验测定NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3COOH>H2CO3 |
| C.NH4Cl溶液加水稀释过程中c(H+)+c(NH3·H2O)=c(OH一) |
| D.向AgI沉淀中加入饱和KCl溶液,有白色沉淀生成,说明AgCl比AgI更难溶 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】酸碱中和滴定常用于测定酸或碱的浓度。实验小组用0.1000 mol∙L-1的NaOH溶液滴定20.00 mL 0.1000 mol∙L-1的CH3COOH溶液。下列滴定过程中存在关系式或说法不正确 的是
| A.滴定开始后溶液中始终存在:c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| B.V(NaOH)=10.00 mL时溶液中存在:c(Na+)=c(CH3COO-) |
| C.V(NaOH)=20.00 mL时溶液中存在:c(CH3COOH)+c(H+)=c(OH-) |
D. 随V(NaOH)的增大而增大 随V(NaOH)的增大而增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】次氯酸钠是消灭新型冠状病毒常用的消毒液,常温下 ,向10mL 0. 1 mol • L-1 HClO溶液中滴入0.1mol •L-1NaOH溶液,溶液中由水电离出的氢离子浓度的负对数[-lg c水( H+)]与所加NaOH 溶液体积的关系如图所示。下列说法正确的是
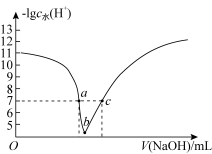

| A.0.1mol •L-1NaClO 溶液中 ClO-的个数小于 NA |
| B.c 点溶液对应的 pH = 7 |
| C.a 点溶液中存在:c( Na+ ) =c( ClO-) +c(HClO ) |
| D.b 点溶液中存在:c( Na+ )>c( ClO-)>c(OH-)>c( H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各溶液中,微粒的物质的量浓度关系错误的是
A. 溶液: 溶液: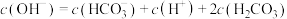 |
B.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液: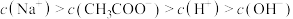 |
C.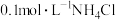 溶液: 溶液: |
D.向硝酸钠溶液中滴加稀盐酸得到的 的混合溶液: 的混合溶液: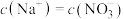 |
您最近一年使用:0次
单选题
|
适中
(0.65)
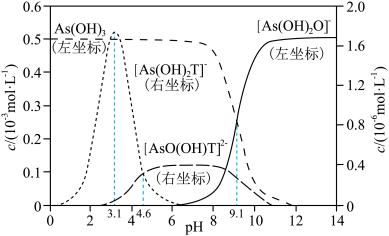
【推荐3】下图是亚砷酸As(OH)3和酒石酸(H2T, ,
, )混合体系中部分物种的c-pH图(浓度:总As为
)混合体系中部分物种的c-pH图(浓度:总As为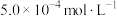 ,总T为
,总T为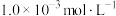 )。下列说法错误的是
)。下列说法错误的是
 ,
, )混合体系中部分物种的c-pH图(浓度:总As为
)混合体系中部分物种的c-pH图(浓度:总As为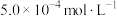 ,总T为
,总T为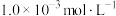 )。下列说法错误的是
)。下列说法错误的是
A.pH=7.0时,溶液中浓度最高的物种为 |
B.pH=3.1时, 的浓度比 的浓度比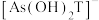 的高 的高 |
C.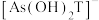 的酸性比 的酸性比 的强 的强 |
D. 的 的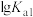 为-9.1 为-9.1 |
您最近一年使用:0次



