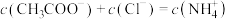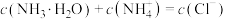常温下,将NaOH溶液滴加到等物质的量浓度的HX、HY两种酸溶液中,混合溶液的pH与离子浓度的关系如图所示。下列说法错误的是

| A.HX的酸性比HY强 |
| B.Ka(HY)的数量级为10-4 |
| C.b点溶液中c(Y-)一定大于a点溶液中c(X-) |
| D.a、b两点溶液中c(Na+)的差值为c(X-)-c(Y-) |
2021·四川绵阳·一模 查看更多[3]
四川省绵阳市2021-2022学年高三上学期第一次考试理综化学试题(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)安徽省淮北市树人高级中学2023-2024学年高二下学期开学考试化学试题
更新时间:2021-11-03 00:43:43
|
相似题推荐
单选题
|
较难
(0.4)
真题
名校
【推荐1】常温下,用浓度为0.100 mol·L-1的NaOH溶液分别逐滴加入到20.00 mL 0.100 0 mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确的是( )
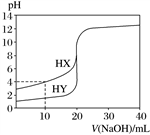

| A.V(NaOH)=10.00 mL时,两份溶液中c(X-)>c(Y-) |
| B.V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) |
| C.V(NaOH)=20.00 mL时,c(OH-)>c(H+)>c(Na+)>c(X-) |
| D.pH=7时,两份溶液中c(X-)=c(Na+)=c(Y-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】缓冲溶液指的是由弱酸及其盐、弱碱及其盐组成的混合溶液,能在一定程度上抵消、减轻外加强酸或强碱对溶液酸碱度的影响,从而保持溶液的pH值相对稳定。缓冲溶液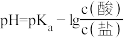 ,当酸和盐浓度相等时缓冲能力最强。丙酸(
,当酸和盐浓度相等时缓冲能力最强。丙酸(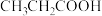 ,简写成HR)的酸性比亚硝酸(
,简写成HR)的酸性比亚硝酸( )弱。298K时,用pH为13的NaOH溶液滴定16.00ml
)弱。298K时,用pH为13的NaOH溶液滴定16.00ml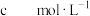 HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知:
HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知: ,
,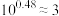 。下列叙述错误的是
。下列叙述错误的是
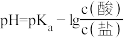 ,当酸和盐浓度相等时缓冲能力最强。丙酸(
,当酸和盐浓度相等时缓冲能力最强。丙酸(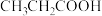 ,简写成HR)的酸性比亚硝酸(
,简写成HR)的酸性比亚硝酸( )弱。298K时,用pH为13的NaOH溶液滴定16.00ml
)弱。298K时,用pH为13的NaOH溶液滴定16.00ml HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知:
HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知: ,
,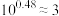 。下列叙述错误的是
。下列叙述错误的是
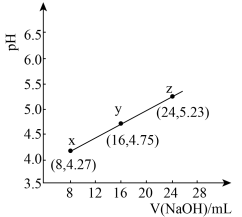
| A.当溶液pH为4.75时,缓冲能力最强 |
B.上述丙酸溶液浓度为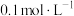 |
C.y点溶液中: |
D.其他相同, 替代HR,曲线位于图中曲线下方 替代HR,曲线位于图中曲线下方 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某温度下,改变0.10mol•L-1K2X2O7溶液的pH时,各种含X元素粒子及OH-浓度变化如图所示。下列有关说法正确的是


A. |
| B.KW=1×10-13 |
C.E点溶液中存在:c(K+)>5c(X2O ) ) |
D.反应 的平衡常数K=1×10-13.2 的平衡常数K=1×10-13.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
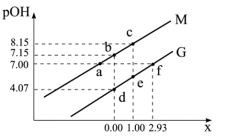
【推荐2】乙二胺( )是二元弱碱,在水中的电离原理类似于氨。
)是二元弱碱,在水中的电离原理类似于氨。
电离方程式为:第一级电离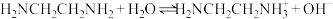
第二级电离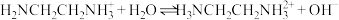
已知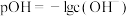 。常温下,向乙二胺溶液中滴加某浓度硫酸溶液,调节
。常温下,向乙二胺溶液中滴加某浓度硫酸溶液,调节 的值,测得溶液的
的值,测得溶液的 随离子浓度变化关系如图所示。下列说法错误的是
随离子浓度变化关系如图所示。下列说法错误的是
 )是二元弱碱,在水中的电离原理类似于氨。
)是二元弱碱,在水中的电离原理类似于氨。电离方程式为:第一级电离
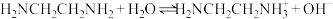
第二级电离
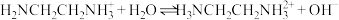
已知
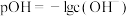 。常温下,向乙二胺溶液中滴加某浓度硫酸溶液,调节
。常温下,向乙二胺溶液中滴加某浓度硫酸溶液,调节 的值,测得溶液的
的值,测得溶液的 随离子浓度变化关系如图所示。下列说法错误的是
随离子浓度变化关系如图所示。下列说法错误的是
| A.溶液中水的电离程度:b点大于a点 |
B.曲线G代表 与 与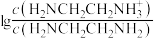 的变化关系 的变化关系 |
C.常温下, 的 的 的数量级为 的数量级为 |
D.等浓度等体积的 溶液与 溶液与 溶液混合,所得溶液是呈中性 溶液混合,所得溶液是呈中性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
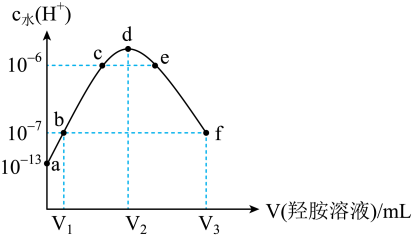
【推荐3】常温下,向20 mL的某稀盐酸中滴入0.1 mol·L-1的羟胺溶液, 羟胺的电离方程式为:NH2OH+H2O  NH3OH++OH-(25℃常温时, Kb=9.0×l0-9)。溶液中由水电离出的氢离子浓度随滴入羟胺溶液体积的变化如图(已知:lg3=0.5),下列分析正确的是
NH3OH++OH-(25℃常温时, Kb=9.0×l0-9)。溶液中由水电离出的氢离子浓度随滴入羟胺溶液体积的变化如图(已知:lg3=0.5),下列分析正确的是
 NH3OH++OH-(25℃常温时, Kb=9.0×l0-9)。溶液中由水电离出的氢离子浓度随滴入羟胺溶液体积的变化如图(已知:lg3=0.5),下列分析正确的是
NH3OH++OH-(25℃常温时, Kb=9.0×l0-9)。溶液中由水电离出的氢离子浓度随滴入羟胺溶液体积的变化如图(已知:lg3=0.5),下列分析正确的是
| A.0.1 mol·L-1羟胺溶液的 pH=8.5 | B.b点溶液中:c(H+) =c(OH-) |
| C.d点对应溶液中存在:c(H+)=c (OH-)+c (NH2OH) | D.该稀盐酸的浓度为0.2 mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】已知 溶液呈酸性,
溶液呈酸性, 溶液呈碱性。对于浓度均为
溶液呈碱性。对于浓度均为 的
的 溶液和
溶液和 溶液,溶液中各微粒的物质的量浓度关系正确的是(R表示S或C)
溶液,溶液中各微粒的物质的量浓度关系正确的是(R表示S或C)
 溶液呈酸性,
溶液呈酸性, 溶液呈碱性。对于浓度均为
溶液呈碱性。对于浓度均为 的
的 溶液和
溶液和 溶液,溶液中各微粒的物质的量浓度关系正确的是(R表示S或C)
溶液,溶液中各微粒的物质的量浓度关系正确的是(R表示S或C)A.两溶液中均有 |
B.两溶液中均有c(Na+)+c(H+)═c(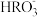 )+c( )+c(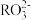 )+c(OH−) )+c(OH−) |
C.两溶液中均有c(H+)+c(H2RO3)=c(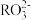 )+c(OH-) )+c(OH-) |
D.两溶液中c(Na+)、c(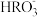 )、 )、 分别对应相等 分别对应相等 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,用0.5mol/LNaHCO3溶液滴定25.00mL0.25mol/LCaCl2溶液,测得混合溶液的pH随滴加NaHCO3溶液体积的变化如图所示,当滴加25.00mL NaHCO3溶液时出现较为明显的白色沉淀[已知:常温下,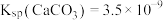 、
、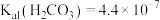 、
、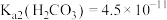 、
、 ]。
]。

下列说法错误的是
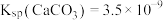 、
、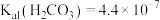 、
、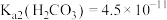 、
、 ]。
]。
下列说法错误的是
A.常温下,向饱和NaHCO3溶液中加入少量NaHCO3固体,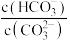 不变 不变 |
B.从 点到 点到 点, 点, 的电离平衡正向移动 的电离平衡正向移动 |
C. 点溶液中 点溶液中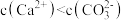 |
D. 点溶液中 点溶液中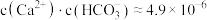 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】25℃,用浓度为 的NaOH溶液滴定20.00mL浓度为
的NaOH溶液滴定20.00mL浓度为 的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法不正确的是
的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法不正确的是
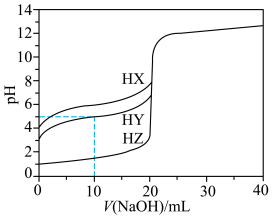
 的NaOH溶液滴定20.00mL浓度为
的NaOH溶液滴定20.00mL浓度为 的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法不正确的是
的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法不正确的是
| A.在相同温度下,同浓度的三种酸溶液的导电能力:HZ>HY>HX |
B.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,溶液中存在: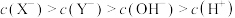 |
| C.滴定至终点时,消耗的NaOH溶液体积相同 |
D.根据滴定曲线,可知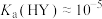 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,向二元弱碱联氨(N2H4)的水溶液中滴加盐酸,所得混合溶液中 和
和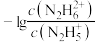 与pOH的变化关系如图所示。
与pOH的变化关系如图所示。
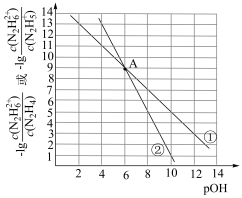
已知:①联氨在水中的电离方式类似NH3;② 。下列说法错误的是
。下列说法错误的是
 和
和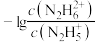 与pOH的变化关系如图所示。
与pOH的变化关系如图所示。
已知:①联氨在水中的电离方式类似NH3;②
 。下列说法错误的是
。下列说法错误的是A.曲线①表示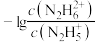 与pOH的关系 与pOH的关系 |
B.A点溶液中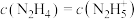 |
C.常温下,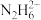 的二级水解常数 的二级水解常数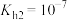 |
| D.常温下,N2H5Cl溶液的pH<7 |
您最近一年使用:0次

 盐酸和醋酸(
盐酸和醋酸(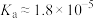 )的混合溶液中滴加0.1 mol⋅L
)的混合溶液中滴加0.1 mol⋅L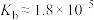 ),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是
),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是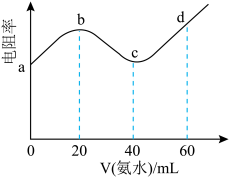
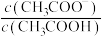 逐渐增大
逐渐增大