25℃,水的电离达到平衡:H2O⇌H++OH-  >0,下列叙述正确的是
>0,下列叙述正确的是
 >0,下列叙述正确的是
>0,下列叙述正确的是| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,pH变大 |
| C.向水中加入少量固体Na2S,平衡逆向移动,c(OH-)降低 |
| D.将水加热,c(H+)增大,c(OH-)增大,Kw增大 |
更新时间:2021-11-13 09:25:05
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】广西的地质组成决定了它多溶洞的特点,广西德保吉星岩贯穿五座大山,洞内水陆兼备,上下共有四层。洞内有大量绚丽多姿、玲珑剔透的石笋、钟乳石、石柱、石幔、石花等。研究发现,钟乳石质量受温度、人类活动影响;测得钟乳石质量与温度、游客日流量关系如图所示。下列叙述正确的是

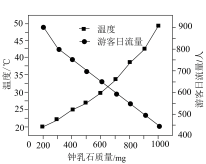


| A.夏天碳酸钙溶解度增大,钟乳石质量减少 |
| B.钟乳石形成过程中只涉及离子化合物的转化 |
| C.游客日流量增大,CO2浓度增大导致钟乳石溶解 |
| D.“滴水穿石”过程,体现了温度对钟乳石的影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验中,对现象的解释不正确 的是
| 选项 | A | B |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 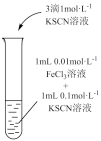 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 |
| 选项 | C | D |
| 装置及操作 |  分别测定20℃和80℃蒸馏水的电导率 |  |
| 现象 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在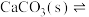  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在3个容积均为2.0L的恒容密闭容器中,反应H2O(g) + C(s)  CO(g) +H2(g) ΔH>0 ,分别在一定温度下达到平衡,下列说法正确的是
CO(g) +H2(g) ΔH>0 ,分别在一定温度下达到平衡,下列说法正确的是
 CO(g) +H2(g) ΔH>0 ,分别在一定温度下达到平衡,下列说法正确的是
CO(g) +H2(g) ΔH>0 ,分别在一定温度下达到平衡,下列说法正确的是容器 | 温度 (T1>T2) | 起始时物质的量/mol | 平衡时物质的量/mol | |||
| n(H2O) | n(C) | n(CO) | n(H2) | n(CO) | ||
| I | T1 | 0.6 | 1.2 | 0 | 0 | 0.2 |
| II | T1 | 1.2 | 1.2 | 0 | 0 | x |
| III | T2 | 0 | 0 | 0.6 | 0.6 | y |
| A.当温度为T1时,该反应的化学平衡常数值为0.1 |
| B.达到平衡时,容器II中H2O的转化率比容器I中的小 |
| C.若5min后容器I中达到平衡,则H2O的平衡浓度为1.0 mol/L |
| D.达到平衡时,容器III中 CO的转化率小于66.6% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.由水电离的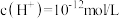 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.无色溶液中: 、 、 、 、 、 、 |
C.含有 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各组离子能在指定溶液中,可能大量共存的是
①无色溶液中:K+、Na+、CO 、SO
、SO
②pH=11的溶液中:Na+、Ba2+、AlO 、ClO-
、ClO-
③水电离出的c(H+) =10-12mol·L-1的溶液中:Mg2+、NH 、HCO
、HCO 、S2-
、S2-
④加入Al放出H2的溶液中:Cu2+、NH 、Cl-、NO
、Cl-、NO
⑤无色溶液中:K+、Na+、 、
、
⑥酸性溶液中:Fe2+、Al3+、NO 、Cl-
、Cl-
①无色溶液中:K+、Na+、CO
 、SO
、SO
②pH=11的溶液中:Na+、Ba2+、AlO
 、ClO-
、ClO-③水电离出的c(H+) =10-12mol·L-1的溶液中:Mg2+、NH
 、HCO
、HCO 、S2-
、S2-④加入Al放出H2的溶液中:Cu2+、NH
 、Cl-、NO
、Cl-、NO
⑤无色溶液中:K+、Na+、
 、
、
⑥酸性溶液中:Fe2+、Al3+、NO
 、Cl-
、Cl-| A.①②④ | B.①②④⑥ | C.①② | D.①②⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25°C时,向20 mL 0.10 mol·L-1一元酸HA中逐滴加入0.10 mol·L-1 NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
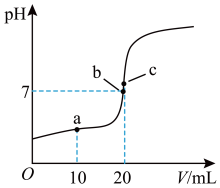

| A.HA是强酸 |
| B.a点,c(Na+) = c(A-) + c(HA) |
| C.b点为滴定终点,c(Na+) > c(A-) |
| D.c点,水的电离程度最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在某温度时将  氨水滴入
氨水滴入  盐酸中,溶液 pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
盐酸中,溶液 pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
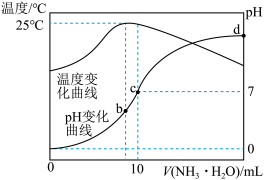
 氨水滴入
氨水滴入  盐酸中,溶液 pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
盐酸中,溶液 pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是 
A.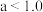 |
B.水的电离程度: |
C.c点: |
D.d点: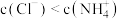 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】H2A为二元弱酸。室温下,下列指定溶液中微粒物质的量浓度关系正确的是(忽略溶液混合引起的体积变化)
| A.0.1mol/LH2A溶液:c(H2A)>c(HA-)>c(A2-)>c(H+) |
| B.0.1mol/LNaHA溶液(pH<7):c(Na+)>c(HA-);c(H2A)>c(A2-) |
| C.0.1mol/LNaHA溶液和0.1mol/LNaOH溶液等体积混合:c(OH-)=c(H+)+c(HA-)+2c(H2A) |
| D.0.1mol/LNaHA溶液(pH<7)和0.1mol/LH2A溶液等体积混合:c(Na+)>c(HA-)+2c(A2-) |
您最近一年使用:0次

 )
)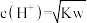 的溶液一定是中性
的溶液一定是中性 大的酸溶液中
大的酸溶液中 一定比
一定比 大
大 的盐酸和
的盐酸和 的硫酸等体积混合(混合后体积变化不计),所得溶液
的硫酸等体积混合(混合后体积变化不计),所得溶液
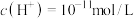 时,此溶液的
时,此溶液的 或者3
或者3

