根据下列实验及现象,能量关系正确的是
| 实验及现象 | 能量关系 | |
| A | 将“NO2球”置于热水中,红棕色加深 | N2O4(g) 2NO2(g) △H<0 2NO2(g) △H<0 |
| B | NaOH与HCl溶液混合,溶液温度升高 |  |
| C | 钠投入水中,熔化成小球 | 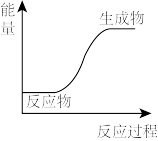 |
| D | 微热含酚酞的Na2CO3溶液,红色加深 | CO (aq)+H2O(1) (aq)+H2O(1)  HCO HCO (aq)+OH-(aq) △H<0 (aq)+OH-(aq) △H<0 |
| A.A | B.B | C.C | D.D |
更新时间:2022-01-02 21:16:51
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】钠与水的反应现象与产生现象原因解释合理的是
| A.钠浮在水面上——熔点低 | B.水蒸气——生成气体 |
| C.咝咝发出响声——反应剧烈 | D.游动——密度小于水 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】将块金属钠投入盛有 溶液的试管中,不可能观察到的现象是
溶液的试管中,不可能观察到的现象是
 溶液的试管中,不可能观察到的现象是
溶液的试管中,不可能观察到的现象是| A.钠在液面上四处游动 | B.溶液中有红色金属析出 |
| C.有气泡冒出 | D.生成蓝色沉淀 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】关于硫酸工业中的催化氧化反应,可以用勒夏特列原理解释的是
| A.升温至450℃左右 | B.选择V2O5做催化剂 |
| C.选择常压条件 | D.通入过量氧气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在硫酸工业生产中,通过下列反应使SO2氧化成SO3: 2SO2(g) +O2(g)  2SO3(g) ΔH= -196.6kJ/mol。下 表列出了在不同温度和压强下,反应达到平衡时SO2的转化率
2SO3(g) ΔH= -196.6kJ/mol。下 表列出了在不同温度和压强下,反应达到平衡时SO2的转化率
从化学反应速率、化学平衡及生产成本、产量等角度综合分析,在实际生产中有关该反应适宜条件选择的说法正确的是
 2SO3(g) ΔH= -196.6kJ/mol。下 表列出了在不同温度和压强下,反应达到平衡时SO2的转化率
2SO3(g) ΔH= -196.6kJ/mol。下 表列出了在不同温度和压强下,反应达到平衡时SO2的转化率| 温度/℃ | 平衡时的转化率 | ||||
| 0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
| A.SO2的转化率与温度成反比,故采用尽可能低的温度 |
| B.该反应在450℃左右、1MPa (常压)下进行较为合适 |
| C.SO2的转化率与压强成正比,故采用尽可能高的压强 |
| D.为了提高的SO2的转化率,应使用合适的催化剂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】有①NaOH溶液 ② 溶液 ③
溶液 ③ 溶液各25mL,物质的量浓度均为
溶液各25mL,物质的量浓度均为 ,下列说法正确的是
,下列说法正确的是
 溶液 ③
溶液 ③ 溶液各25mL,物质的量浓度均为
溶液各25mL,物质的量浓度均为 ,下列说法正确的是
,下列说法正确的是| A.3种溶液pH的大小顺序是①>②>③ |
B.若分别加入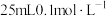 盐酸后,pH最大的是③ 盐酸后,pH最大的是③ |
| C.若将3种溶液稀释相同倍数,pH变化最大的是② |
| D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是①>③>② |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】化学与人类生产、生活密切相关。下列描述中不涉及盐类水解原理的是
| A.明矾净水 | B.氯化铵溶液除铁锈 |
| C.用食盐腌制肉制品 | D.用草木灰去除油污 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.26g苯乙烯( )含有 )含有 的数目为 的数目为 |
B. 的 的 溶液中,含有 溶液中,含有 的数目等于 的数目等于 |
C.3.2gCu在足量 或硫蒸气中完全反应失去的电子数均为0.1 或硫蒸气中完全反应失去的电子数均为0.1 |
D.2.0g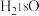 与 与 的混合物中所含中子数为 的混合物中所含中子数为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.水解反应是吸热反应 | B.升高温度可以抑制盐类的水解 |
| C.正盐水溶液的pH均为7 | D.酸式盐的pH均小于7 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】关于FeCl3溶液水解的说法错误的是( )
| A.水解达到平衡时加水稀释,平衡向正反应方向移动 |
| B.浓度为5 mol/L和0.5 mol/L的两种FeCl3 溶液,其他条件相同时,Fe3+水解程度前者比后者大 |
| C.有50℃和20℃的同浓度的FeCl3溶液,其他条件相同时,Fe3+的水解程度前者比后者大 |
| D.为抑制Fe3+水解,较好地保存FeCl3溶液应加入少量HCl |
您最近一年使用:0次

 的NaHCO3溶液中滴加2滴甲基橙
的NaHCO3溶液中滴加2滴甲基橙

