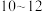可用作合金添加剂、有机化工的催化剂。钒钛磁铁矿炼钢后剩余的尾渣中含有
可用作合金添加剂、有机化工的催化剂。钒钛磁铁矿炼钢后剩余的尾渣中含有 、
、 、
、 、
、 、
、 等,利用该钒渣制备
等,利用该钒渣制备 的工艺流程如下:
的工艺流程如下: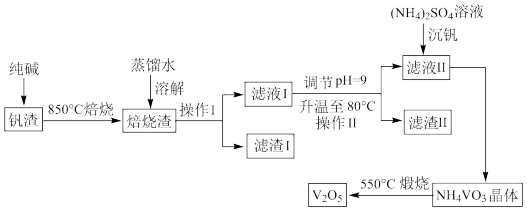
已知:①焙烧后
 、
、 、
、 分别生成
分别生成 、
、 、
、 。
。②
 价钒在溶液中的主要存在形式与溶液
价钒在溶液中的主要存在形式与溶液 的关系如下表:
的关系如下表:
|
|
|
|
|
主要离子 |
|
|
|
|
(1)写出焙烧时
 发生反应的化学方程式:
发生反应的化学方程式:(2)“滤渣Ⅰ”的成分是
(3)用离子方程式表示
 溶液显碱性的原因:
溶液显碱性的原因: 的
的 溶液中各离子浓度由大到小的顺序为
溶液中各离子浓度由大到小的顺序为(4)“沉钒”操作中,需控制溶液的
 为
为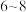 ,原因为
,原因为(5)煅烧生成的气体产物可以用
更新时间:2022-01-23 18:25:38
|
相似题推荐
【推荐1】 是一种很好的压电和介电材料,一种以铌铁矿(主要成分为:
是一种很好的压电和介电材料,一种以铌铁矿(主要成分为: 、
、 、
、 和少量的FeO、CaO、MgO)为原料的制取工艺流程如下:
和少量的FeO、CaO、MgO)为原料的制取工艺流程如下:
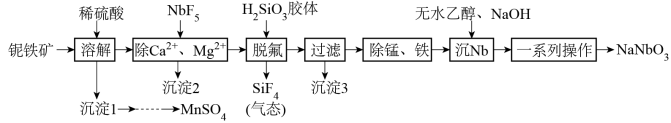
(1)为了加速“溶解”,可采取的措施有______ (除粉碎、搅拌外,写1种);溶解过程中 与FeO反应的化学方程式:
与FeO反应的化学方程式:______ ;沉淀1的主要成分是 和
和______ (填化学式)。
(2)“除 、
、 ”,当溶液中
”,当溶液中 时,溶液中
时,溶液中 的最大值为
的最大值为______  。[已知:
。[已知: ,
, ]
]
(3)“一系列操作”包括过滤和______ 。
(4)钛酸钡 也是一种强介电化合物。工业上,以
也是一种强介电化合物。工业上,以 、
、 为原料,采用草酸盐共沉淀法制备草酸氧钛钡晶体
为原料,采用草酸盐共沉淀法制备草酸氧钛钡晶体 ,再高温煅烧制得
,再高温煅烧制得 粉末。
粉末。
① 水解所得
水解所得 经焙烧得到
经焙烧得到 ,写出
,写出 水解的化学方程式
水解的化学方程式______ 。
②草酸与草酸盐在实验和工业生产中都起着重要的作用。常温, 溶液呈
溶液呈______ 性(填:“酸”、“碱”或“中”),原因是______ 。[已知 ,
, ]
]
 是一种很好的压电和介电材料,一种以铌铁矿(主要成分为:
是一种很好的压电和介电材料,一种以铌铁矿(主要成分为: 、
、 、
、 和少量的FeO、CaO、MgO)为原料的制取工艺流程如下:
和少量的FeO、CaO、MgO)为原料的制取工艺流程如下:
(1)为了加速“溶解”,可采取的措施有
 与FeO反应的化学方程式:
与FeO反应的化学方程式: 和
和(2)“除
 、
、 ”,当溶液中
”,当溶液中 时,溶液中
时,溶液中 的最大值为
的最大值为 。[已知:
。[已知: ,
, ]
](3)“一系列操作”包括过滤和
(4)钛酸钡
 也是一种强介电化合物。工业上,以
也是一种强介电化合物。工业上,以 、
、 为原料,采用草酸盐共沉淀法制备草酸氧钛钡晶体
为原料,采用草酸盐共沉淀法制备草酸氧钛钡晶体 ,再高温煅烧制得
,再高温煅烧制得 粉末。
粉末。①
 水解所得
水解所得 经焙烧得到
经焙烧得到 ,写出
,写出 水解的化学方程式
水解的化学方程式②草酸与草酸盐在实验和工业生产中都起着重要的作用。常温,
 溶液呈
溶液呈 ,
, ]
]
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】新冠病毒已经给人类带来巨大灾难。研究表明,过氧乙酸(CH3COOOH)能有效地杀灭病毒。一种制备过氧乙酸工艺流程如图:

回答下列问题:
(1)“电解”发生反应为2NH4HSO4 (NH4)2S2O8+H2↑。在电解过程中,理论上电路中转移2mol电子,将生成
(NH4)2S2O8+H2↑。在电解过程中,理论上电路中转移2mol电子,将生成______ L(标准状况下)H2。
(2)“水解”时又生成了NH4HSO4,写出该反应的化学方程式:______ 。
(3)分离H2O2溶液时,采取“减压蒸馏”,目的是______ 。
(4)“合成”反应为可逆反应,写出该反应的化学方程式:_______ 。
(5)过氧乙酸浓度测定
取amL过氧乙酸溶液,用硫酸使溶液酸化,再用浓度为bmol•L-1的KMnO4标准溶液滴定其中的H2O2(2MnO +5H2O2+6H+=2Mn2++5O2↑+8H2O),耗用的KMnO4标准溶液的体积为V1mL(滴定过程中KMnO4不与过氧乙酸反应)。
+5H2O2+6H+=2Mn2++5O2↑+8H2O),耗用的KMnO4标准溶液的体积为V1mL(滴定过程中KMnO4不与过氧乙酸反应)。
另取amL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟KI反应生成I2(H2O2+2I-+2H+=I2+2H2O;CH3COOOH+2I-+2H+=CH3COOH+I2+H2O)。再用浓度为cmol•L-1的Na2S2O3标准溶液滴定生成的I2(I2+2S2O =S4O
=S4O +2I-),耗用Na2S2O3的体积为V2mL。过氧乙酸的浓度为
+2I-),耗用Na2S2O3的体积为V2mL。过氧乙酸的浓度为______ mol•L-1(用含a、b、c、V1、V2的代数式表示)。

回答下列问题:
(1)“电解”发生反应为2NH4HSO4
 (NH4)2S2O8+H2↑。在电解过程中,理论上电路中转移2mol电子,将生成
(NH4)2S2O8+H2↑。在电解过程中,理论上电路中转移2mol电子,将生成(2)“水解”时又生成了NH4HSO4,写出该反应的化学方程式:
(3)分离H2O2溶液时,采取“减压蒸馏”,目的是
(4)“合成”反应为可逆反应,写出该反应的化学方程式:
(5)过氧乙酸浓度测定
取amL过氧乙酸溶液,用硫酸使溶液酸化,再用浓度为bmol•L-1的KMnO4标准溶液滴定其中的H2O2(2MnO
 +5H2O2+6H+=2Mn2++5O2↑+8H2O),耗用的KMnO4标准溶液的体积为V1mL(滴定过程中KMnO4不与过氧乙酸反应)。
+5H2O2+6H+=2Mn2++5O2↑+8H2O),耗用的KMnO4标准溶液的体积为V1mL(滴定过程中KMnO4不与过氧乙酸反应)。另取amL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟KI反应生成I2(H2O2+2I-+2H+=I2+2H2O;CH3COOOH+2I-+2H+=CH3COOH+I2+H2O)。再用浓度为cmol•L-1的Na2S2O3标准溶液滴定生成的I2(I2+2S2O
 =S4O
=S4O +2I-),耗用Na2S2O3的体积为V2mL。过氧乙酸的浓度为
+2I-),耗用Na2S2O3的体积为V2mL。过氧乙酸的浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】请按要求回答下列问题:
(1)25 ℃时,向纯水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为_____________ ,由水电离出的c(OH-)=________ mol·L-1。
(2)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
①25 ℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为___________________________ 。(用a b c表示)
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为_________ 。
(3)室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:

试分析图中a、b、c、d四个点,水的电离程度最大的是________ ;在b点,溶液中各离子浓度由大到小的排列顺序是_____________________________ 。
(1)25 ℃时,向纯水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为
(2)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为
(3)室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:

试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,溶液中
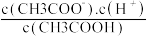
_______ (填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式_______________________________ 。
(2)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因_______________________ 。加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为_______________________________ 。
(3)常温下向20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分 数随溶液pH变化的情况如下:
数随溶液pH变化的情况如下:
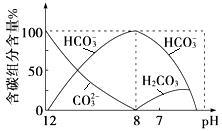
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32-________ (填“能”或“不能”)大量共存;
②当pH=7时,溶液中含碳元素的主要微粒有__________ 、_________ ,溶液中含量最多的三种微粒的物质的量浓度的大小关系为_______________________ ;
(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,溶液中
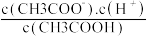
(2)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因
(3)常温下向20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分
 数随溶液pH变化的情况如下:
数随溶液pH变化的情况如下:
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32-
②当pH=7时,溶液中含碳元素的主要微粒有
您最近一年使用:0次
【推荐2】开发稳定高效的脱硫脱硝工艺是当前国内外研究的热点。
(1)天然气中含有的H2S会腐蚀管道和设备,可在1200℃下进行脱硫处理,其中涉及H2S与O2的反应,产物为SO2和水蒸气。若1molH2S参与该反应放热586.16kJ,则该反应的热化学方程式是__ 。
(2)烟气中的SO2可用“双碱法”洗除:先用NaOH溶液吸收烟气中的SO2,再往所得溶液中加入CaO,反应得到NaOH和CaSO3,原理可表示为:NaOH(aq) Na2SO3(aq)。
Na2SO3(aq)。
①Na2SO3溶液中阴离子的浓度由大到小的顺序:__ 。
②“双碱法”洗除SO2的优点是__ (任写一点)。
(3)过二硫酸钾(K2S2O8)是一种白色、无味晶体,溶于水,不溶于乙醇,有强氧化性。可作为燃煤锅炉烟气脱硝的氧化剂。
①S2O82-的结构式为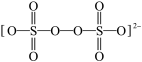 ,则过二硫酸钾(K2S2O8)所含化学键有:
,则过二硫酸钾(K2S2O8)所含化学键有:__ ,1个S2O82-中含有化合价为-1价的氧原子的个数是___ 。
②脱硝过程中依次发生两步反应:第1步K2S2O8将NO氧化成HNO2,第2步K2S2O8继续氧化HNO2,第2步的氧化产物为__ 。
③实验室中通过电解饱和KHSO4水溶液的方法制备K2S2O8。
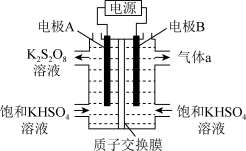
电极B为电解池__ 极(填“阳”或“阴”,气体a为__ (写化学式),电极A的电极反应式为__ 。
(1)天然气中含有的H2S会腐蚀管道和设备,可在1200℃下进行脱硫处理,其中涉及H2S与O2的反应,产物为SO2和水蒸气。若1molH2S参与该反应放热586.16kJ,则该反应的热化学方程式是
(2)烟气中的SO2可用“双碱法”洗除:先用NaOH溶液吸收烟气中的SO2,再往所得溶液中加入CaO,反应得到NaOH和CaSO3,原理可表示为:NaOH(aq)
 Na2SO3(aq)。
Na2SO3(aq)。①Na2SO3溶液中阴离子的浓度由大到小的顺序:
②“双碱法”洗除SO2的优点是
(3)过二硫酸钾(K2S2O8)是一种白色、无味晶体,溶于水,不溶于乙醇,有强氧化性。可作为燃煤锅炉烟气脱硝的氧化剂。
①S2O82-的结构式为
 ,则过二硫酸钾(K2S2O8)所含化学键有:
,则过二硫酸钾(K2S2O8)所含化学键有:②脱硝过程中依次发生两步反应:第1步K2S2O8将NO氧化成HNO2,第2步K2S2O8继续氧化HNO2,第2步的氧化产物为
③实验室中通过电解饱和KHSO4水溶液的方法制备K2S2O8。

电极B为电解池
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】用滴定法测定某醋酸溶液样品中醋酸的含量,操作如下已知:该条件下,醋酸和NaOH以物质的量1︰1反应时得到溶液的pH为8.7。
i.准确量取10.00 mL醋酸溶液样品,加入蒸馏水至总体积为100.00 mL,取其中20.00 mL进行滴定实验,用酸度计测量溶液的pH变化;
ⅱ.逐滴滴入0.1000 mol/L的NaOH溶液,当酸度计显示pH=8.7时停止滴定,记录消耗的NaOH溶液的体积 ;
;
ⅲ.平行测定多次(数据见表1);
iv.分析处理数据。
表1:实验数据记录表
(1)醋酸的电离方程式为_________ 。
(2)第1次滴定曲线如图所示,下列说法正确的是_____ 。
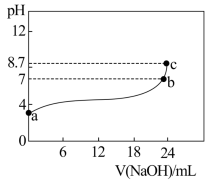
A.a点溶液:
B.b点溶液: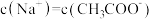
C.c点溶液:
(3)滴定过程中,从a点到c点水电离出的 逐渐
逐渐______ (填“增大”、“减小”或“不变”).用平衡移动原理解释:___________ 。
(4)根据表1中的有效数据,计算消耗的NaOH溶液的平均体积 =
=__________ mL。该醋酸溶液样品中醋酸的含量是__________ g/100mL。
i.准确量取10.00 mL醋酸溶液样品,加入蒸馏水至总体积为100.00 mL,取其中20.00 mL进行滴定实验,用酸度计测量溶液的pH变化;
ⅱ.逐滴滴入0.1000 mol/L的NaOH溶液,当酸度计显示pH=8.7时停止滴定,记录消耗的NaOH溶液的体积
 ;
;ⅲ.平行测定多次(数据见表1);
iv.分析处理数据。
表1:实验数据记录表
| 编号 | 1 | 2 | 3 | 4 |
 /mL /mL | 23.99 | 25.00 | 24.01 | 24.00 |
(2)第1次滴定曲线如图所示,下列说法正确的是

A.a点溶液:

B.b点溶液:
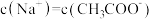
C.c点溶液:

(3)滴定过程中,从a点到c点水电离出的
 逐渐
逐渐(4)根据表1中的有效数据,计算消耗的NaOH溶液的平均体积
 =
=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化铬绿(Cr2O3)的性质独特,在冶金、颜料等领域有着不可替代的地位。一种利用淀粉水热还原铬酸钠制备氧化铬绿的工艺流程如下:

已知:①向含少量Na2CO3的铬酸钠碱性溶液中通入CO2可制得不同碳化率的铬酸钠碳化母液;
②“还原”反应剧烈放热,可制得Cr(OH)3浆料。
(1)该工艺中“还原”反应最初使用的是蔗糖或甲醛,后来改用价格低廉的淀粉。请写出甲醛(HCHO)与铬酸钠(Na2CrO4)溶液反应的离子方程式_________ 。
(2)将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列有关说法错误 的是_____ (填标号)。
A 该反应一定无需加热即可进行 B 必要时可使用冷却水进行温度控制
C 铬酸钠可适当过量,使淀粉充分反应 D 应建造废水回收池,回收含铬废水
(3)测得反应完成后在不同恒温温度、不同碳化率下Cr(Ⅵ)还原率如下图。实际生产过程中Cr(Ⅵ)还原率可高达99.5%以上,“还原”阶段采用的最佳反应条件为_________ 。
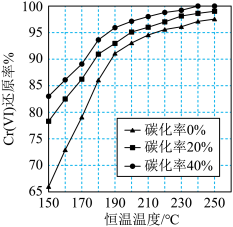
(4)滤液中所含溶质为_______ 。该水热法制备氧化铬绿工艺的优点有_________ 、________ (请写出两条)。
(5)由水热法制备的氢氧化铬为无定型氢氧化铬[Cr(OH)3·nH2O]。将洗涤并干燥后的氢氧化铬滤饼充分煅烧,质量损失与固体残留质量比为9:19,经计算得出n=_________ 。
(6)重铬酸钠(Na2Cr2O7·H2O)与硫酸铵热分解法也是一种生产氧化铬绿的方法,生产过程中产生的气体对环境无害,其化学反应方程式为_________ 。

已知:①向含少量Na2CO3的铬酸钠碱性溶液中通入CO2可制得不同碳化率的铬酸钠碳化母液;
②“还原”反应剧烈放热,可制得Cr(OH)3浆料。
(1)该工艺中“还原”反应最初使用的是蔗糖或甲醛,后来改用价格低廉的淀粉。请写出甲醛(HCHO)与铬酸钠(Na2CrO4)溶液反应的离子方程式
(2)将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列有关说法
A 该反应一定无需加热即可进行 B 必要时可使用冷却水进行温度控制
C 铬酸钠可适当过量,使淀粉充分反应 D 应建造废水回收池,回收含铬废水
(3)测得反应完成后在不同恒温温度、不同碳化率下Cr(Ⅵ)还原率如下图。实际生产过程中Cr(Ⅵ)还原率可高达99.5%以上,“还原”阶段采用的最佳反应条件为

(4)滤液中所含溶质为
(5)由水热法制备的氢氧化铬为无定型氢氧化铬[Cr(OH)3·nH2O]。将洗涤并干燥后的氢氧化铬滤饼充分煅烧,质量损失与固体残留质量比为9:19,经计算得出n=
(6)重铬酸钠(Na2Cr2O7·H2O)与硫酸铵热分解法也是一种生产氧化铬绿的方法,生产过程中产生的气体对环境无害,其化学反应方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】镍电池的电极活性材料为多组分合金(主要成分为镍、钴,还含有铝、铁等),可重新回收利用。利用废镍电池资源化生产醋酸钴晶体 的工艺流程如下。
的工艺流程如下。
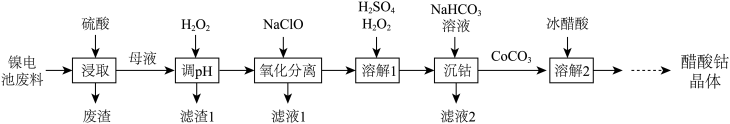
已知:①浸取母液中除铝元素外,其他金属元素的化合价均为 价。
价。
②部分金属阳离子沉淀的 如下表。
如下表。
请回答下列问题:
(1)“浸取”时可以提高浸取率的操作有_______ (任写1条)。
(2)“调 ”时溶液的
”时溶液的 范围是
范围是_______ ,所得滤渣1的主要成分为_______ (填化学式)。
(3)“氧化分离”操作控制溶液 ,加入
,加入 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)“溶解1”操作中加入 的作用为
的作用为_______ ,“沉钴”操作过程中发生反应的离子方程式为_______ 。
(5)“溶解2”操作后得到醋酸钴晶体,要使该醋酸钴晶体的纯度更高,所采取的实验操作名称应为_______ 。
(6)碱金属可以插入石墨层中,钾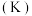 的石墨插层化合物具有超导性,其中K层平行于石墨层。图1为其晶胞图,垂直于石墨层方向的原子投影如图2所示。
的石墨插层化合物具有超导性,其中K层平行于石墨层。图1为其晶胞图,垂直于石墨层方向的原子投影如图2所示。

C—C键的键长为 ,则K层中m与n两个K原子之间的距离为
,则K层中m与n两个K原子之间的距离为_______  ,设
,设 为阿伏加德罗常数的值,若晶胞参数分别为
为阿伏加德罗常数的值,若晶胞参数分别为 、
、 、
、 ,则该石墨插层化合物的晶胞密度为
,则该石墨插层化合物的晶胞密度为_______  (用含x、y、z、
(用含x、y、z、 的代数式表示)。
的代数式表示)。
 的工艺流程如下。
的工艺流程如下。
已知:①浸取母液中除铝元素外,其他金属元素的化合价均为
 价。
价。②部分金属阳离子沉淀的
 如下表。
如下表。| 沉淀物 |  |  |  |  |  |  |
开始沉淀 | 2.2 | 7.4 | 7.6 | 0.1 | 4.0 | 7.6 |
完全沉淀 | 3.2 | 8.9 | 9.2 | 1.1 | 5.2 | 9.2 |
(1)“浸取”时可以提高浸取率的操作有
(2)“调
 ”时溶液的
”时溶液的 范围是
范围是(3)“氧化分离”操作控制溶液
 ,加入
,加入 发生反应的离子方程式为
发生反应的离子方程式为(4)“溶解1”操作中加入
 的作用为
的作用为(5)“溶解2”操作后得到醋酸钴晶体,要使该醋酸钴晶体的纯度更高,所采取的实验操作名称应为
(6)碱金属可以插入石墨层中,钾
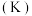 的石墨插层化合物具有超导性,其中K层平行于石墨层。图1为其晶胞图,垂直于石墨层方向的原子投影如图2所示。
的石墨插层化合物具有超导性,其中K层平行于石墨层。图1为其晶胞图,垂直于石墨层方向的原子投影如图2所示。
C—C键的键长为
 ,则K层中m与n两个K原子之间的距离为
,则K层中m与n两个K原子之间的距离为 ,设
,设 为阿伏加德罗常数的值,若晶胞参数分别为
为阿伏加德罗常数的值,若晶胞参数分别为 、
、 、
、 ,则该石墨插层化合物的晶胞密度为
,则该石墨插层化合物的晶胞密度为 (用含x、y、z、
(用含x、y、z、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】镍是一种常用的催化剂。以红土镍矿(主要含有Fe2O3、FeO、NiO、SiO2等)为原料,制取纳米镍粉,同时获得净水剂黄钠铁矾 的工艺流程如下:
的工艺流程如下:

回答下列问题:
(1)黄钠铁矾 中,铁的化合价为
中,铁的化合价为___________ 价;黄钠铁矾能净水的原因是___________ 。
(2)过滤操作时要遵循“一贴、二低、三靠”的原则,其中“二低”指的是滤纸边缘略低于漏斗口、___________ 。
(3)“沉铁”过程加入Na2CO3的目的是___________ ,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、pH的关系如图所示(图中阴影部分表示的是黄钠铁矾稳定存在区域)。若反应在120℃时进行,加入的Na2CO3偏多,则所得黄钠铁矾中混有的杂质是___________ (填化学式);检验沉铁反应是否完全的方法是___________ 。

(4)“转化”过程,向“过滤II”所得滤液(富含Ni2+)中加入N2H4,控制溶液中NaOH的浓度,可得到不同晶态物质( 、Ni或二者的混合物)。当生成
、Ni或二者的混合物)。当生成 和Ni的物质的量之比为1:2时,该反应的离子方程式为
和Ni的物质的量之比为1:2时,该反应的离子方程式为___________ ;在其他条件不变的情况下,随NaOH浓度增大,产物中Ni的含量增加,原因是___________ 。
(5)化学镀镍是金属表面镀镍的常用方法,以NiSO4为镀液,次亚磷酸钠(NaH2PO2)为还原剂,在90℃的酸性溶液中发生反应,NaH2PO2被氧化为亚磷酸(H3PO3)。写出化学镀镍反应的离子方程式:___________ 。
 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)黄钠铁矾
 中,铁的化合价为
中,铁的化合价为(2)过滤操作时要遵循“一贴、二低、三靠”的原则,其中“二低”指的是滤纸边缘略低于漏斗口、
(3)“沉铁”过程加入Na2CO3的目的是

(4)“转化”过程,向“过滤II”所得滤液(富含Ni2+)中加入N2H4,控制溶液中NaOH的浓度,可得到不同晶态物质(
 、Ni或二者的混合物)。当生成
、Ni或二者的混合物)。当生成 和Ni的物质的量之比为1:2时,该反应的离子方程式为
和Ni的物质的量之比为1:2时,该反应的离子方程式为(5)化学镀镍是金属表面镀镍的常用方法,以NiSO4为镀液,次亚磷酸钠(NaH2PO2)为还原剂,在90℃的酸性溶液中发生反应,NaH2PO2被氧化为亚磷酸(H3PO3)。写出化学镀镍反应的离子方程式:
您最近一年使用:0次