工业上可将CO2、H2O合成CH3OH从而有效降低企业二氧化碳的排放量,其中涉及的主要反应如下:
Ⅰ.CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
Ⅱ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2<0
CH3OH(g)+H2O(g) △H2<0
Ⅲ.CO2(g)+H2(g) CO(g)+H2O(g) △H3=+40.9kJ/mol
CO(g)+H2O(g) △H3=+40.9kJ/mol
(1)下列关于上述反应说法正确的是____ (填序号)。
(2)使用某种新型催化剂,将1molCO2和2molH2在1L密闭容器中进行反应,且仅发生反应Ⅱ、Ⅲ,CO2的平衡转化率和甲醇的选择率随温度的变化趋势如图所示。(甲醇的选择率:转化的CO2中生成甲醇的物质的量分数)
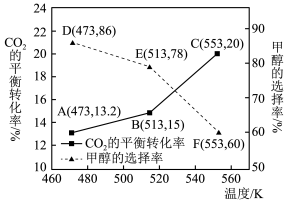
①达到平衡时,反应体系内甲醇的产量最高的是___ (填“473K”、“513K”或“553K”)。
②计算反应Ⅲ在553K时的平衡常数K=___ (计算结果保留3位小数)。
③随着温度的升高,CO2的平衡转化率逐渐增加但是甲醇的选择性却逐渐降低的原因是___ 。
(3)通过实验表明,CO2在一定条件下可以被电化学还原。
①写出CO2在酸性介质中电还原为甲醇的电极反应式为____ 。
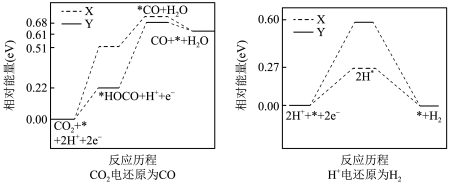
②两种不同催化剂X、Y上,CO2电还原为CO的反应进程中(H+被电还原为H2同时发生)相对能量变化如图。由此判断,更易催化CO2电还原为CO的催化剂是____ (填“X”或“Y”)。
Ⅰ.CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1Ⅱ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2<0
CH3OH(g)+H2O(g) △H2<0Ⅲ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+40.9kJ/mol
CO(g)+H2O(g) △H3=+40.9kJ/mol(1)下列关于上述反应说法正确的是
| A.反应Ⅰ的△H1>0 | B.反应Ⅱ在较低温度下可以自发进行 |
| C.反应Ⅲ的△S=0 | D.对于反应Ⅱ,高温高压有利于提高甲醇平衡产率 |

①达到平衡时,反应体系内甲醇的产量最高的是
②计算反应Ⅲ在553K时的平衡常数K=
③随着温度的升高,CO2的平衡转化率逐渐增加但是甲醇的选择性却逐渐降低的原因是
(3)通过实验表明,CO2在一定条件下可以被电化学还原。
①写出CO2在酸性介质中电还原为甲醇的电极反应式为
②两种不同催化剂X、Y上,CO2电还原为CO的反应进程中(H+被电还原为H2同时发生)相对能量变化如图。由此判断,更易催化CO2电还原为CO的催化剂是

更新时间:2022-02-24 13:13:25
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】我国高含硫天然气资源丰富,天然气脱硫和甲烷与硫化氢重整制氢具有重要的现实意义。回答下列问题:
(1)天然气脱硫工艺涉及如下反应:
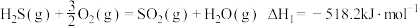

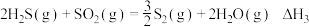
则
_______ 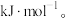
(2)甲烷与 重整制氢是一条全新的
重整制氢是一条全新的 转化与制氢技术路线。为了研究甲烷对
转化与制氢技术路线。为了研究甲烷对 制氢的影响,理论计算表明,原料初始组成
制氢的影响,理论计算表明,原料初始组成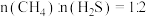 ,在体系压强为0.1MPa,反应
,在体系压强为0.1MPa,反应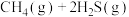

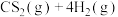 达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示:
达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示:

①图中表示 变化的曲线分别是_______ 、_______ 。反应达平衡的标志是_______ (填标号)。
A. B.
B.  的体积分数不再变化
的体积分数不再变化
C. 不再变化 D.混合气体的密度不再改变
不再变化 D.混合气体的密度不再改变
②由图可知该反应的△H_______ 0(填“>”“<”或“=”),判断的理由是_______ 。
③M点对应温度下, 的转化率为
的转化率为 _______ ;950℃时该反应的 
_______  。
。
(3) 燃料电池的原理如图所示。电池的负极反应式为
燃料电池的原理如图所示。电池的负极反应式为_______ 。该电池理论输出电压为0.800 V,则该燃料电池的理论效率为_______ (已知:燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比;法拉第常数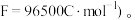

(1)天然气脱硫工艺涉及如下反应:
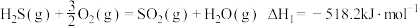

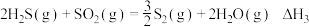
则

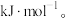
(2)甲烷与
 重整制氢是一条全新的
重整制氢是一条全新的 转化与制氢技术路线。为了研究甲烷对
转化与制氢技术路线。为了研究甲烷对 制氢的影响,理论计算表明,原料初始组成
制氢的影响,理论计算表明,原料初始组成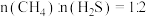 ,在体系压强为0.1MPa,反应
,在体系压强为0.1MPa,反应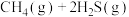

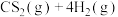 达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示:
达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示:
①图中表示 变化的曲线分别是
A.
 B.
B.  的体积分数不再变化
的体积分数不再变化 C.
 不再变化 D.混合气体的密度不再改变
不再变化 D.混合气体的密度不再改变②由图可知该反应的△H
③M点对应温度下,
 的转化率为
的转化率为 
 。
。(3)
 燃料电池的原理如图所示。电池的负极反应式为
燃料电池的原理如图所示。电池的负极反应式为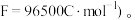

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】I.利用CO2直接加氢合成二甲醚包括以下三个相互联系的反应:
甲醇的合成CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
甲醇脱水2CH3OH(g)⇌CH3OCH3(g)+H2O(g)
逆水汽变换CO2(g)+H2(g)⇌CO(g)+H2O(g)
相关物质变化的焓变示意图如下:
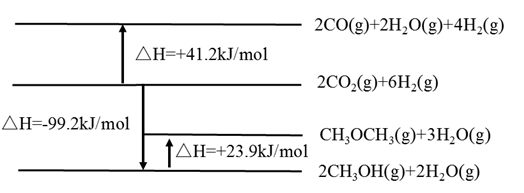
请回答:
(1)请写出CO2直接加氢合成二甲醚的热化学方程式:_____________________ 。
(2)保持恒温恒压的条件,当装置a充入1molCO2、装置b充入2molCO2,在其他条件不变时,请在下图中分别画出平衡时CH3OCH3的体积分数随投料比[ ]变化的曲线图,请用a、b标注曲线
]变化的曲线图,请用a、b标注曲线____________ 。

(3)在恒容密闭容器里按体积比为1:3充入二氧化碳和氢气,一定条件下反应达到平衡状态,当改变反应的某个条件后, 下列变化能说明平衡一定向逆反应方向移动的是__________ 。
A.正反应速率先增大后逐渐减小 B.逆反应速率先增大后逐渐减小
C.化学平衡常数K值增大 D.反应物的体积百分含量增大
E.混合气体的密度减小 F.氢气的转化率减小
(4)在恒压、CO2和H2起始物质的量之比为1:3的条件下,CO2平衡转化率和平衡时二甲醚的选择性随温度的变化如图。
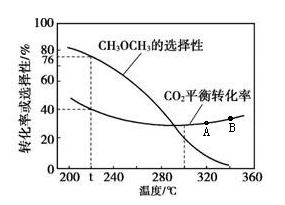
CH3OCH3的选择性=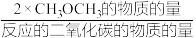 ×100%
×100%
①CO2平衡转化率随温度升高显示如图所示变化的原因是____________ 。
②关于合成二甲醚工艺的理解,下列说法正确的是__________ 。
A.合成二甲醚的反应在A点和B点时的化学平衡常数K(A)小于K(B)
B.当温度、压强一定时,在原料气(CO2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
C.其他条件不变,在恒容条件下的二甲醚平衡选择性比恒压条件下的平衡选择性低
D.由图象可知,CO2加氢合成二甲醚应该选择具有良好的低温活性的催化剂
II.汽车尾气是城市空气污染的一个重要因素,常用以下反应净化汽车尾气:2NO(g)+2CO(g) 2CO2(g)+N2(g)在某温度T1℃下,2 L密闭容器中充入NO、CO各0.8mol,测得不同时间的NO和CO物质的量如下表:
2CO2(g)+N2(g)在某温度T1℃下,2 L密闭容器中充入NO、CO各0.8mol,测得不同时间的NO和CO物质的量如下表:
(5)上述反应达到平衡后,继续加入NO、CO、CO2各0.4mol和N2______ mol时,平衡不移动。
甲醇的合成CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
甲醇脱水2CH3OH(g)⇌CH3OCH3(g)+H2O(g)
逆水汽变换CO2(g)+H2(g)⇌CO(g)+H2O(g)
相关物质变化的焓变示意图如下:

请回答:
(1)请写出CO2直接加氢合成二甲醚的热化学方程式:
(2)保持恒温恒压的条件,当装置a充入1molCO2、装置b充入2molCO2,在其他条件不变时,请在下图中分别画出平衡时CH3OCH3的体积分数随投料比[
 ]变化的曲线图,请用a、b标注曲线
]变化的曲线图,请用a、b标注曲线
(3)在恒容密闭容器里按体积比为1:3充入二氧化碳和氢气,一定条件下反应达到平衡状态,当改变反应的某个条件后, 下列变化能说明平衡一定向逆反应方向移动的是
A.正反应速率先增大后逐渐减小 B.逆反应速率先增大后逐渐减小
C.化学平衡常数K值增大 D.反应物的体积百分含量增大
E.混合气体的密度减小 F.氢气的转化率减小
(4)在恒压、CO2和H2起始物质的量之比为1:3的条件下,CO2平衡转化率和平衡时二甲醚的选择性随温度的变化如图。

CH3OCH3的选择性=
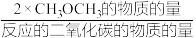 ×100%
×100%①CO2平衡转化率随温度升高显示如图所示变化的原因是
②关于合成二甲醚工艺的理解,下列说法正确的是
A.合成二甲醚的反应在A点和B点时的化学平衡常数K(A)小于K(B)
B.当温度、压强一定时,在原料气(CO2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
C.其他条件不变,在恒容条件下的二甲醚平衡选择性比恒压条件下的平衡选择性低
D.由图象可知,CO2加氢合成二甲醚应该选择具有良好的低温活性的催化剂
II.汽车尾气是城市空气污染的一个重要因素,常用以下反应净化汽车尾气:2NO(g)+2CO(g)
 2CO2(g)+N2(g)在某温度T1℃下,2 L密闭容器中充入NO、CO各0.8mol,测得不同时间的NO和CO物质的量如下表:
2CO2(g)+N2(g)在某温度T1℃下,2 L密闭容器中充入NO、CO各0.8mol,测得不同时间的NO和CO物质的量如下表:| 时间(s) | 0 | 2 | 4 | 6 | 8 | 10 |
| n(NO)(mol) | 0.8 | 0.64 | 0.52 | 0.44 | 0.40 | 0.40 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】 (丙烯)是重要基本有机原料。
(丙烯)是重要基本有机原料。 (丙烷)催化脱氢制C3H6过程如下:
(丙烷)催化脱氢制C3H6过程如下:
Ⅰ.主反应:
 ;
;
Ⅱ.副反应:

回答下列问题:
(1)已知断裂1 mol下列化学键所需能量如下表:
上述主反应的
___________  。
。
(2)一定条件下, 催化脱氢制
催化脱氢制 发生上述Ⅰ、Ⅱ反应,
发生上述Ⅰ、Ⅱ反应, 和
和 的平衡体积分数与温度、压强的关系如图所示(图中压强分别为
的平衡体积分数与温度、压强的关系如图所示(图中压强分别为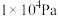 和
和 )。
)。 时,图中表示
时,图中表示 和
和 体积分数变化的曲线分别为
体积分数变化的曲线分别为___________ 、___________ 。
②提高 催化脱氢制
催化脱氢制 的反应平衡转化率的方法是
的反应平衡转化率的方法是___________ (任写一种)。
(3)在压力(117.5 kPa)恒定,以 作为稀释气,不同水烃比[
作为稀释气,不同水烃比[ 、10、15]时,
、10、15]时, 催化脱氢制备
催化脱氢制备 反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图所示。
反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图所示。
ⅰ.丙烷的浓度过低;
ⅱ.___________ 。
②M点对应条件下,若 的选择性为60%,则反应Ⅰ的分压平衡常数
的选择性为60%,则反应Ⅰ的分压平衡常数 为
为___________ kPa[ 的选择性
的选择性 ]。
]。
(4)利用 的弱氧化性,科研人员开发了
的弱氧化性,科研人员开发了 氧化脱氢制
氧化脱氢制 的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。
的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。___________ 。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是___________ 。
(5)研究表明, 氧化脱氢制
氧化脱氢制 的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的
的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的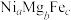 的立方晶胞结构如图4所示。已知晶胞的边长为n pm,设
的立方晶胞结构如图4所示。已知晶胞的边长为n pm,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。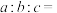
___________ 。
②该晶体密度是___________  (用含n、
(用含n、 的代数式表示)。
的代数式表示)。
 (丙烯)是重要基本有机原料。
(丙烯)是重要基本有机原料。 (丙烷)催化脱氢制C3H6过程如下:
(丙烷)催化脱氢制C3H6过程如下:Ⅰ.主反应:

 ;
;Ⅱ.副反应:


回答下列问题:
(1)已知断裂1 mol下列化学键所需能量如下表:
| 化学键 |  |  |  |
能量/ | 436.0 | 413.4 | 344.7 |

 。
。(2)一定条件下,
 催化脱氢制
催化脱氢制 发生上述Ⅰ、Ⅱ反应,
发生上述Ⅰ、Ⅱ反应, 和
和 的平衡体积分数与温度、压强的关系如图所示(图中压强分别为
的平衡体积分数与温度、压强的关系如图所示(图中压强分别为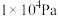 和
和 )。
)。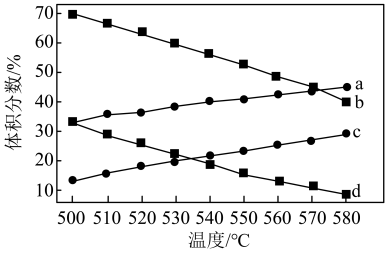
 时,图中表示
时,图中表示 和
和 体积分数变化的曲线分别为
体积分数变化的曲线分别为②提高
 催化脱氢制
催化脱氢制 的反应平衡转化率的方法是
的反应平衡转化率的方法是(3)在压力(117.5 kPa)恒定,以
 作为稀释气,不同水烃比[
作为稀释气,不同水烃比[ 、10、15]时,
、10、15]时, 催化脱氢制备
催化脱氢制备 反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图所示。
反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图所示。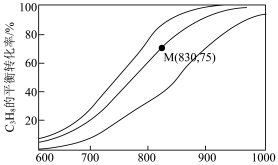
ⅰ.丙烷的浓度过低;
ⅱ.
②M点对应条件下,若
 的选择性为60%,则反应Ⅰ的分压平衡常数
的选择性为60%,则反应Ⅰ的分压平衡常数 为
为 的选择性
的选择性 ]。
]。(4)利用
 的弱氧化性,科研人员开发了
的弱氧化性,科研人员开发了 氧化脱氢制
氧化脱氢制 的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。
的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。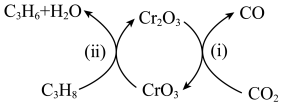
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是
(5)研究表明,
 氧化脱氢制
氧化脱氢制 的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的
的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的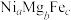 的立方晶胞结构如图4所示。已知晶胞的边长为n pm,设
的立方晶胞结构如图4所示。已知晶胞的边长为n pm,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。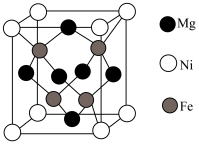
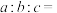
②该晶体密度是
 (用含n、
(用含n、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】I.能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)已知:C(s)+O2(g)=CO2(g) △H1=—393.5kJ·mol-1
H2(g)+ O2(g)=H2O(g) △H2=—241.8kJ·mol-1
O2(g)=H2O(g) △H2=—241.8kJ·mol-1
CO(g)+ O2(g)=CO2(g) △H3=—283.0kJ·mol-1
O2(g)=CO2(g) △H3=—283.0kJ·mol-1
则煤气化主要反应C(s)+H2O(g)=CO(g)+H2(g)的△H=____ 。
II.为了减少CO的排放,某环境研究小组以CO和H2为原料合成清洁能源二甲醚(DME),反应为4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) △H=—198kJ·mol-1。
CH3OCH3(g)+H2O(g) △H=—198kJ·mol-1。
(2)如图所示能正确反映平衡常数K随温度变化关系的曲线为____ (填曲线标记字母)。

(3)在一定温度下,向2.0L固定容积的密闭容器中充入2molH2和1molCO,经过一段时间后,反应4H2(g)+2CO(g) CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见表:
CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见表:
①0~20min的平均反应速率v(CO)=____ mol·L-1·min-1。
②达到平衡时,H2的转化率为____ 。
③在上述温度下,该反应的平衡常数K=____ 。
④能表明该反应达到平衡状态的是____ (填字母)。
A.CO的转化率等于H2O的产率 B.混合气体的平均相对分子质量不变
C.v(CO)与v(H2)的比值不变 D.混合气体的密度不变
⑤在上述温度下,向平衡后的2L容器中再充入0.4molH2和0.4molCH3OCH3(g),则化学平衡____ (填“向左”“向右”或“不”)移动。
(1)已知:C(s)+O2(g)=CO2(g) △H1=—393.5kJ·mol-1
H2(g)+
 O2(g)=H2O(g) △H2=—241.8kJ·mol-1
O2(g)=H2O(g) △H2=—241.8kJ·mol-1CO(g)+
 O2(g)=CO2(g) △H3=—283.0kJ·mol-1
O2(g)=CO2(g) △H3=—283.0kJ·mol-1则煤气化主要反应C(s)+H2O(g)=CO(g)+H2(g)的△H=
II.为了减少CO的排放,某环境研究小组以CO和H2为原料合成清洁能源二甲醚(DME),反应为4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g) △H=—198kJ·mol-1。
CH3OCH3(g)+H2O(g) △H=—198kJ·mol-1。(2)如图所示能正确反映平衡常数K随温度变化关系的曲线为

(3)在一定温度下,向2.0L固定容积的密闭容器中充入2molH2和1molCO,经过一段时间后,反应4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见表:
CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见表:| 时间/min | 0 | 20 | 40 | 80 | 100 |
| n(H2)/mol | 2.0 | 1.4 | 0.85 | 0.4 | — |
| n(CO)/mol | 1.0 | — | 0.425 | 0.2 | 0.2 |
| n(CH3OCH3)/mol | 0 | 0.15 | — | — | 0.4 |
| n(H2O)/mol | 0 | 0.15 | 0.2875 | 0.4 | 0.4 |
①0~20min的平均反应速率v(CO)=
②达到平衡时,H2的转化率为
③在上述温度下,该反应的平衡常数K=
④能表明该反应达到平衡状态的是
A.CO的转化率等于H2O的产率 B.混合气体的平均相对分子质量不变
C.v(CO)与v(H2)的比值不变 D.混合气体的密度不变
⑤在上述温度下,向平衡后的2L容器中再充入0.4molH2和0.4molCH3OCH3(g),则化学平衡
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)在C和 的反应体系中:
的反应体系中:
反应1:

反应2:
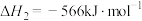
反应3:
 。
。
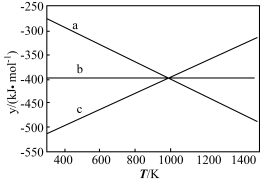
设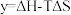 ,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是____ 。
(2)雨水中含有来自大气的 ,溶于水中的
,溶于水中的 进一步和水反应,发生电离:
进一步和水反应,发生电离:
①
②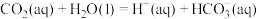 25℃时,反应②的平衡常数为
25℃时,反应②的平衡常数为 。
。
溶液中 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为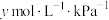 ,当大气压强为
,当大气压强为 ,大气中
,大气中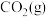 的物质的量分数为
的物质的量分数为 时,溶液中
时,溶液中 浓度为
浓度为_______  (写出表达式,考虑水的电离,忽略
(写出表达式,考虑水的电离,忽略 的电离)
的电离)
(3)在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应有:
的反应体系中,发生的主要反应有:
I.
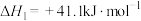
II.
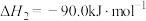
III.
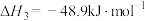
 时,往某密闭容器中按投料比
时,往某密闭容器中按投料比 充入
充入 和
和 。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。

①图中Y代表_______ (填化学式)。
②体系中 的物质的量分数受温度的影响不大,原因是
的物质的量分数受温度的影响不大,原因是_______ 。
③在下图中画出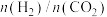 随温度变化趋势图
随温度变化趋势图_______ 。

(1)在C和
 的反应体系中:
的反应体系中:反应1:


反应2:

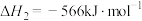
反应3:

 。
。设
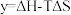 ,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
(2)雨水中含有来自大气的
 ,溶于水中的
,溶于水中的 进一步和水反应,发生电离:
进一步和水反应,发生电离:①

②
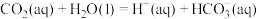 25℃时,反应②的平衡常数为
25℃时,反应②的平衡常数为 。
。溶液中
 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为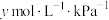 ,当大气压强为
,当大气压强为 ,大气中
,大气中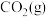 的物质的量分数为
的物质的量分数为 时,溶液中
时,溶液中 浓度为
浓度为 (写出表达式,考虑水的电离,忽略
(写出表达式,考虑水的电离,忽略 的电离)
的电离)(3)在某
 催化加氢制
催化加氢制 的反应体系中,发生的主要反应有:
的反应体系中,发生的主要反应有:I.

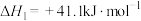
II.

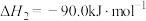
III.

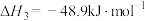
 时,往某密闭容器中按投料比
时,往某密闭容器中按投料比 充入
充入 和
和 。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
①图中Y代表
②体系中
 的物质的量分数受温度的影响不大,原因是
的物质的量分数受温度的影响不大,原因是③在下图中画出
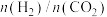 随温度变化趋势图
随温度变化趋势图
您最近一年使用:0次
【推荐3】基于CaSO4为载氧体的天然气燃烧是一种新型绿色的燃烧方式,CaSO4作为氧和热量的有效载体,能够高效低能耗地实现CO2的分离和捕获。其原理如下图所示:

(1)已知在燃料反应器中发生如下反应:
i.4CaSO4(s)+CH4(g)=4CaO(s)+CO2(g)+4SO2(g)+2H2O(g) ΔH1=akJ/mol
ii.CaSO4(s)+CH4(g)=CaS(s)+CO2(g)+2H2O(g) ΔH2=bkJ/mol
ⅲ. CaS(s)+3CaSO4(s)= 4CaO(s)+4SO2(g) ΔH3=ckJ/mol
①燃料反应器中主反应为_________ (填“i”“ii”或“ⅲ”)。
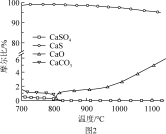
②反应i和ii的平衡常数Kp与温度的关系如图1,则a_______ 0(填“ >”“ =“或“<” );720℃时反应ⅲ的平衡常数Kp=________ 。

③下列措施可提高反应ii中甲烷平衡转化率和反应速率的是_______ 。
A.增加CaSO4固体的投入量 B.将水蒸气冷凝
C.升温 D.增大甲烷流量
(2)如图2所示,该燃料反应器最佳温度范围为850℃ -900℃之间,从化学反应原理的角度说明原因:______________________________________________________ 。
(3)空气反应器中发生的反应为CaS(s) +2O2(g)=CaSO4(s) ΔH4=dkJ/mol
①根据热化学原理推测该反应为__________ 反应。
②在天然气燃烧过程中,可循环利用的物质为________ 。
(4)该原理总反应的热化学方程式为_____________________________________________ 。

(1)已知在燃料反应器中发生如下反应:
i.4CaSO4(s)+CH4(g)=4CaO(s)+CO2(g)+4SO2(g)+2H2O(g) ΔH1=akJ/mol
ii.CaSO4(s)+CH4(g)=CaS(s)+CO2(g)+2H2O(g) ΔH2=bkJ/mol
ⅲ. CaS(s)+3CaSO4(s)= 4CaO(s)+4SO2(g) ΔH3=ckJ/mol
①燃料反应器中主反应为
②反应i和ii的平衡常数Kp与温度的关系如图1,则a

③下列措施可提高反应ii中甲烷平衡转化率和反应速率的是
A.增加CaSO4固体的投入量 B.将水蒸气冷凝
C.升温 D.增大甲烷流量
(2)如图2所示,该燃料反应器最佳温度范围为850℃ -900℃之间,从化学反应原理的角度说明原因:

(3)空气反应器中发生的反应为CaS(s) +2O2(g)=CaSO4(s) ΔH4=dkJ/mol
①根据热化学原理推测该反应为
②在天然气燃烧过程中,可循环利用的物质为
(4)该原理总反应的热化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】近日,科学家开发新型催化剂实现一氧化二氮对C4馏分中2-丁烯的气相选择性氧化,反应原理如图所示。

反应1:CH3CH=CHCH3(g)+N2O(g) CH3CH2COCH3(g)+N2(g) ΔH1;
CH3CH2COCH3(g)+N2(g) ΔH1;
反应2:CH3CH=CHCH3(g)+2N2O(g) 2CH3CHO(g)+2N2(g) ΔH2<0。
2CH3CHO(g)+2N2(g) ΔH2<0。
(1)几种共价键的键能数据如下表所示。
已知N2O的结构式为N=N=O。根据键能估算:ΔH1=_______ kJ·mol-1。
(2)在恒温恒容密闭容器中充入CH3CH=CHCH3(g)和N2O(g),发生上述反应1和反应2,下列情况不能说明反应已达到平衡状态的是_______(填字母)。
(3)一定温度下,向恒压密闭容器中充入CH3CH=CHCH3(g)和N2O(g),发生上述反应1和反应2,测得平衡体系中N2的体积分数与起始投料比[ ]的关系如图1所示。
]的关系如图1所示。

在M、N、Q三点中,CH3CH=CHCH3(g)的转化率由小到大排序为_______ (填字母)。图1中,N点的氮气的体积分数小于50%的原因是_______ 。
(4)反应1的速率方程为v正=k正c(CH3CH=CHH3)·c(N2O),v逆=k逆c(CH3CH2COCH3)·c(N2)(k正、k逆为正、逆反应速率常数,与温度、催化剂有关)。已知:阿伦尼乌斯经验公式为Rlnk=- (R为常数,T为温度,k为速率常数,Ea为活化能)。测得反应1在不同催化剂Cat1、Cat2作用下,速率常数与温度的倒数关系如图2所示。
(R为常数,T为温度,k为速率常数,Ea为活化能)。测得反应1在不同催化剂Cat1、Cat2作用下,速率常数与温度的倒数关系如图2所示。

催化效果较高的催化剂是_______ (填“Cat1”或“Cat2”)。
(5)在反应器中充入1mol2-丁烯和2molN2O(g),发生上述反应,测得2-丁烯的平衡转化率与温度、压强的关系如图3所示。X点时丁酮(CH3CH2COCH3)的选择性为 [CH3CH2COCH3的选择性=
[CH3CH2COCH3的选择性= ]。
]。

①其他条件不变,升高温度,2-丁烯的平衡转化率降低的原因是_______ 。p_______ 31kPa(填“>”“<”或“=”)。
②Y点反应1的压强平衡常数Kp为______________ (结果保留两位有效数字)。
(6)以熔融碳酸盐(如K2CO3)为电解质,丁烯(C4H8)/空气燃料电池的能量转化率较高。电池反应为C4H8+6O2=4CO2+4H2O负极反应式为_______ 。

反应1:CH3CH=CHCH3(g)+N2O(g)
 CH3CH2COCH3(g)+N2(g) ΔH1;
CH3CH2COCH3(g)+N2(g) ΔH1;反应2:CH3CH=CHCH3(g)+2N2O(g)
 2CH3CHO(g)+2N2(g) ΔH2<0。
2CH3CHO(g)+2N2(g) ΔH2<0。(1)几种共价键的键能数据如下表所示。
| 共价键 | C-H | C-C | C=C | C=O | N≡N | N=O | N=N |
| 键能/kJ·mol | 413 | 347 | 614 | 745 | 945 | 607 | 418 |
(2)在恒温恒容密闭容器中充入CH3CH=CHCH3(g)和N2O(g),发生上述反应1和反应2,下列情况不能说明反应已达到平衡状态的是_______(填字母)。
| A.混合气体密度不随时间变化 |
| B.混合气体平均摩尔质量不随时间变化 |
| C.混合气体总压强不随时间变化 |
| D.混合气体中N2浓度不随时间变化 |
 ]的关系如图1所示。
]的关系如图1所示。
在M、N、Q三点中,CH3CH=CHCH3(g)的转化率由小到大排序为
(4)反应1的速率方程为v正=k正c(CH3CH=CHH3)·c(N2O),v逆=k逆c(CH3CH2COCH3)·c(N2)(k正、k逆为正、逆反应速率常数,与温度、催化剂有关)。已知:阿伦尼乌斯经验公式为Rlnk=-
 (R为常数,T为温度,k为速率常数,Ea为活化能)。测得反应1在不同催化剂Cat1、Cat2作用下,速率常数与温度的倒数关系如图2所示。
(R为常数,T为温度,k为速率常数,Ea为活化能)。测得反应1在不同催化剂Cat1、Cat2作用下,速率常数与温度的倒数关系如图2所示。
催化效果较高的催化剂是
(5)在反应器中充入1mol2-丁烯和2molN2O(g),发生上述反应,测得2-丁烯的平衡转化率与温度、压强的关系如图3所示。X点时丁酮(CH3CH2COCH3)的选择性为
 [CH3CH2COCH3的选择性=
[CH3CH2COCH3的选择性= ]。
]。
①其他条件不变,升高温度,2-丁烯的平衡转化率降低的原因是
②Y点反应1的压强平衡常数Kp为
(6)以熔融碳酸盐(如K2CO3)为电解质,丁烯(C4H8)/空气燃料电池的能量转化率较高。电池反应为C4H8+6O2=4CO2+4H2O负极反应式为
您最近一年使用:0次
【推荐2】CO2的综合利用,通过化学的方法实现CO2的资源化利用是一种理想的CO2减排途径。
Ⅰ.利用酸性水溶液电解池在铂电极上捕集CO2制储氢物质HCOOH
(1)CO2被___________ (填“氧化”或“还原”)为HCOOH,该铂电极为___________ 极。
(2)写出该铂电极的电极方程式___________ 。
(3)当电路中转移3 mol电子时,理论上可生成HCOOH___________ g。
Ⅱ.利用CO2制备CO
一定温度下,在恒容密闭容器中投入一定量CO2和H2进行反应:CO2(g) + H2(g) CO(g) + H2O(g)。
CO(g) + H2O(g)。
(4)下列事实能说明上述反应达到平衡状态的是__________。
(5)在恒定温度与容积下,可以提高CO2平衡转化率的措施有__________。
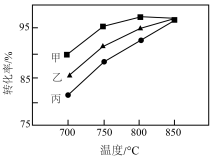
(6)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是_________。
Ⅲ.利用CO2制备甲醇
一定条件下,向恒容密闭容器中通入一定量的CO2和H2.涉及反应如下:
主反应:CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH = −90.4 kJ/mol
CH3OH(g) + H2O(g) ΔH = −90.4 kJ/mol
副反应:CO2(g) + H2(g) CO(g) + H2O(g) ΔH = +40.5 kJ/mol
CO(g) + H2O(g) ΔH = +40.5 kJ/mol
(7)其他条件相同,不同压强下,平衡时CO2转化率随温度的变化关系如图所示。
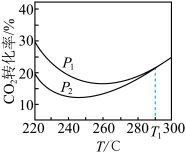
①压强P1___________ P2(填“<”或“>”)。
②图中温度高于T1时,两条曲线重叠的原因是:___________ 。
(8)实际工业生产中,需要在260℃、压强恒为4.0 MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04 mol/min、n(CO2):n(H2) = 1:3,持续通入原料,同时控制出气流量。
①为了维持体系压强恒定,需控制出气流量小于进气流量,原因为:___________ 。
②已知出气流量为0.03 mol/min,单位时间CO2的转化率为60 %,则流出气体中CO的百分含量为___________ 。
Ⅰ.利用酸性水溶液电解池在铂电极上捕集CO2制储氢物质HCOOH
(1)CO2被
(2)写出该铂电极的电极方程式
(3)当电路中转移3 mol电子时,理论上可生成HCOOH
Ⅱ.利用CO2制备CO
一定温度下,在恒容密闭容器中投入一定量CO2和H2进行反应:CO2(g) + H2(g)
 CO(g) + H2O(g)。
CO(g) + H2O(g)。(4)下列事实能说明上述反应达到平衡状态的是__________。
| A.体系内n(CO) : n(H2O) = 1 : 1 | B.体系压强不再发生变化 |
| C.体系内各物质浓度不再发生变化 | D.体系内CO的体积分数不再发生变化 |
(5)在恒定温度与容积下,可以提高CO2平衡转化率的措施有__________。
| A.向反应容器中充入H2 | B.向反应容器中充入CO2 |
| C.添加更有效的催化剂 | D.利用合适试剂干燥混合气体 |
(6)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是_________。

| A.850℃下,该时间段内甲、乙、丙可能均达到平衡 |
| B.700℃下,甲对应的活化能最大 |
| C.一般催化剂既能降低活化能,又能降低过渡态的能量 |
| D.其它条件一定时,随着温度升高,单位体积内活化分子数占比增大 |
Ⅲ.利用CO2制备甲醇
一定条件下,向恒容密闭容器中通入一定量的CO2和H2.涉及反应如下:
主反应:CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ΔH = −90.4 kJ/mol
CH3OH(g) + H2O(g) ΔH = −90.4 kJ/mol副反应:CO2(g) + H2(g)
 CO(g) + H2O(g) ΔH = +40.5 kJ/mol
CO(g) + H2O(g) ΔH = +40.5 kJ/mol(7)其他条件相同,不同压强下,平衡时CO2转化率随温度的变化关系如图所示。

①压强P1
②图中温度高于T1时,两条曲线重叠的原因是:
(8)实际工业生产中,需要在260℃、压强恒为4.0 MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04 mol/min、n(CO2):n(H2) = 1:3,持续通入原料,同时控制出气流量。
①为了维持体系压强恒定,需控制出气流量小于进气流量,原因为:
②已知出气流量为0.03 mol/min,单位时间CO2的转化率为60 %,则流出气体中CO的百分含量为
您最近一年使用:0次
【推荐3】氮、碳氧化物的排放会对环境造成污染。多年来化学工作者对氮、碳的氧化物做了广泛深入的研究并取得一些重要成果。
I.已知2NO(g)+O2(g)⇌2NO2(g)的反应历程分两步:
第一步:2NO(g)⇌N2O2(g)(快) ∆H1<0;v1正=k1正c2(NO); v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g)⇌2NO2(g)(慢 )∆H2<0;v2正=k2正c(N2O2)c(O2); v2逆=k2逆c2(NO2)
①在两步的反应中,哪一步反应的活化能更大______ (填“第一步”或“第二步”)。
②一定温度下,反应2NO(g)+O2(g)⇌2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=_______ ;
II.(1)利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中部分反应的热化方程式为:
①CH4(g)=C(s)+2H2(g) ΔH1>0
②CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2>0
③CO(g)+H2(g)=C(s)+H2O(g) ΔH3<0
则反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH=_________ (用含ΔH1、ΔH2、ΔH3的代数式表示)
(2)在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g)+CH4(g)⇌2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图所示。

y点:v(正)_____ v(逆)(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,求x点对应温度下反应的平衡常数Kp=____ 。
III.设计如图装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中电解制备过程的总反应化学方程式为________ 。

I.已知2NO(g)+O2(g)⇌2NO2(g)的反应历程分两步:
第一步:2NO(g)⇌N2O2(g)(快) ∆H1<0;v1正=k1正c2(NO); v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g)⇌2NO2(g)(慢 )∆H2<0;v2正=k2正c(N2O2)c(O2); v2逆=k2逆c2(NO2)
①在两步的反应中,哪一步反应的活化能更大
②一定温度下,反应2NO(g)+O2(g)⇌2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
II.(1)利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中部分反应的热化方程式为:
①CH4(g)=C(s)+2H2(g) ΔH1>0
②CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2>0
③CO(g)+H2(g)=C(s)+H2O(g) ΔH3<0
则反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH=
(2)在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g)+CH4(g)⇌2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图所示。

y点:v(正)
III.设计如图装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中电解制备过程的总反应化学方程式为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】在双碳目标驱动下,大批量氢燃料客车在2022年北京冬奥会上投入使用。氢源的获取和利用成为科学研究热点。回答下列问题:
Ⅰ.氢源的获取:电解液氨制氢
氨分子中具有较高的含氢量,因此是制氢的优选原料。现以液氨为原料,使用 非水电解质电解制氢。(已知:电解过程中电解液内含氮微粒只有
非水电解质电解制氢。(已知:电解过程中电解液内含氮微粒只有 、
、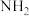 和
和 )
)
(1)产生 的电极反应式为
的电极反应式为______ 。
Ⅱ.氢源的利用: 还原
还原 制甲醇
制甲醇
(2)800℃时, 还原
还原 反应的热化学方程式及其平衡常数如下:
反应的热化学方程式及其平衡常数如下:
反应1:
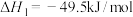

反应2: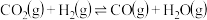

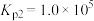
反应3: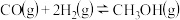

______ 
(3)800℃时,正反应进行的程度“反应2”______ “反应1”(选填“>”或“<”),判断依据是______ 。
(4)反应1在一定条件下建立平衡,关于反应1的相关描述正确的是______。
(5)某温度下,向2L恒容密闭容器中充入0.5mol 和0.9mol
和0.9mol 发生反应1和反应2,经过5min达到平衡状态,反应过程中
发生反应1和反应2,经过5min达到平衡状态,反应过程中 和
和 的物质的量随时间变化情况如下图所示:
的物质的量随时间变化情况如下图所示:
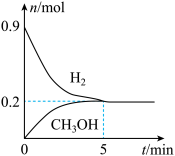
平衡时, 的转化率为
的转化率为______ ,该温度下,反应2的化学平衡常数
______ 。
(6) 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:______ 。
Ⅰ.氢源的获取:电解液氨制氢
氨分子中具有较高的含氢量,因此是制氢的优选原料。现以液氨为原料,使用
 非水电解质电解制氢。(已知:电解过程中电解液内含氮微粒只有
非水电解质电解制氢。(已知:电解过程中电解液内含氮微粒只有 、
、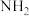 和
和 )
)(1)产生
 的电极反应式为
的电极反应式为Ⅱ.氢源的利用:
 还原
还原 制甲醇
制甲醇(2)800℃时,
 还原
还原 反应的热化学方程式及其平衡常数如下:
反应的热化学方程式及其平衡常数如下:反应1:

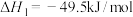

反应2:
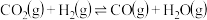

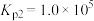
反应3:
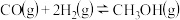


(3)800℃时,正反应进行的程度“反应2”
(4)反应1在一定条件下建立平衡,关于反应1的相关描述正确的是______。
| A.使用高效催化剂可降低反应的活化能,增大活化分子百分数,加快化学反应速率 |
| B.该反应的反应物总能量小于生成物总能量 |
| C.容器内气体的平均相对分子质量不再改变说明反应达到了平衡 |
D.增大压强,反应1的化学平衡常数 变小 变小 |
 和0.9mol
和0.9mol 发生反应1和反应2,经过5min达到平衡状态,反应过程中
发生反应1和反应2,经过5min达到平衡状态,反应过程中 和
和 的物质的量随时间变化情况如下图所示:
的物质的量随时间变化情况如下图所示:
平衡时,
 的转化率为
的转化率为
(6)
 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体在中性和碱性溶液中不能稳定存在。
回答下列问题:
(1)用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的_________ (填化学式),至沉淀不再产生后。再加入过里的Na2CO3和NaOH,充分反应后将沉淀一并滤去。在无隔膜电解槽中用惰性电极电解一段时间生成NaClO3,阳极反应式为_______
(2)X酸是_________ 。写出二氧化氯发生器中生成ClO2的化学方程式_______ ,吸收塔内的温度不宜过高的原因为________
(3)亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2有毒,经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列分析正确的是(_____ )
A.亚氯酸钠在碱性条件下较稳定
B.25℃时,HClO2的浓度随PH增大而增大
C.PH=6时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 25℃时,该溶液在pH=4时比pH=2时更适合漂白
(4)akg 30%的双氧水理论上可最多制得___ kg NaClO2·3H2O

已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体在中性和碱性溶液中不能稳定存在。
回答下列问题:
(1)用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的
(2)X酸是
(3)亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2有毒,经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列分析正确的是(

A.亚氯酸钠在碱性条件下较稳定
B.25℃时,HClO2的浓度随PH增大而增大
C.PH=6时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 25℃时,该溶液在pH=4时比pH=2时更适合漂白
(4)akg 30%的双氧水理论上可最多制得
您最近一年使用:0次
【推荐3】如今 的综合应用越来越成熟。
的综合应用越来越成熟。
(1) 可氧化
可氧化 脱氢转化为更有工业价值的
脱氢转化为更有工业价值的 。
。
查阅资料,计算 氧化
氧化 脱氢反应的反应热
脱氢反应的反应热
i.查阅______ 的燃烧热数据(填化学式)
ii.查阅水的汽化热:
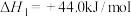
利用上述数据,得如下热化学方程式:
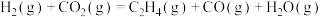
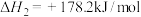
(2) 催化加氢制
催化加氢制 ,能助力“碳达峰”,发生的主要反应有:
,能助力“碳达峰”,发生的主要反应有:
反应Ⅰ

反应Ⅱ

反应Ⅲ

①反应Ⅱ自发进行的条件是______ (填“高温”“低温”或“任意温度”)。
②反应Ⅲ在热力学上趋势大于反应Ⅰ,其原因是______ 。
(3)在5MPa下, 和
和 按物质的量之比1:4进行投料,只发生上述(2)的反应Ⅰ和反应Ⅲ,平衡时
按物质的量之比1:4进行投料,只发生上述(2)的反应Ⅰ和反应Ⅲ,平衡时 和
和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。
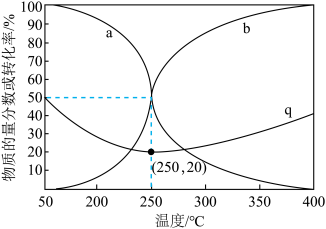
①图中 代表的物质是
代表的物质是______ 。
②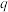 曲线在250℃之后随温度升高而增大的原因是
曲线在250℃之后随温度升高而增大的原因是____________ 。
③250°C时,反应Ⅰ的平衡常数 =
=______ 。
(4)已知25℃时,大气中的 溶于水存在以下过程:
溶于水存在以下过程:
①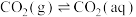

②

过程①的平衡常数 ,其中
,其中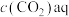 表示溶液中的
表示溶液中的 浓度,
浓度,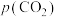 表示大气中
表示大气中 的分压(单位:kPa)。其他条件不变时,温度升高,
的分压(单位:kPa)。其他条件不变时,温度升高,
______ (填“增大”或“减小”);当大气压强为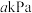 ,溶液中的
,溶液中的 时(忽略
时(忽略 和水的电离),大气中
和水的电离),大气中 的体积分数为
的体积分数为______ %(用含 ,
, 、
、 、
、 的字母表示)。
的字母表示)。
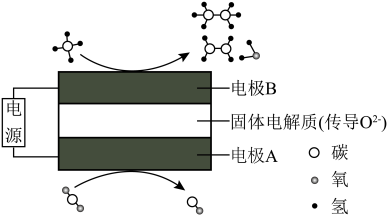
(5)科学家利用电化学装置实现两种分子 和
和 的耦合转化,其原理如图所示:当消耗
的耦合转化,其原理如图所示:当消耗 和
和 的物质的量之比为10:9时,对应的阳极的电极反应式为:
的物质的量之比为10:9时,对应的阳极的电极反应式为:______ 。
 的综合应用越来越成熟。
的综合应用越来越成熟。(1)
 可氧化
可氧化 脱氢转化为更有工业价值的
脱氢转化为更有工业价值的 。
。查阅资料,计算
 氧化
氧化 脱氢反应的反应热
脱氢反应的反应热i.查阅
ii.查阅水的汽化热:

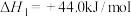
利用上述数据,得如下热化学方程式:
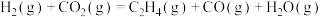
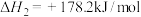
(2)
 催化加氢制
催化加氢制 ,能助力“碳达峰”,发生的主要反应有:
,能助力“碳达峰”,发生的主要反应有:反应Ⅰ


反应Ⅱ


反应Ⅲ


①反应Ⅱ自发进行的条件是
②反应Ⅲ在热力学上趋势大于反应Ⅰ,其原因是
(3)在5MPa下,
 和
和 按物质的量之比1:4进行投料,只发生上述(2)的反应Ⅰ和反应Ⅲ,平衡时
按物质的量之比1:4进行投料,只发生上述(2)的反应Ⅰ和反应Ⅲ,平衡时 和
和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。
①图中
 代表的物质是
代表的物质是②
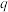 曲线在250℃之后随温度升高而增大的原因是
曲线在250℃之后随温度升高而增大的原因是③250°C时,反应Ⅰ的平衡常数
 =
=(4)已知25℃时,大气中的
 溶于水存在以下过程:
溶于水存在以下过程:①
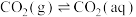

②


过程①的平衡常数
 ,其中
,其中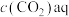 表示溶液中的
表示溶液中的 浓度,
浓度,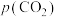 表示大气中
表示大气中 的分压(单位:kPa)。其他条件不变时,温度升高,
的分压(单位:kPa)。其他条件不变时,温度升高,
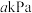 ,溶液中的
,溶液中的 时(忽略
时(忽略 和水的电离),大气中
和水的电离),大气中 的体积分数为
的体积分数为 ,
, 、
、 、
、 的字母表示)。
的字母表示)。(5)科学家利用电化学装置实现两种分子
 和
和 的耦合转化,其原理如图所示:当消耗
的耦合转化,其原理如图所示:当消耗 和
和 的物质的量之比为10:9时,对应的阳极的电极反应式为:
的物质的量之比为10:9时,对应的阳极的电极反应式为:
您最近一年使用:0次



