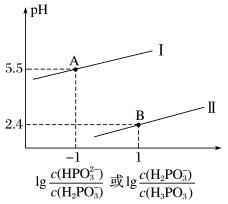
已知亚磷酸(H3PO3)是二元弱酸,常温下,向某浓度的亚磷酸溶液中逐滴加入一定浓度的NaOH溶液,混合溶液的pH与离子浓度的关系如图所示,下列说法正确的是

A.NaOH与H3PO3等物质的量混合时,溶液中存在下列粒子且粒子浓度关系为:c(Na+)+c(H+)=2c(HPO )+c(H2PO )+c(H2PO )+3c(PO )+3c(PO )+c(OH-) )+c(OH-) |
B.曲线II表示的是pH与lg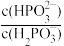 的变化关系图,Ka2=10-1.4 的变化关系图,Ka2=10-1.4 |
C.NaH2PO3溶液中:c(HPO )>c(H3PO3) )>c(H3PO3) |
D.当混合溶液呈中性时,c(HPO )<c(H2PO )<c(H2PO ) ) |
2020·湖南岳阳·一模 查看更多[4]
湖南省岳阳市2020届高三教学质量监测(一)化学试题(已下线)【奋进985】05-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)第25讲 盐类水解(讲)-2023年高考化学一轮复习讲练测(全国通用)江西省重点校2022-2023学年高三上学期第三次联考化学试题.
更新时间:2022-04-08 09:17:58
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】根据下表提供的数据,下列说法正确的是
| 化学式 |  |  |  |
| 电离常数 |  | 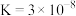 | 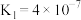  |
A.向 溶液中通入少量 溶液中通入少量 发生反应: 发生反应: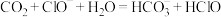 |
B.等浓度的 和 和 的混合溶液中离子浓度有如下关系:c(Na+)>c( 的混合溶液中离子浓度有如下关系:c(Na+)>c(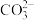 )>c(ClO-)>c(OH-) )>c(ClO-)>c(OH-) |
C.等浓度的 溶液和 溶液和 溶液中,水电离的 溶液中,水电离的 前者小于后者 前者小于后者 |
D. 相等的溶液中,溶质浓度由大到小的顺序为:Na2CO3>NaClO>NaHCO3>CH3COONa 相等的溶液中,溶质浓度由大到小的顺序为:Na2CO3>NaClO>NaHCO3>CH3COONa |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】室温下,通过下列实验探究 溶液的性质。
溶液的性质。
实验Ⅰ:向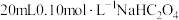 溶液中滴加
溶液中滴加 溶液。
溶液。
实验Ⅱ:向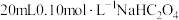 溶液中滴加
溶液中滴加 溶液。
溶液。
已知: 的电离常数
的电离常数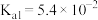 ,
,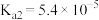 ,
,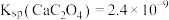 ,溶液混合后体积变化忽略不计。下列说法正确的是
,溶液混合后体积变化忽略不计。下列说法正确的是
 溶液的性质。
溶液的性质。实验Ⅰ:向
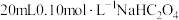 溶液中滴加
溶液中滴加 溶液。
溶液。实验Ⅱ:向
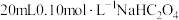 溶液中滴加
溶液中滴加 溶液。
溶液。已知:
 的电离常数
的电离常数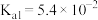 ,
,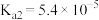 ,
,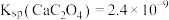 ,溶液混合后体积变化忽略不计。下列说法正确的是
,溶液混合后体积变化忽略不计。下列说法正确的是| A.实验Ⅰ滴定达终点读数时,应双手一上一下持滴定管保证其竖直 |
B.实验Ⅰ滴定至溶液中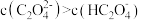 时, 时,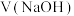 至少大于10mL 至少大于10mL |
C.实验Ⅱ初始阶段发生反应的离子方程式为 |
D.实验Ⅱ最后阶段发生反应(最简整数比)的化学平衡常数表达式为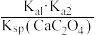 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列溶液中有关物质的量浓度关系正确的是
| A.0.1 mol.L-1 的 NaHA 溶液 pH=l 则有:c(Na+)= c(H2A) + c(HA-) + c(A2-) |
| B.强酸HA溶液与弱碱MOH溶液混合后溶液呈中性,则有:c(M+)= c(A-) |
| C.pH相等的CH3COONa 和Na2CO3 两种溶液:c(CH3COONa)<c(Na2CO3) |
| D.NaHSO3 溶液呈酸性,则有:c(Na+)>c(HSO3-)>c(SO32-) >c(H+)> c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列说法正确的是
| A.常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(B—)>c(H+)>c(Na+)>c(OH—) |
| B.同浓度同体积的NaClO溶液和CH3COONa溶液,离子总数前者小于后者 |
| C.在1mol/LCH3COOH溶液中加入少量冰醋酸,醋酸电离平衡正向移动且电离程度增大 |
D.常温下,c( )相等的①NH3·H2O②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ )相等的①NH3·H2O②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,用NaOH调节不同浓度的二元弱酸( H2A)的酸性,在其pH均为3时,各溶液中pHA-与pH2A或pA2-的关系如图所示[pX=-lgc(X)]。下列说法正确的是


| A.Ka1(H2A)/Ka2(H2A)=104 |
| B.0.1 mol·L-1的NaHA溶液中:c(HA-)>c(H2A)>c(A2-) |
| C.Q点时,c(Na+)>2c(A2-) |
| D.向R点溶液中加入NaOH固体可以达到Q点 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】室温下,一种以 溶液、
溶液、 溶液和氨水为原料制取
溶液和氨水为原料制取 的流程如下图所示:已知室温时
的流程如下图所示:已知室温时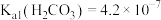 、
、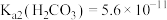 、
、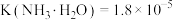 。忽略溶液混合时体积变化。下列说法正确的是
。忽略溶液混合时体积变化。下列说法正确的是

 溶液、
溶液、 溶液和氨水为原料制取
溶液和氨水为原料制取 的流程如下图所示:已知室温时
的流程如下图所示:已知室温时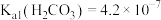 、
、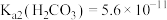 、
、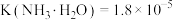 。忽略溶液混合时体积变化。下列说法正确的是
。忽略溶液混合时体积变化。下列说法正确的是
A.10mL 0.1  与0.1 与0.1 氨水的混合溶液中存在: 氨水的混合溶液中存在: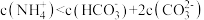 |
B.反应的离子方程式为 |
C.过滤所得滤液中存在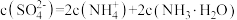 |
D.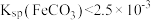 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
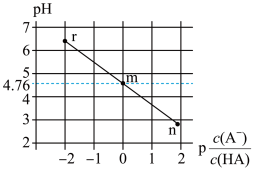
【推荐2】常温下,将NaOH溶液滴加到HA溶液中,测得混合溶液的pH与p 转化关系如图所示[已知:p
转化关系如图所示[已知:p =-lg
=-lg ]。下列叙述错误的是( )
]。下列叙述错误的是( )
 转化关系如图所示[已知:p
转化关系如图所示[已知:p =-lg
=-lg ]。下列叙述错误的是( )
]。下列叙述错误的是( )
| A.m点:c(A-)=c(HA) |
| B.Ka(HA)的数量级为10-6 |
| C.水的电离程度:m<r |
| D.r点:c(H+)+c(Na+)=c(A-)+c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
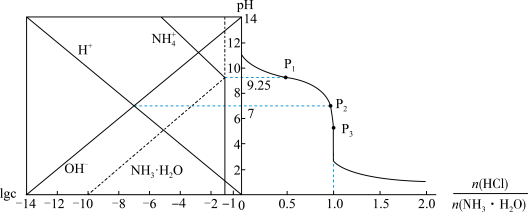
【推荐1】25 °C时,将HCl气体缓慢通入0.10 mol·L-1的氨水中,溶液的pH、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 的关系如图所示。若忽略溶液体积变化,下列有关说法错误的是
的关系如图所示。若忽略溶液体积变化,下列有关说法错误的是
 的关系如图所示。若忽略溶液体积变化,下列有关说法错误的是
的关系如图所示。若忽略溶液体积变化,下列有关说法错误的是
| A.25 ° C时, NH3·H2O的电离平衡常数为10-4.75 |
| B.P1所示溶液:c(Cl-) < 0.05 mol·L-1 |
C.P2所示溶液:c( )= 100c( NH3·H2O ) )= 100c( NH3·H2O ) |
D.P3所示溶液:c(Cl- )>c( ) >c(H+)>c(OH-) ) >c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
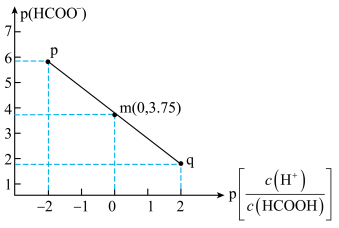
【推荐2】25℃下,将KOH溶液滴加到甲酸溶液中,测得混合溶液中的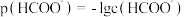 与
与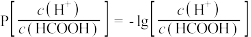 的变化关系如图所示。下列叙述错误的是
的变化关系如图所示。下列叙述错误的是
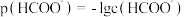 与
与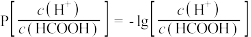 的变化关系如图所示。下列叙述错误的是
的变化关系如图所示。下列叙述错误的是
| A.25℃时 Ka(HCOOH)=10-3.75 |
B.滴加KOH溶液过程中, 始终不变 始终不变 |
| C.溶液中K+浓度:c(q)<c(p) |
D.m点所示溶液中 |
您最近一年使用:0次

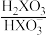 和
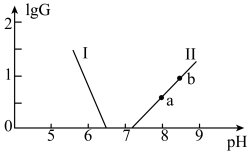
和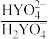 缓冲对。常温下,该水溶液中各缓冲对微粒浓度之比的对数值lgG[G表示
缓冲对。常温下,该水溶液中各缓冲对微粒浓度之比的对数值lgG[G表示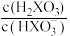 或
或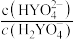 与溶液pH的变化关系如图所示(已知:常温下,H3YO4的电离平衡常数为
与溶液pH的变化关系如图所示(已知:常温下,H3YO4的电离平衡常数为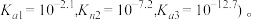
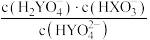 逐渐增大
逐渐增大 时,
时,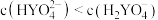
 溶液中加入
溶液中加入 固体,
固体, 、
、 、
、 、
、 等粒子浓度变化情况如图所示(忽略溶液体积、温度的变化及
等粒子浓度变化情况如图所示(忽略溶液体积、温度的变化及
 ,
,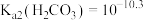 ;
; ,下列说法错误的是
,下列说法错误的是 溶液中存在:
溶液中存在:
 时,
时,
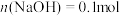 时,
时,