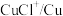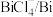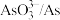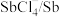臭氧( )在
)在 催化下可以将烟气中的
催化下可以将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可以在其他条件下被还原为
也可以在其他条件下被还原为 。回答下列问题:
。回答下列问题:
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为_______ ,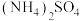 的晶体类型为
的晶体类型为_______ 晶体。
(2) 基态核外电子排布式为
基态核外电子排布式为_______ 。
(3)N、H、O三种元素的电负性由小到大的顺序为_______ 。
(4) 的沸点高于
的沸点高于 ,这是因为
,这是因为_______ 。
(5) 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为_______ 。
 )在
)在 催化下可以将烟气中的
催化下可以将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可以在其他条件下被还原为
也可以在其他条件下被还原为 。回答下列问题:
。回答下列问题:(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为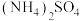 的晶体类型为
的晶体类型为(2)
 基态核外电子排布式为
基态核外电子排布式为(3)N、H、O三种元素的电负性由小到大的顺序为
(4)
 的沸点高于
的沸点高于 ,这是因为
,这是因为(5)
 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为
更新时间:2022-07-23 21:42:33
|
相似题推荐
【推荐1】碲(Te)是一种重要的稀有分散元素,广泛应用于冶金、石油、化工、航空、电子等领域。以某冶炼厂的湿阳极泥(含水26%,主要含锑、砷、铅、铋、银和少量铜、碲等)为原料回收碲的流程如下:
请回答下列问题:
(1)52Te的基态原子的电子排布式为___________ 。
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是_______________ ;氧化后的原料还需粉碎、过筛,目的是_________________ 。
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为___________ 、___________ ;添加 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式________________ 。
(4)电解时为防止除Te以外的单质生成,需控制电位的范围为___________ ;加入饱和Na2SO3溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成_____________ (填化学式)。
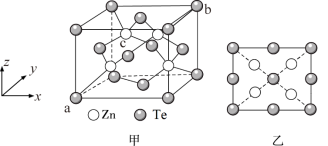
(5)将碲与锌一起加热,然后升华可制得碲化锌。碲化锌是一种重要的半导体材料,图甲为它的一种立方晶胞结构,图乙为该晶胞沿z轴投影图。已知a点的坐标为(0,0,0),b点的坐标为(1,1,1),则c点的坐标为_______________ ,设ZnTe的摩尔质量为M,阿伏加德罗常数的值为NA,密度为dg/cm3,则Zn与Te最近距离为___________ nm(列出计算式即可)。
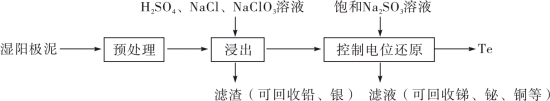
物质 |
|
|
|
|
|
氧化还原电位(E)/V | 0.342 | 0.568 | 0.16 | 小于0.16 | 小于0.16 |
(1)52Te的基态原子的电子排布式为
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为
 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式(4)电解时为防止除Te以外的单质生成,需控制电位的范围为
 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成(5)将碲与锌一起加热,然后升华可制得碲化锌。碲化锌是一种重要的半导体材料,图甲为它的一种立方晶胞结构,图乙为该晶胞沿z轴投影图。已知a点的坐标为(0,0,0),b点的坐标为(1,1,1),则c点的坐标为
您最近一年使用:0次
【推荐2】一种高硫锰矿的主要成分为 ,主要杂质为
,主要杂质为 ,还含有少量
,还含有少量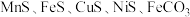 等,其中
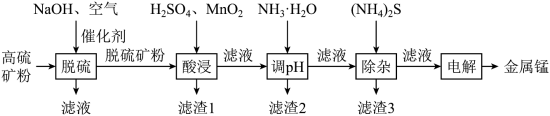
等,其中 含量较大。研究人员设计了如下流程,制得了金属锰。
含量较大。研究人员设计了如下流程,制得了金属锰。
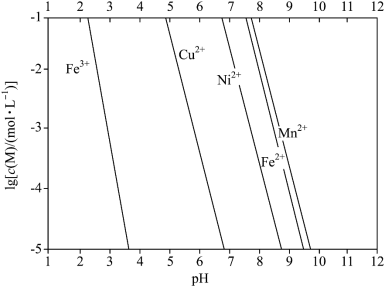
已知:①金属离子的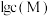 与溶液
与溶液 的关系如下图所示。
的关系如下图所示。
②金属硫化物的溶度积常数如下表。
回答下列问题。
(1)碱性溶液中,在催化剂存在下通空气氧化脱硫,硫化物中的硫元素被氧化为单质。写出硫化亚铁发生反应的化学方程式___________ 。
(2)根据矿物组成,脱硫时能被 部分溶解的物质是
部分溶解的物质是___________ 。若未经脱硫直接酸浸,会产生的污染物是___________ 。
(3)酸浸时,加入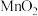 的作用是
的作用是___________ (用离子方程式表示)。
(4)调溶液 到5左右,滤渣2的主要成分是
到5左右,滤渣2的主要成分是___________ ;加入适量的 除去的主要离子是
除去的主要离子是___________ 。
(5)除杂后的 溶液通过电解制得金属锰,惰性阳极发生的电极反应为
溶液通过电解制得金属锰,惰性阳极发生的电极反应为___________ 。
(6)请写出基态Mn原子的价层电子排布式___________ ;锰的化合物 是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为a pm,则晶体密度为
是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为a pm,则晶体密度为___________  。
。

 ,主要杂质为
,主要杂质为 ,还含有少量
,还含有少量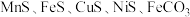 等,其中
等,其中 含量较大。研究人员设计了如下流程,制得了金属锰。
含量较大。研究人员设计了如下流程,制得了金属锰。
已知:①金属离子的
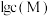 与溶液
与溶液 的关系如下图所示。
的关系如下图所示。
②金属硫化物的溶度积常数如下表。
| 金属硫化物 |  |  |  |  |
 |  | 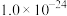 |  |  |
(1)碱性溶液中,在催化剂存在下通空气氧化脱硫,硫化物中的硫元素被氧化为单质。写出硫化亚铁发生反应的化学方程式
(2)根据矿物组成,脱硫时能被
 部分溶解的物质是
部分溶解的物质是(3)酸浸时,加入
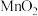 的作用是
的作用是(4)调溶液
 到5左右,滤渣2的主要成分是
到5左右,滤渣2的主要成分是 除去的主要离子是
除去的主要离子是(5)除杂后的
 溶液通过电解制得金属锰,惰性阳极发生的电极反应为
溶液通过电解制得金属锰,惰性阳极发生的电极反应为(6)请写出基态Mn原子的价层电子排布式
 是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为a pm,则晶体密度为
是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为a pm,则晶体密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)K2Cr2O7 是一种强氧化剂,在酸性条件下与乙醇发生如下反应:3CH3CH2OH+2K2Cr2O7+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
①Cr 基态核外电子排布式为:___________ 。
②K、S、O 三种元素第一电离能由大到小的顺序为___________ 。
③乙醇的沸点比甲醚(CH3OCH3)的高,主要原因是:___________ 。
(2)NH3BH3 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。在该分子中,与 N原子相连的H 呈正电性(Hδ+),与 B 原子相连的H 呈负电性(Hδ-)。
①H、B、N、O 四种元素电负性由大到小的顺序是___________ 。
②基态硼原子中,核外存在___________ 对自旋相反的电子,电子占据的最高能级的电子云轮廓图为___________ 形。
(1)K2Cr2O7 是一种强氧化剂,在酸性条件下与乙醇发生如下反应:3CH3CH2OH+2K2Cr2O7+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
①Cr 基态核外电子排布式为:
②K、S、O 三种元素第一电离能由大到小的顺序为
③乙醇的沸点比甲醚(CH3OCH3)的高,主要原因是:
(2)NH3BH3 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。在该分子中,与 N原子相连的H 呈正电性(Hδ+),与 B 原子相连的H 呈负电性(Hδ-)。
①H、B、N、O 四种元素电负性由大到小的顺序是
②基态硼原子中,核外存在
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】锌及其化合物在工农业生产及科学研究中具有广泛的用途。回答下列问题:
(1)Zn位于元素周期表的___________ 区,基态Zn2+的核外电子排布式为___________ 。
(2)氨基酸锌是研究最早和使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图1是氨基酸锌的结构简式。
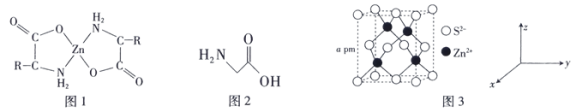
①组成氨基酸锌的C、N、O的电负性由大到小的顺序是___________ 。
②氨基酸锌的Zn2+形成配位键,其中提供空轨道的原子是___________ 。
③最简单的氨基酸是甘氨酸(结构简式如图2),其结构中π键与σ键的数量比为___________ 。
(3)ZnS可用于制白色颜料、玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS的晶胞如图3所示。
①上图中 的坐标有
的坐标有 、
、 ,与
,与 距离最近的
距离最近的 还有
还有___________ (填坐标)。
②Zn2+占据___________ (填“八面体”或“四面体”)空隙,空隙利用率为___________ %。
③ZnS的密度为___________  。
。
(1)Zn位于元素周期表的
(2)氨基酸锌是研究最早和使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图1是氨基酸锌的结构简式。

①组成氨基酸锌的C、N、O的电负性由大到小的顺序是
②氨基酸锌的Zn2+形成配位键,其中提供空轨道的原子是
③最简单的氨基酸是甘氨酸(结构简式如图2),其结构中π键与σ键的数量比为
(3)ZnS可用于制白色颜料、玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS的晶胞如图3所示。
①上图中
 的坐标有
的坐标有 、
、 ,与
,与 距离最近的
距离最近的 还有
还有②Zn2+占据
③ZnS的密度为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铜及其化合物在生产生活中用途广泛。回答下列问题:
(1)目前,低压甲醇铜基催化剂的主要组分是CuO、ZnO和Al2O3,下列氧原子电子排布图表示的状态中,能量最高的是__ (填序号)。
A. B.
B.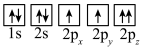
C. D.
D.
(2)铜离子是人体内多种酶的辅因子,某化合物与Cu+结合形成如图所示的离子。
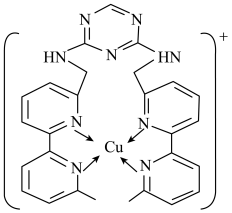
①该离子中含有化学键的类型有___ (填序号)。
A.极性键 B.离子键 C.非极性键 D.配位键
②H、N、Cu三种元素的电负性由大到小的顺序是___ 。H、N、Cu三种元素形成单质其熔点由低到高顺序为___ 。
(3)某磷青铜晶胞结构如图所示:
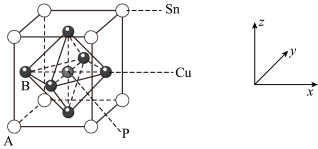
①其中原子坐标参数A为(0,0,0);B为(0, ,
, )。则P原子的坐标参数为
)。则P原子的坐标参数为___ 。
②该晶体中距离Cu原子最近的Sn原子有__ 个,这些Sn原子所呈现的构型为___ 。
(1)目前,低压甲醇铜基催化剂的主要组分是CuO、ZnO和Al2O3,下列氧原子电子排布图表示的状态中,能量最高的是
A.
 B.
B.
C.
 D.
D.
(2)铜离子是人体内多种酶的辅因子,某化合物与Cu+结合形成如图所示的离子。

①该离子中含有化学键的类型有
A.极性键 B.离子键 C.非极性键 D.配位键
②H、N、Cu三种元素的电负性由大到小的顺序是
(3)某磷青铜晶胞结构如图所示:

①其中原子坐标参数A为(0,0,0);B为(0,
 ,
, )。则P原子的坐标参数为
)。则P原子的坐标参数为②该晶体中距离Cu原子最近的Sn原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硅电池、锂离子电池都是现代高性能电池的代表,高性能的电极材料与物质结构密切相关。
(1)LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与PO 的结构密切相关,PO
的结构密切相关,PO 的空间结构为
的空间结构为___ 。P、O、S的电负性从大到小的顺序为___ 。
(2)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸(如图)常被用作碳包覆的碳源,其易溶于水的原因是____ ,抗坏血酸中碳原子的杂化方式为___ 、___ ,1mol抗坏血酸中手性碳原子的数目为____ 。

(3)Li+过度脱出易导致锂电池结构坍塌产生O2而爆炸,实验证实O2因具有单电子而成为顺磁性分子,下列结构式(黑点代表电子)中最有可能代表O2分子结构的是___ 。(填字母)
(1)LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与PO
 的结构密切相关,PO
的结构密切相关,PO 的空间结构为
的空间结构为(2)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸(如图)常被用作碳包覆的碳源,其易溶于水的原因是

(3)Li+过度脱出易导致锂电池结构坍塌产生O2而爆炸,实验证实O2因具有单电子而成为顺磁性分子,下列结构式(黑点代表电子)中最有可能代表O2分子结构的是
A. | B. | C.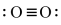 | D.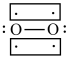 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铝的单质及化合物在工农业生产中有着重要的应用,单质Al可用作火箭和飞机外壳,冰晶石可用于冶炼铝时的助熔剂等。回答下列问题:
(1)Al在元素周期表中的位置为_______ ,有_______ 种不同运动状态的电子。
(2)①Al的卤化物的熔点如下:
表中卤化物熔点差异的原因是_______ 。
②实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。已知Al2Cl6分子中正负电荷中心重合,则Al2Cl6属于_______ 分子(填“极性”或“非极性”),分子中Al采取_______ 杂化。

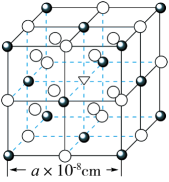
(3)冰晶石(Na3AlF6)是炼铝的助熔剂,已知冰晶石(Na3AlF6)熔融时的电离方程式为Na3AlF6=3Na++ ,现有冰晶石的结构单元如图所示,
,现有冰晶石的结构单元如图所示, 位于大立方体顶点和面心,
位于大立方体顶点和面心, 位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中
位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中 、
、 中的一种。
中的一种。
①Na3AlF6中含有的化学键类型有_______ (填字母)。
A.离子键 B.金属键 C.氢键 D.配位键
②大立方体的体心处▽代表_______ (填离子符号);
③请计算冰晶石晶体的密度_______ 。
(4)三乙基铝是一种金属有机物,可做火箭燃料,其结构简式为 。
。
①三乙基铝中Al的VSEPR模型为_______ 。
②三乙基铝中所含元素的电负性从大到小的顺序为_______ (用元素符号表示)。
(1)Al在元素周期表中的位置为
(2)①Al的卤化物的熔点如下:
 |  |  | |
| 熔点/K | 256.8 | 304 | 413 |
②实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。已知Al2Cl6分子中正负电荷中心重合,则Al2Cl6属于

(3)冰晶石(Na3AlF6)是炼铝的助熔剂,已知冰晶石(Na3AlF6)熔融时的电离方程式为Na3AlF6=3Na++
 ,现有冰晶石的结构单元如图所示,
,现有冰晶石的结构单元如图所示, 位于大立方体顶点和面心,
位于大立方体顶点和面心, 位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中
位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中 、
、 中的一种。
中的一种。
①Na3AlF6中含有的化学键类型有
A.离子键 B.金属键 C.氢键 D.配位键
②大立方体的体心处▽代表
③请计算冰晶石晶体的密度
(4)三乙基铝是一种金属有机物,可做火箭燃料,其结构简式为
 。
。①三乙基铝中Al的VSEPR模型为
②三乙基铝中所含元素的电负性从大到小的顺序为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】 、
、 、
、 、
、 、
、 五种分属于不同主族的短周期元素,原子序数依次增大,
五种分属于不同主族的短周期元素,原子序数依次增大, 的气态氢化物分子中只有一对孤电子对;
的气态氢化物分子中只有一对孤电子对; 的原子半径是短周期中最大的,
的原子半径是短周期中最大的, 的离子半径是第三周期元素形成的简单离子半径中最小的,
的离子半径是第三周期元素形成的简单离子半径中最小的, 的最外层p轨道上有一对成对电子。
的最外层p轨道上有一对成对电子。
(1) 在周期表中的位置是
在周期表中的位置是__________ 。
(2) 、
、 、
、 的电负性大小顺序为
的电负性大小顺序为__________ (用元素符号表示);
(3) 的最高正价氧化物的分子构型为
的最高正价氧化物的分子构型为____ :将该氧化物溶于水,则所得溶液的阴离子中的 杂化轨道类型为
杂化轨道类型为____ 。
(4)将 的单质与
的单质与 的最高价氧化物对应的水化物混合,其反应的离子方程式为:
的最高价氧化物对应的水化物混合,其反应的离子方程式为:__________ ;
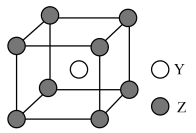
(5)如图所示为 、
、 形成的合金晶胞结构,如果将含
形成的合金晶胞结构,如果将含 的该合金置于足量的水中充分反应,放出标准状况下气体的体积为
的该合金置于足量的水中充分反应,放出标准状况下气体的体积为__________  。
。
 、
、 、
、 、
、 、
、 五种分属于不同主族的短周期元素,原子序数依次增大,
五种分属于不同主族的短周期元素,原子序数依次增大, 的气态氢化物分子中只有一对孤电子对;
的气态氢化物分子中只有一对孤电子对; 的原子半径是短周期中最大的,
的原子半径是短周期中最大的, 的离子半径是第三周期元素形成的简单离子半径中最小的,
的离子半径是第三周期元素形成的简单离子半径中最小的, 的最外层p轨道上有一对成对电子。
的最外层p轨道上有一对成对电子。(1)
 在周期表中的位置是
在周期表中的位置是(2)
 、
、 、
、 的电负性大小顺序为
的电负性大小顺序为(3)
 的最高正价氧化物的分子构型为
的最高正价氧化物的分子构型为 杂化轨道类型为
杂化轨道类型为(4)将
 的单质与
的单质与 的最高价氧化物对应的水化物混合,其反应的离子方程式为:
的最高价氧化物对应的水化物混合,其反应的离子方程式为:(5)如图所示为
 、
、 形成的合金晶胞结构,如果将含
形成的合金晶胞结构,如果将含 的该合金置于足量的水中充分反应,放出标准状况下气体的体积为
的该合金置于足量的水中充分反应,放出标准状况下气体的体积为 。
。
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为___________ ;第一电离能I1(Si)___________ I1(Ge)(填“>”或“<”)。
(2)基态Ge原子价电子排布式为___________ ;SiO2、GeO2具有类似的晶体结构,SiO2熔点较高,其原因是___________
(3)如图为硼酸晶体的片层结构,其中硼原子的杂化方式为___________ 。该晶体中存在的作用力有___________ 。
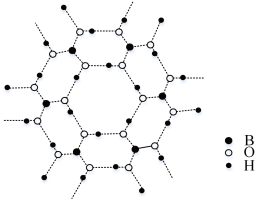
A.共价键B.离子键C.氢键
(4)Fe和Cu可分别与氧元素形成低价态氧化物FeO和Cu2O。
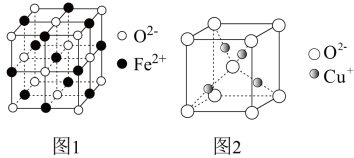
①FeO立方晶胞结构如图1所示,则Fe2+的配位数为___________ 。
②Cu2O立方晶胞结构如图2所示,若晶胞边长为acm,则该晶体的密度为___________ g·cm-3。(用含a、NA的代数式表示,NA代表阿伏加 德罗常数)
(1)C、O、Si三种元素电负性由大到小的顺序为
(2)基态Ge原子价电子排布式为
(3)如图为硼酸晶体的片层结构,其中硼原子的杂化方式为

A.共价键B.离子键C.氢键
(4)Fe和Cu可分别与氧元素形成低价态氧化物FeO和Cu2O。

①FeO立方晶胞结构如图1所示,则Fe2+的配位数为
②Cu2O立方晶胞结构如图2所示,若晶胞边长为acm,则该晶体的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F、G为六种短周期元素,且原子序数依次增大。A与B、C、D均能形成10电子化合物,C的气态氢化物能使紫色石蕊溶液变蓝,A、D能形成两种液态化合物A2D和A2D2,E是短周期中原子半径最大的原子,F元素的周期序数与主族序数相等,A、G和C、E的原子序数之和相等。
(1)D与E组成的某种化合物呈淡黄色,写出其电子式___________ ,所含的化学键类型为___________ 。1.5mol该黄色固体与足量CO2反应时的电子转移数目为___________ 。
(2)比较B和C的简单气态氢化物的沸点大小___________ 。(用化学式表示)
(3)写出F单质与NaOH溶液反应的化学方程式___________ 。
(4)在一定条件下,E元素的单质能与A元素的单质化合生成EA,EA能与水反应放氢气,则其化学方程式为___________ 。
(5)CD2是常见的大气污染物,工业生产中可用NaOH溶液吸收,消除其污染,写出相关化学方程式___________ 。
(1)D与E组成的某种化合物呈淡黄色,写出其电子式
(2)比较B和C的简单气态氢化物的沸点大小
(3)写出F单质与NaOH溶液反应的化学方程式
(4)在一定条件下,E元素的单质能与A元素的单质化合生成EA,EA能与水反应放氢气,则其化学方程式为
(5)CD2是常见的大气污染物,工业生产中可用NaOH溶液吸收,消除其污染,写出相关化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】合成氨工业中,原料气(N2、 H2 及少量CO,NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气中的CO,其反应( Ac-代表CH3COO-)为[Cu(NH3)2 ]Ac+CO+ NH3 = [Cu(NH3)3 CO]Ac [醋酸羰基三氨合铜(I) ]。
(1)基态铜原子的电子排布式为_______ 。
(2)配合物Cu(NH3)2]Ac所含元素中,电负性最小的是_______ (填元素符号,下同);基态原子的第一电离能最大的是_______ 。
(3)[Cu(NH3)3CO]+的中心原子的配位数为_______ 。
(4)在一定条件下NH3与CO2能合成尿素Co(NH2)2 ],尿素中C原子和N原子的轨道杂化类型分别为_______ 、 _______ ;1 mol尿素分子中,σ键的数目为_______ NA。
(5)N、P、As属于同族元素,它们的最简单氢化物的沸点由大到小的顺序为_______ (用化学式表示),其原因是_______ 。
(6)铜的化合物种类很多,其中氯化亚铜的晶胞结构如图所示。
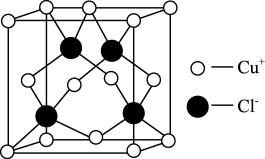
①晶胞内的4个Cl-相互连接所形成的立体构型是_______ 。
②已知晶胞的棱长为a nm,阿伏加德罗常数的值为NA,则氯化亚铜的密度ρ=_______ ( 填计算式即可)g·cm-3。
(1)基态铜原子的电子排布式为
(2)配合物Cu(NH3)2]Ac所含元素中,电负性最小的是
(3)[Cu(NH3)3CO]+的中心原子的配位数为
(4)在一定条件下NH3与CO2能合成尿素Co(NH2)2 ],尿素中C原子和N原子的轨道杂化类型分别为
(5)N、P、As属于同族元素,它们的最简单氢化物的沸点由大到小的顺序为
(6)铜的化合物种类很多,其中氯化亚铜的晶胞结构如图所示。

①晶胞内的4个Cl-相互连接所形成的立体构型是
②已知晶胞的棱长为a nm,阿伏加德罗常数的值为NA,则氯化亚铜的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】(NH4)2Fe(SO4)2是分析化学中的重要试剂,受热时分解,产物中含有铁氧化物、SO2,SO3,NH3和水蒸气等。回答下列问题:
(1)Fe2+的电子排布式为______ 。
(2)H,N,O、S的电负性由小到大的顺序是______ 。N、O、S的第一电离能由小到大的顺序是______ 。
(3)H2O2与H2S的相对分子质量相同,但常温下H2O2为液体,H2S为气体,原因是______ 。(NH4)2Fe(SO4)2受热分解时的气态产物中,属于非极性分子的是______ 。
(4)N的一种化合物N2O与CO2互为等电子体,二者结构相似,N2O分子中O只与一个N相连,N2O分子中 键和
键和 键数目之比是
键数目之比是______ 。
(5)(NH4)2Fe(SO4)2溶液中存在多种离子,其中空间结构为正四面体的有______ ;其溶液中存在H3O+离子,该离子中H—O—H的键角______ (填“>”“=”或“<”)单个H2O分子中H—O—H的键角。
(1)Fe2+的电子排布式为
(2)H,N,O、S的电负性由小到大的顺序是
(3)H2O2与H2S的相对分子质量相同,但常温下H2O2为液体,H2S为气体,原因是
(4)N的一种化合物N2O与CO2互为等电子体,二者结构相似,N2O分子中O只与一个N相连,N2O分子中
 键和
键和 键数目之比是
键数目之比是(5)(NH4)2Fe(SO4)2溶液中存在多种离子,其中空间结构为正四面体的有
您最近一年使用:0次