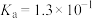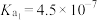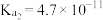已知25 ℃时0.1 mol·L-1醋酸溶液的pH约为3,向其中加入醋酸钠晶体,等晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,增大了c(OH-),因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大。
(1)上述两种解释中________ (填“甲”或“乙”)正确。
(2)为了验证上述哪种解释正确,继续做如下实验:向0.1 mol·L-1的醋酸溶液中加入少量下列物质中的________ (填写编号字母),然后测定溶液的pH。
(3)若________ (填“甲”或“乙”)的解释正确,溶液的pH应________ (填“增大”、“减小”或“不变”)(已知25 ℃ 时,CH3COONH4溶液呈中性)。
(4)常温下将0.010 mol CH3COONa和0.004 mol HCl溶于水,配制成0.5 L混合溶液。判断:
①溶液中共有________ 种粒子。
②溶液中有两种粒子的物质的量的和一定等于0.010 mol,它们是________ 和________ 。
③溶液中n(CH3COO-)+n(OH-)-n(H+)=________ mol。
(1)上述两种解释中
(2)为了验证上述哪种解释正确,继续做如下实验:向0.1 mol·L-1的醋酸溶液中加入少量下列物质中的
| A.固体CH3COOK | B.固体CH3COONH4 |
| C.气体NH3 | D.固体NaHCO3 |
(3)若
(4)常温下将0.010 mol CH3COONa和0.004 mol HCl溶于水,配制成0.5 L混合溶液。判断:
①溶液中共有
②溶液中有两种粒子的物质的量的和一定等于0.010 mol,它们是
③溶液中n(CH3COO-)+n(OH-)-n(H+)=
12-13高二·全国·课时练习 查看更多[3]
福建省莆田第十五中学2018-2019学年高二下学期期中测试化学试题江苏省南京师大苏州实验学校2019-2020学年高二9月月考化学试题(已下线)2012年鲁科版高中化学选修6 2.2认识发生在盐溶液中的化学反应练习卷
更新时间:2016-12-09 04:24:32
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】在一个体积为2L的真空密闭容器中加入0.5molCaCO3,发生反应CaCO3(s) CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
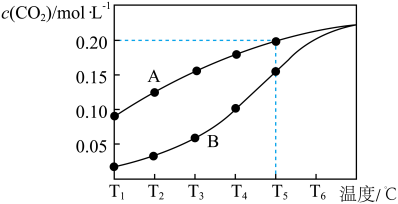
(1)该反应正反应为___ (填“吸”或“放”)热反应,温度为T5℃时,该反应耗时40s达到平衡,则T5℃时,该反应的平衡常数数值为___ 。
(2)如果该反应的平衡常数K值变大,该反应___ (选填编号)。
a.一定向逆反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向正反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)请说明随温度的升高,曲线B向曲线A逼近的原因:___ 。
(4)在T5℃下,维持温度和容器体积不变,向上述平衡体系中再充入0.5molN2,则最后平衡时容器中的CaCO3的质量为___ g。
(5)已知苯酚和碳酸的电离平衡常数如图所示。请写出二氧化碳通入苯酚钠溶液的化学反应离子方程式___ ,请用电离平衡原理解释上述反应发生的原因以及确定生成物的依据___ 。
 CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
(1)该反应正反应为
(2)如果该反应的平衡常数K值变大,该反应
a.一定向逆反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向正反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)请说明随温度的升高,曲线B向曲线A逼近的原因:
(4)在T5℃下,维持温度和容器体积不变,向上述平衡体系中再充入0.5molN2,则最后平衡时容器中的CaCO3的质量为
(5)已知苯酚和碳酸的电离平衡常数如图所示。请写出二氧化碳通入苯酚钠溶液的化学反应离子方程式
| 物质 | 电离平衡常数(25℃) |
| C6H5OH | Ki=1.28×10-10 |
| H2CO3 | Ki1=4.3×10-7 |
| Ki2=5.6×10-11 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol·L-1的醋酸溶液,用0.2 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250 mL 0.2 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、___ 和____ 。
(2)为标定某醋酸溶液的准确浓度,用0.200 0 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
则该醋酸溶液的准确浓度为________ 。(保留小数点后四位)
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸溶液的pH,结果如下:
回答下列问题:
(1)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是_________
(2)从表中的数据,还可以得出另一结论:随着醋酸溶液浓度的减小,醋酸的电离程度________ (填“增大”“减小”或“不变”)。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol·L-1的醋酸溶液,用0.2 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250 mL 0.2 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、
(2)为标定某醋酸溶液的准确浓度,用0.200 0 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸溶液的pH,结果如下:
| 醋酸溶液浓度(mol·L-1) | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
(1)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是
(2)从表中的数据,还可以得出另一结论:随着醋酸溶液浓度的减小,醋酸的电离程度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如下图所示,请回答:
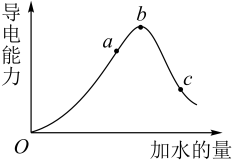
(1)写出醋酸的电离方程式___________________________________________ 。
(2)a、b、c三点溶液中氢离子浓度由小到大的顺序为__________________ 。
(3)a、b、c三点中醋酸的电离程度最大的是_________ 。
(4)取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲_____ 10C(H+)乙(填“大于”、“小于”或 “等于”)

(1)写出醋酸的电离方程式
(2)a、b、c三点溶液中氢离子浓度由小到大的顺序为
(3)a、b、c三点中醋酸的电离程度最大的是
(4)取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
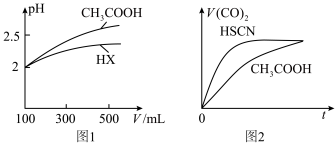
【推荐1】已知25℃时,部分弱酸的电离平衡常数如下表:
(1)25℃时,在 的
的 溶液中由水电离出来的
溶液中由水电离出来的
__________ .
(2) 溶液显
溶液显_________ 性,用离子方程式表示原因____________ ;请写出少量 通入到过量的
通入到过量的 溶液中发生反应的离子方程式:
溶液中发生反应的离子方程式:_________________________ .
(3) 溶液中加少量的
溶液中加少量的 固体,电离平衡
固体,电离平衡__________ 移动(填“正向”、“逆向”或“不”);体积均为100mL,pH均为2的 与一元酸HX溶液,加水稀释过程中pH与溶液体积的关系如图1所示,则
与一元酸HX溶液,加水稀释过程中pH与溶液体积的关系如图1所示,则
_________ (填“>”或“<”)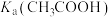 .
.
(4)25℃时,将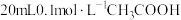 溶液和
溶液和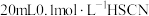 溶液分别与
溶液分别与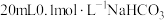 溶液混合,实验测得产生的气体体积
溶液混合,实验测得产生的气体体积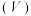 随时间
随时间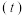 的变化如图2所示:反应初始阶段两种溶液产生
的变化如图2所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是________________________ ;假设混合后,两份溶液的体积仍相等,则反应结束后所得两溶液中,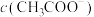
_____________ (填“>”、“<”或“=”) 
弱酸 |
|
|
|
|
电离平衡常数 |
|
|
|
|
(1)25℃时,在
 的
的 溶液中由水电离出来的
溶液中由水电离出来的
(2)
 溶液显
溶液显 通入到过量的
通入到过量的 溶液中发生反应的离子方程式:
溶液中发生反应的离子方程式:(3)
 溶液中加少量的
溶液中加少量的 固体,电离平衡
固体,电离平衡 与一元酸HX溶液,加水稀释过程中pH与溶液体积的关系如图1所示,则
与一元酸HX溶液,加水稀释过程中pH与溶液体积的关系如图1所示,则
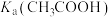 .
.
(4)25℃时,将
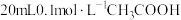 溶液和
溶液和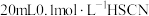 溶液分别与
溶液分别与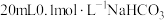 溶液混合,实验测得产生的气体体积
溶液混合,实验测得产生的气体体积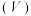 随时间
随时间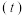 的变化如图2所示:反应初始阶段两种溶液产生
的变化如图2所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是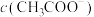

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示。根据该表,回答下列问题:
(1)假若 、
、 、HS-都是酸,则在相同条件下,试比较
、HS-都是酸,则在相同条件下,试比较 、H2CO3 、HS- 酸性由强到弱的顺序是
、H2CO3 、HS- 酸性由强到弱的顺序是________ 。
(2)Na2CO3溶液通入H2S的化学方程式是:__________ 。
(3)写出碳酸第一级电离的平衡常数表达式=__________ 。
(4))若保持温度不变,在CH3COOH溶液中通入少量HCl,则下列物理量变小的是________ 。
A.c(CH3COO-) B.c(H+) C.CH3COOH的电离平衡常数
(5)H+浓度相同的等体积的两份溶液HCl(A)和 CH3COOH(E),在相同温度下分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是_____ (填写序号)。
①反应所需要的时间E>A ②开始反应时的速率A>E ③参加反应的锌的物质的量A=E ④反应过程的平均速率E>A ⑤A溶液里有锌剩余 ⑥E溶液里有锌剩余
(6)已知 25℃时,相同浓度的 HF、CH3COOH、H2S溶液,其中酸性最强的是___ ,未电离的溶质分子浓度最大的是___ 。
| 化学式 | HF | CH3COOH | H2SO3 | H2CO3 | H2S |
| 电离平衡 常数(Ka) | 4.0×10-4 | 1.8×10-5 | K1=1.54×10-2 K2=1.02×10-7 | K1=4.4×10-7 K2=4.7×10-11 | K1=9.1×10-8 K2=1.1×10-12 |
(1)假若
 、
、 、HS-都是酸,则在相同条件下,试比较
、HS-都是酸,则在相同条件下,试比较 、H2CO3 、HS- 酸性由强到弱的顺序是
、H2CO3 、HS- 酸性由强到弱的顺序是(2)Na2CO3溶液通入H2S的化学方程式是:
(3)写出碳酸第一级电离的平衡常数表达式=
(4))若保持温度不变,在CH3COOH溶液中通入少量HCl,则下列物理量变小的是
A.c(CH3COO-) B.c(H+) C.CH3COOH的电离平衡常数
(5)H+浓度相同的等体积的两份溶液HCl(A)和 CH3COOH(E),在相同温度下分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是
①反应所需要的时间E>A ②开始反应时的速率A>E ③参加反应的锌的物质的量A=E ④反应过程的平均速率E>A ⑤A溶液里有锌剩余 ⑥E溶液里有锌剩余
(6)已知 25℃时,相同浓度的 HF、CH3COOH、H2S溶液,其中酸性最强的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室从废电路板粉碎金属料(主要含金属Cu,还含少量Zn、Fe、Pb等金属)中回收铜,其实验流程如下:

已知:一定pH范围内,Cu2+、Zn2+等能与氨形成配离子。
(1)“氨浸”在题图1所示的装置中进行。

①鼓入空气,金属Cu可被氧化生成[Cu(NH3)4] 2+,其离子方程式为________ ;
②空气流量过大,会降低Cu元素的浸出率,其原因是_____________ 。
③“氨浸”时向氨水中加入一定量(NH4)2SO4固体,有利于Cu2+转化为[Cu(NH3)4]2+,其原因是_________ 。
(2)洗涤滤渣所得的滤液与“过滤”所得滤液合并的目的是________________ 。
(3)滤液中主要阳离子为[Cu(NH3)4]2+、NH ,还含有一定量的[Zn(NH3)4]2+。其中铜氨配离子的离解反应可表示为:[Cu(NH3)4]2+(aq)
,还含有一定量的[Zn(NH3)4]2+。其中铜氨配离子的离解反应可表示为:[Cu(NH3)4]2+(aq)  Cu2+(aq) +4NH3(aq),该反应的平衡常数表达式为
Cu2+(aq) +4NH3(aq),该反应的平衡常数表达式为________ ;某有机溶剂HR可高效萃取离解出的Cu2+(实现Cu2+与Zn2+的有效分离),其原理为(org表示有机相):Cu2+(aq) + 2HR(org)  CuR2(org) + 2H+(org);再向有机相中加入稀硫酸,反萃取得到CuSO4溶液。
CuR2(org) + 2H+(org);再向有机相中加入稀硫酸,反萃取得到CuSO4溶液。

结合题图2和题图3,补充完整以滤液为原料,制取较纯净CuSO4·5H2O晶体的实验方案:_______ ,蒸发浓缩,冷却结晶,过滤洗涤干燥。(实验中可选用的试剂:有机溶剂HR、2mol·L−1硫酸、3mol·L−1硫酸)。

已知:一定pH范围内,Cu2+、Zn2+等能与氨形成配离子。
(1)“氨浸”在题图1所示的装置中进行。

①鼓入空气,金属Cu可被氧化生成[Cu(NH3)4] 2+,其离子方程式为
②空气流量过大,会降低Cu元素的浸出率,其原因是
③“氨浸”时向氨水中加入一定量(NH4)2SO4固体,有利于Cu2+转化为[Cu(NH3)4]2+,其原因是
(2)洗涤滤渣所得的滤液与“过滤”所得滤液合并的目的是
(3)滤液中主要阳离子为[Cu(NH3)4]2+、NH
 ,还含有一定量的[Zn(NH3)4]2+。其中铜氨配离子的离解反应可表示为:[Cu(NH3)4]2+(aq)
,还含有一定量的[Zn(NH3)4]2+。其中铜氨配离子的离解反应可表示为:[Cu(NH3)4]2+(aq)  Cu2+(aq) +4NH3(aq),该反应的平衡常数表达式为
Cu2+(aq) +4NH3(aq),该反应的平衡常数表达式为 CuR2(org) + 2H+(org);再向有机相中加入稀硫酸,反萃取得到CuSO4溶液。
CuR2(org) + 2H+(org);再向有机相中加入稀硫酸,反萃取得到CuSO4溶液。 
结合题图2和题图3,补充完整以滤液为原料,制取较纯净CuSO4·5H2O晶体的实验方案:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】 是重要的基础化工原料,其产量和消费量通常可以作为衡量一个国家工业发展水平的指标。请回答下列问题:
是重要的基础化工原料,其产量和消费量通常可以作为衡量一个国家工业发展水平的指标。请回答下列问题:
(1) 俗称纯碱,用离子方程式表示
俗称纯碱,用离子方程式表示 溶液呈碱性的原因
溶液呈碱性的原因_______ 。
(2) 溶液和
溶液和 溶液等体积混合,写出溶液中的钠元素和碳元素的物料守恒式
溶液等体积混合,写出溶液中的钠元素和碳元素的物料守恒式_______ ,将该混合溶液蒸干并灼烧得到的物质是_______ (填化学式)。
(3)已知:
向 溶液中滴加少量草酸溶液,发生反应的离子方程式
溶液中滴加少量草酸溶液,发生反应的离子方程式_______ 。
(4)常温下,将 粉末置于盛有
粉末置于盛有 蒸馏水的烧杯中,然后向烧杯中加入
蒸馏水的烧杯中,然后向烧杯中加入 固体(忽略溶液体积的变化)并充分搅拌,加入
固体(忽略溶液体积的变化)并充分搅拌,加入 固体的过程中,溶液中
固体的过程中,溶液中 和
和 的浓度变化曲线如图所示:
的浓度变化曲线如图所示:

①
_______ 。
②若使 ,全部转化为
,全部转化为 ,要加入的
,要加入的 的物质的量至少为
的物质的量至少为_______ 。
(5)一种熔融 燃料电池原理示意如图:
燃料电池原理示意如图:

①电池工作时, 向电极
向电极_______ (填“A”或“B”)移动。
②电极A上 参与的电极反应是
参与的电极反应是_______ 。
 是重要的基础化工原料,其产量和消费量通常可以作为衡量一个国家工业发展水平的指标。请回答下列问题:
是重要的基础化工原料,其产量和消费量通常可以作为衡量一个国家工业发展水平的指标。请回答下列问题:(1)
 俗称纯碱,用离子方程式表示
俗称纯碱,用离子方程式表示 溶液呈碱性的原因
溶液呈碱性的原因(2)
 溶液和
溶液和 溶液等体积混合,写出溶液中的钠元素和碳元素的物料守恒式
溶液等体积混合,写出溶液中的钠元素和碳元素的物料守恒式(3)已知:
 |  |
 |  |
向
 溶液中滴加少量草酸溶液,发生反应的离子方程式
溶液中滴加少量草酸溶液,发生反应的离子方程式(4)常温下,将
 粉末置于盛有
粉末置于盛有 蒸馏水的烧杯中,然后向烧杯中加入
蒸馏水的烧杯中,然后向烧杯中加入 固体(忽略溶液体积的变化)并充分搅拌,加入
固体(忽略溶液体积的变化)并充分搅拌,加入 固体的过程中,溶液中
固体的过程中,溶液中 和
和 的浓度变化曲线如图所示:
的浓度变化曲线如图所示:
①

②若使
 ,全部转化为
,全部转化为 ,要加入的
,要加入的 的物质的量至少为
的物质的量至少为(5)一种熔融
 燃料电池原理示意如图:
燃料电池原理示意如图:
①电池工作时,
 向电极
向电极②电极A上
 参与的电极反应是
参与的电极反应是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】草酸(H2C2O4,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用,常温下,H2C2O4:Ka1=5.4×10-2,Ka2=5.4×10-5。H2CO3:K1=4×10-7K2=6×10-11。
(1)NaHCO3溶液显____ 性。
(2)常温下,0.1mol·L-1的Na2C2O4溶液pH=a,0.1 mol·L-1的Na2CO3溶液pH=b,则a___ b(填“>”“<”或“=”)。
(3)常温下,pH=3的H2C2O4溶液的物质的量浓度为c1,水电离出的c(H+)为c3;pH=4的H2C2O4溶液的物质的量浓度为c2,水电离出的c(H+)为c4。则c1_____ 10c2(填“>”“<”或“=”,下同);10c3___ c4。
(4)常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4)=c(Na+)

①该草酸溶液的物质的量浓度为_________ (结果保留三位小数)。
②a点所示溶液中各离子的浓度由大到小的顺序为__________ 。
(1)NaHCO3溶液显
(2)常温下,0.1mol·L-1的Na2C2O4溶液pH=a,0.1 mol·L-1的Na2CO3溶液pH=b,则a
(3)常温下,pH=3的H2C2O4溶液的物质的量浓度为c1,水电离出的c(H+)为c3;pH=4的H2C2O4溶液的物质的量浓度为c2,水电离出的c(H+)为c4。则c1
(4)常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4)=c(Na+)

①该草酸溶液的物质的量浓度为
②a点所示溶液中各离子的浓度由大到小的顺序为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】为了保护环境,充分利用资源,可将工业废弃物转变成重要的化工原料。
请回答下列问题:
(1)可用NaClO3氧化酸性FeCl2废液得到FeCl3,FeCl3具有净水作用,但腐蚀设备。
①写出NaClO3氧化酸性FeCl2的离子方程式:__________________________ 。
②若酸性FeCl2废液中:c(Fe2+)=2.0×10-2 mol∕L,c(Fe3+)=1.0×10-3 mol∕L,c(Cl-)=5.3×10-2 mol∕L,则该溶液的pH约为_________ 。
③FeCl3净水的原理是:_________________ (用离子方程式及适当文字回答);FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是_________ (用离子方程式表示)。
(2)可用废铁屑为原料,按下图的工艺流程制备聚合硫酸铁(PFS),PFS是一种新型的
絮凝剂,处理污水比FeCl3高效,且腐蚀性小。
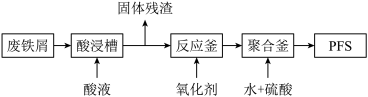
①酸浸时最合适的酸是______________ 。
②反应釜中加入的氧化剂,下列试剂中最合适的是____________ (填标号)。
a.HNO3 b.KMnO4 c.Cl2 d.H2O2
检验其中Fe2+是否完全被氧化,应选择____________________ (填标号)。
a.K3[Fe(CN)6]溶液 b.Na2SO3溶液 c.KSCN溶液
③生成PFS的离子方程式为:xFe3++yH2O ⇌ Fex(OH)y(3x-y)++yH+欲使平衡正向移动可采用的方法是____________ (填标号)。
a.加入NaHCO3 b.降温 c.加水稀释 d.加入NH4Cl
(3)废铁屑在一定条件下,可制得FeS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li+FeS2=Fe+2Li2S,维持电流强度为1A,a电池工作1小时,理论上消耗FeS2__________ g。(已知1mol电子的电量为96500C)
请回答下列问题:
(1)可用NaClO3氧化酸性FeCl2废液得到FeCl3,FeCl3具有净水作用,但腐蚀设备。
①写出NaClO3氧化酸性FeCl2的离子方程式:
②若酸性FeCl2废液中:c(Fe2+)=2.0×10-2 mol∕L,c(Fe3+)=1.0×10-3 mol∕L,c(Cl-)=5.3×10-2 mol∕L,则该溶液的pH约为
③FeCl3净水的原理是:
(2)可用废铁屑为原料,按下图的工艺流程制备聚合硫酸铁(PFS),PFS是一种新型的
絮凝剂,处理污水比FeCl3高效,且腐蚀性小。

①酸浸时最合适的酸是
②反应釜中加入的氧化剂,下列试剂中最合适的是
a.HNO3 b.KMnO4 c.Cl2 d.H2O2
检验其中Fe2+是否完全被氧化,应选择
a.K3[Fe(CN)6]溶液 b.Na2SO3溶液 c.KSCN溶液
③生成PFS的离子方程式为:xFe3++yH2O ⇌ Fex(OH)y(3x-y)++yH+欲使平衡正向移动可采用的方法是
a.加入NaHCO3 b.降温 c.加水稀释 d.加入NH4Cl
(3)废铁屑在一定条件下,可制得FeS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li+FeS2=Fe+2Li2S,维持电流强度为1A,a电池工作1小时,理论上消耗FeS2
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成离子化合物Y2O和Y2O2。
(1)Y2O2中含有的化学键是___________ 。
(2)用电子式表示Y2O的形成过程:___________ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是___________ (填化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是___________ (填化学式)。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式:___________ 。
(1)Y2O2中含有的化学键是
(2)用电子式表示Y2O的形成过程:
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】水溶液中的行为是中学化学的重要内容,按要求回答下列问题.
(1)在醋酸水溶液中存在平衡CH3COOH CH3COO-+ H+若分别改变下列条件: ①加水稀释②加热③加少量固体醋酸钠,其中能使醋酸电离程度增大的是
CH3COO-+ H+若分别改变下列条件: ①加水稀释②加热③加少量固体醋酸钠,其中能使醋酸电离程度增大的是_______ ,能使溶液pH增大的是_______ (填序号)。
(2)常温下,0.1mol·L-1NaHCO3溶液的pH 大于8,则溶液中Na+、HCO3-、CO32-、OH-四种微粒的浓度由大到小的顺序为:________________________________ 。
(3)AlCl3溶液加热蒸干并灼烧最终得到物质是________ (填化学式),将NaHCO3与Al2 (SO4)3溶液混合后可做泡沫灭火剂,其原理是_______ (用离子方程式表示)。
(4)已知下列物质在20℃下的Ksp如下:
① 当向含相同 浓度Cl-、Br-、I-的溶液中滴加AgNO3溶液时,_______ 先沉淀(填离子符号),
②向BaCl2 溶液中加入AgNO3和KBr,当两种淀共存时, =
=__________ 。
(1)在醋酸水溶液中存在平衡CH3COOH
 CH3COO-+ H+若分别改变下列条件: ①加水稀释②加热③加少量固体醋酸钠,其中能使醋酸电离程度增大的是
CH3COO-+ H+若分别改变下列条件: ①加水稀释②加热③加少量固体醋酸钠,其中能使醋酸电离程度增大的是(2)常温下,0.1mol·L-1NaHCO3溶液的pH 大于8,则溶液中Na+、HCO3-、CO32-、OH-四种微粒的浓度由大到小的顺序为:
(3)AlCl3溶液加热蒸干并灼烧最终得到物质是
(4)已知下列物质在20℃下的Ksp如下:
| 化学式 | AgCl | AgBr | AgI |
| 颜色 | 白色 | 浅黄色 | 黄色 |
| Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 |
① 当向含相同 浓度Cl-、Br-、I-的溶液中滴加AgNO3溶液时,
②向BaCl2 溶液中加入AgNO3和KBr,当两种淀共存时,
 =
=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】锌是一种常用金属,冶炼方法有火法和湿法。回答下列问题:
I.镓(Ga)是火法冶炼锌过程中的副产品,镓与铝同主族且相邻,化学性质与铝相似。
(1)Ga在元素周期表中的位置为___________ 。
(2)下列有关镓和镓的化合物的说法正确的是___________ (填字母)。
A一定条件下,Ga可溶于盐酸和氢氧化钠溶液
B常温下,Ga可与水剧烈反应放出氢气
C.Ga2O3可由Ga(OH)3受热分解得到
D一定条件下,Ga2O3可与NaOH反应生成盐
Ⅱ工业上利用锌熔砂(主要含ZnO、ZnFe2O4,还含有少量 CaO, FeO、CuO、NiO等氧化物)湿法制取金属锌的流程如图所示:

已知:Fe的活泼性强于Ni。
(3) ZnFe2O4可以写成ZnO·Fe2O3,写出ZnFe2O4与H2SO4反应的化学方程式:___________ 。
(4)净化Ⅰ工操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,仅使Fe3+转化为Fe(OH)3沉淀,净化I生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是______________________ 。
(5)净化Ⅱ中加入Zn的目的是______________________ 。
Ⅲ.(6)某化学课外小组拟用废旧电池锌皮(含杂质铁),结合如图所示信息,从提供的试剂中选取适当试剂,制取纯净的ZnSO4·7H2O。

实验步骤如下:
①将锌片完全溶于稍过量的3mol·L-1的稀硫酸,加入___________ (填字母,下同);
A.30%H2O2 B新制氯水 C.FeCl3溶液 D.KSCN溶液
②加入___________ ;
A纯锌粉 B纯碳酸钙粉末 C.纯ZnO粉末 D.3mol·L-1的稀硫酸
③加热到60℃左右并不断搅拌;
④趁热过滤得ZnSO4溶液,再蒸发浓缩、冷却结晶,过滤、洗涤、干燥。
其中步骤③加热的主要目的是_________________________________ 。
I.镓(Ga)是火法冶炼锌过程中的副产品,镓与铝同主族且相邻,化学性质与铝相似。
(1)Ga在元素周期表中的位置为
(2)下列有关镓和镓的化合物的说法正确的是
A一定条件下,Ga可溶于盐酸和氢氧化钠溶液
B常温下,Ga可与水剧烈反应放出氢气
C.Ga2O3可由Ga(OH)3受热分解得到
D一定条件下,Ga2O3可与NaOH反应生成盐
Ⅱ工业上利用锌熔砂(主要含ZnO、ZnFe2O4,还含有少量 CaO, FeO、CuO、NiO等氧化物)湿法制取金属锌的流程如图所示:

已知:Fe的活泼性强于Ni。
(3) ZnFe2O4可以写成ZnO·Fe2O3,写出ZnFe2O4与H2SO4反应的化学方程式:
(4)净化Ⅰ工操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,仅使Fe3+转化为Fe(OH)3沉淀,净化I生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是
(5)净化Ⅱ中加入Zn的目的是
Ⅲ.(6)某化学课外小组拟用废旧电池锌皮(含杂质铁),结合如图所示信息,从提供的试剂中选取适当试剂,制取纯净的ZnSO4·7H2O。

实验步骤如下:
①将锌片完全溶于稍过量的3mol·L-1的稀硫酸,加入
A.30%H2O2 B新制氯水 C.FeCl3溶液 D.KSCN溶液
②加入
A纯锌粉 B纯碳酸钙粉末 C.纯ZnO粉末 D.3mol·L-1的稀硫酸
③加热到60℃左右并不断搅拌;
④趁热过滤得ZnSO4溶液,再蒸发浓缩、冷却结晶,过滤、洗涤、干燥。
其中步骤③加热的主要目的是
您最近一年使用:0次