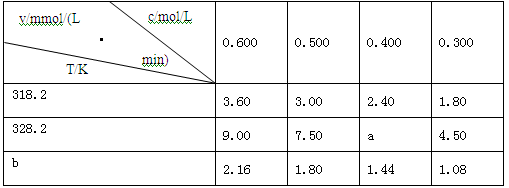
一定温度下,在3个1.0L的恒容密闭容器中分别进行反应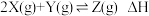 ,达到平衡。相关数据如表。下列说法不正确的是
,达到平衡。相关数据如表。下列说法不正确的是
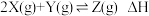 ,达到平衡。相关数据如表。下列说法不正确的是
,达到平衡。相关数据如表。下列说法不正确的是| 容器 | 温度/K | 物质的起始浓度/(mol∙L-1) | 物质的平衡浓度/(mol∙L-1) | ||
| c(X) | c(Y) | c(Z) | c(Z) | ||
| I | 400 | 0.20 | 0.10 | 0 | 0.080 |
| II | 400 | 0.40 | 0.20 | 0 | a |
| III | 500 | 0.20 | 0.10 | 0 | 0.025 |
| A.平衡时,X的转化率:II>I | B.平衡常数:K(Ⅱ)=K(Ⅰ) |
| C.达到平衡所需时间:III<I | D.a=0.16 |
20-21高二上·江苏南通·期中 查看更多[10]
安徽省合肥市第一中学2023-2024学年高二上学期12月月考化学试题广东省深圳市美中学校2022-2023学年高二上学期期中考试化学试题辽宁省东北育才学校高中部2023-2024学年高二上学期第一次月考化学试题广西壮族自治区梧州市苍梧中学2022-2023学年高二上学期11月月考化学试题四川省冕宁中学2022-2023学年高二上学期12月月考化学试题湖南省长沙市长郡中学2022--2023学年高二上学期第二次线上月考化学试题湖南省长沙市长郡中学2022--2023学年高二上学期第二次线上月考化学试题新疆石河子第一中学2022-2023学年高二10月月考化学试题湖南省长郡中学2022-2023学年高二上学期第一次月考化学试题江苏省启东市2020-2021学年高二上学期期中考试化学试题
更新时间:2022-10-09 10:35:31
|
相似题推荐
【推荐1】下列实验方法或方案不能到目的的是( )
| 选项 | 目的 | 实验方法或方案 |
| A | 探究压强对化学平衡的影响 |   |
| B | 测稀硫酸与铁屑的反应速率 | 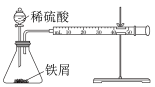 |
| C | 测定中和反应的反应热 | 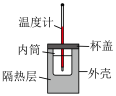 |
| D | 探究温度对化学反应速率的影响 | 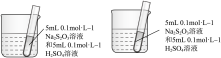 冷水 热水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO2(g)⇌2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正·c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆·c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是
| 容器 编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
| c(NO2) | c(NO) | c(O2) | c(O2) | |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
A.设K为该反应的化学平衡常数,则有K=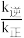 |
| B.达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比为20∶17 |
| C.容器Ⅱ中起始时平衡正向移动,达到平衡时,容器Ⅱ中NO2的转化率比容器Ⅰ中的小 |
| D.若改变温度为T2,且T2>T1,则k正∶k逆<0.8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】二氧化硫的催化氧化反应:2SO2(g)+O2(g) 2SO3(g)是工业制硫酸的重要反应之一,下列说法
2SO3(g)是工业制硫酸的重要反应之一,下列说法错误 的是
 2SO3(g)是工业制硫酸的重要反应之一,下列说法
2SO3(g)是工业制硫酸的重要反应之一,下列说法| A.该反应加入催化剂是为了加快反应速率 |
| B.已知该催化氧化反应K(300 ℃)>K(350 ℃),则该反应正向是放热反应 |
| C.煅烧硫铁矿(主要成分FeS2)可获得SO2,将矿石粉碎成小颗粒可提高反应的平衡转化率 |
| D.保持温度不变,平衡后增大O2的浓度,该反应的平衡常数K不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中,不能用勒夏特列原理解释的是
| A.90℃纯水的pH<7 |
| B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 |
| C.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
D.溴水中存在如下平衡: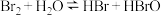 ,当加入NaOH溶液后颜色变浅 ,当加入NaOH溶液后颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
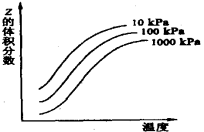
【推荐2】如图是温度和压强对X+Y 2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
 2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
| A.上述可逆反应的正反应为放热反应 |
| B.增大压强平衡正向移动 |
| C.X、Y、Z均为气态 |
| D.X和Y中只有一种为气态,Z为气态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
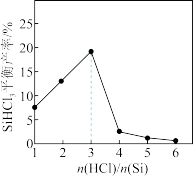
【推荐1】有关反应Si(s)+3HCl(g) SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
 SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
| A.该反应在低温条件下不能自发 |
| B.其他条件不变,增大压强SiHCl3平衡产率减小 |
| C.实际工业生产选择高温,原因是高温时Si的平衡转化率比低温时大 |
D.如图所示,当 >3,SiHCl3平衡产率减小可能发生了副反应 >3,SiHCl3平衡产率减小可能发生了副反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol·L-1、c(B)=0.200mol·L-1及c(C)=0mol·L-1,反应物A的浓度随时间的变化如图所示。下列说法不正确的是
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol·L-1、c(B)=0.200mol·L-1及c(C)=0mol·L-1,反应物A的浓度随时间的变化如图所示。下列说法不正确的是

 C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol·L-1、c(B)=0.200mol·L-1及c(C)=0mol·L-1,反应物A的浓度随时间的变化如图所示。下列说法不正确的是
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol·L-1、c(B)=0.200mol·L-1及c(C)=0mol·L-1,反应物A的浓度随时间的变化如图所示。下列说法不正确的是
| A.与①比较,②可能加入催化剂 |
| B.与①比较,③可能是增大了压强 |
| C.实验②平衡时B的转化率为40% |
| D.该反应的ΔH﹥0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一定温度下,在密闭容器中可能发生如下两个反应,反应1:2A(g)+B(g) 3C(g)+D(s);反应2:C(g)
3C(g)+D(s);反应2:C(g) 2E(g)。若反应开始时充入2molA和2molB,在下列不同条件下达到平衡时,下列说法不正确的是
2E(g)。若反应开始时充入2molA和2molB,在下列不同条件下达到平衡时,下列说法不正确的是
 3C(g)+D(s);反应2:C(g)
3C(g)+D(s);反应2:C(g) 2E(g)。若反应开始时充入2molA和2molB,在下列不同条件下达到平衡时,下列说法不正确的是
2E(g)。若反应开始时充入2molA和2molB,在下列不同条件下达到平衡时,下列说法不正确的是| A.恒温恒压下,当气体的密度不再变化时,反应一定达到平衡 |
| B.恒温恒压下,通入氮气,达新平衡后B的转化率增大 |
| C.恒温恒容下(体积为1L),10分钟后达到平衡时,A的转化率为25%,则10分钟内C的平均速率为0.075mol/(L·min) |
| D.恒温恒容下,如只发生反应1,达到平衡后,再充入2molC和过量的D,达新平衡后气体中A的体积分数增大 |
您最近一年使用:0次
【推荐1】已知CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g),在1L密闭容器中分别加入0.5mol CH4和1 mol NO2保持温度不变,测得n(CH4 )随时间变化的有关实验数据如表所示。下列说法不正确的是
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| n(CH4)/mol | 0.5 | 0.35 | 0.25 | 0.17 | 0.10 | 0.10 |
| A.0~20min内,NO2 的反应速率为0.025 mol•L-1•min-1 |
| B.由实验数据可知,该反应在50min时才达平衡状态 |
| C.随着反应的进行,反应物的浓度降低,反应速率减慢 |
| D.达平衡时,二氧化氮的转化率与甲烷的转化率相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在恒压、NO和O2的起始浓度一定的条件下, 催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是
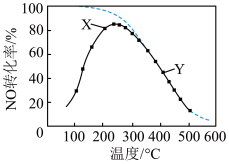
| A.反应2NO(g)+O2(g)=2NO2(g)的 ΔH>0 |
| B.图中X点所示条件下,延长反应时间能提高NO转化率 |
| C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率 |
| D.380℃下,c起始(O2)=5.0 ×10-4 mol·L-1, NO平衡转化率为50%,则平衡常数K<2000 |
您最近一年使用:0次