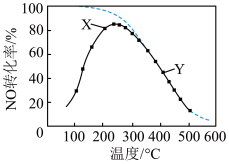
在恒压、NO和O2的起始浓度一定的条件下, 催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是
| A.反应2NO(g)+O2(g)=2NO2(g)的 ΔH>0 |
| B.图中X点所示条件下,延长反应时间能提高NO转化率 |
| C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率 |
| D.380℃下,c起始(O2)=5.0 ×10-4 mol·L-1, NO平衡转化率为50%,则平衡常数K<2000 |
20-21高二上·江苏镇江·期末 查看更多[11]
江苏省南京市第一中学2023-2024学年高一下学期期中考试化学试卷福建省厦门市第一中学2021-2022学年高二上学期 期中考试化学试卷河北省石家庄市河北正定中学2024届高三上学期第二次月考化学试题福建省宁德第一中学2022-2023学年高二上学期第二次月考化学试题山西省晋中市平遥县第二中学校2021-2022学年高二上学期期中考试化学试题内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题河南省范县第一中学2021-2022学年高二上学期期中检测化学试题贵州省毕节市金沙县第一中学2021-2022学年高二上学期期中考试化学试题江苏省扬州市江都区大桥高级中学2020-2021学年高二下学期学情检测(二)化学试题(已下线)【镇江新东方】高二下期中21高二期中校级联考江苏省镇江中学2020-2021学年高二上学期期末考试化学试题
更新时间:2021-06-20 21:45:32
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】将1mol A(g)和2mol B(g)置于2L某密闭容器中,在一定温度下发生反应:A(g)+B(g) C(g)+D(g),并达到平衡。C的体积分数随时间变化如下图I中曲线b所示,反应过程中的能量变化如图II所示,下列说法不正确的是( )
C(g)+D(g),并达到平衡。C的体积分数随时间变化如下图I中曲线b所示,反应过程中的能量变化如图II所示,下列说法不正确的是( )

 C(g)+D(g),并达到平衡。C的体积分数随时间变化如下图I中曲线b所示,反应过程中的能量变化如图II所示,下列说法不正确的是( )
C(g)+D(g),并达到平衡。C的体积分数随时间变化如下图I中曲线b所示,反应过程中的能量变化如图II所示,下列说法不正确的是( )
| A.反应在第4秒钟达到化学平衡状态,0~4秒内,以A表示的化学反应速率是0.225mol·L-1·s-1 |
| B.该温度下,反应的平衡常数数值约为7.36 |
| C.恒温条件下,缩小反应容器体积可以使反应的过程按图I中a曲线进行 |
| D.在上述反应体系中加入催化剂,化学反应速率增大,E1和E2均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐2】一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:
2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
2X(g)+Y(g)
 Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是| A.以X浓度变化表示的反应速率为0.001mol/(L·S) |
B.将容器体积变为20L,Z的平衡浓度变为原来的 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的△H>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】将一定量的CO2与H2通入某密闭容器中合成甲醇,在催化剂作用下发生下述反应:
Ⅰ. CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1<0
CH3OH(g)+H2O(g) ΔH1<0
Ⅱ. CO2(g)+H2(g) H2O(g)+CO(g) ΔH2
H2O(g)+CO(g) ΔH2
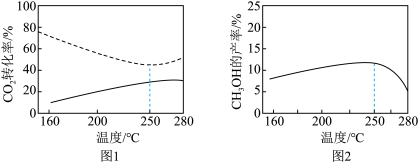
催化反应相同时间,测得不同温度下CO2的转化率如图1所示(图中虚线表示相同条件下CO2的平衡转化率随温度的变化),CH3OH 的产率如图2所示。
下列有关说法正确的是
Ⅰ. CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1<0
CH3OH(g)+H2O(g) ΔH1<0Ⅱ. CO2(g)+H2(g)
 H2O(g)+CO(g) ΔH2
H2O(g)+CO(g) ΔH2催化反应相同时间,测得不同温度下CO2的转化率如图1所示(图中虚线表示相同条件下CO2的平衡转化率随温度的变化),CH3OH 的产率如图2所示。

下列有关说法正确的是
| A.ΔH2 < 0 |
| B.250℃时,容器内反应达平衡 |
| C.250℃后, 随温度升高CH3OH 的产率减小,可能是因为催化剂对反应Ⅰ的活性降低 |
| D.250℃前,随温度升高CO2的平衡转化率减小,可能因为该温度范围内仅发生反应Ⅰ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】将2mL 0.1mol·L -1 FeCl3溶液和2mL 0.01mol·L -1 KSCN溶液混合,发生如下反应:FeCl3(aq)+3KSCN(aq)  Fe(SCN)3(aq)+3KCl(aq),为了使平衡状态向逆反应方向移动,应选择的条件是:①再加入2mL1mol·L -1FeCl3 溶液 ② 加入KCl固体 ③ 加入适量的铁粉 ④ 再加入2mL0.4mol·L -1KSCN溶液
Fe(SCN)3(aq)+3KCl(aq),为了使平衡状态向逆反应方向移动,应选择的条件是:①再加入2mL1mol·L -1FeCl3 溶液 ② 加入KCl固体 ③ 加入适量的铁粉 ④ 再加入2mL0.4mol·L -1KSCN溶液
 Fe(SCN)3(aq)+3KCl(aq),为了使平衡状态向逆反应方向移动,应选择的条件是:①再加入2mL1mol·L -1FeCl3 溶液 ② 加入KCl固体 ③ 加入适量的铁粉 ④ 再加入2mL0.4mol·L -1KSCN溶液
Fe(SCN)3(aq)+3KCl(aq),为了使平衡状态向逆反应方向移动,应选择的条件是:①再加入2mL1mol·L -1FeCl3 溶液 ② 加入KCl固体 ③ 加入适量的铁粉 ④ 再加入2mL0.4mol·L -1KSCN溶液| A.②③ | B.③ | C.②④ | D.①③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关实验结论正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向FeCl3和KSCN的混合溶液中加入KCl溶液 | 溶液红色变浅 | 增大生成物浓度,平衡向逆反应方向移动 |
| B | 某无色溶液中加入硝酸酸化,再加硝酸钡溶液 | 有白色沉淀 | 说明溶液中含有SO42- |
| C | 饱和氯化银溶液与饱和碘化银溶液等体积混合 | 有黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 用洁净的铂丝蘸取少量溶液在酒精灯上灼烧 | 火焰呈紫色 | 该溶液一定是钾盐溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醇水蒸气重整制氢(SRM)是获取理想氢源的有效方法。重整过程发生的反应如下:
反应Ⅰ: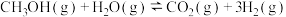

反应Ⅱ: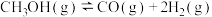

在常压、催化剂下,向密闭容器中充入 和
和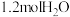 混合气体,t时刻测得
混合气体,t时刻测得 转化率及
转化率及 、
、 的选择性随温度变化情况如图所示(曲线
的选择性随温度变化情况如图所示(曲线 为
为 的选择性),下列说法正确的是
的选择性),下列说法正确的是
反应Ⅰ:
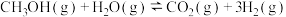

反应Ⅱ:
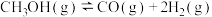

在常压、催化剂下,向密闭容器中充入
 和
和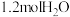 混合气体,t时刻测得
混合气体,t时刻测得 转化率及
转化率及 、
、 的选择性随温度变化情况如图所示(曲线
的选择性随温度变化情况如图所示(曲线 为
为 的选择性),下列说法正确的是
的选择性),下列说法正确的是
A.曲线 为 为 的选择性 的选择性 |
B.图中 时,容器中的 时,容器中的 约为 约为 |
C.选择 作为反应温度比较适宜 作为反应温度比较适宜 |
D.选用 选择性较高的催化剂有利于提高 选择性较高的催化剂有利于提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下,CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数K=1,该温度下在体积均为1L的甲、乙两个恒容密闭容器中,投入CO(g)和H2O(g)的起始浓度及5min时的浓度如表所示。
CO2(g)+H2(g)的平衡常数K=1,该温度下在体积均为1L的甲、乙两个恒容密闭容器中,投入CO(g)和H2O(g)的起始浓度及5min时的浓度如表所示。
下列判断不正确的是( )
 CO2(g)+H2(g)的平衡常数K=1,该温度下在体积均为1L的甲、乙两个恒容密闭容器中,投入CO(g)和H2O(g)的起始浓度及5min时的浓度如表所示。
CO2(g)+H2(g)的平衡常数K=1,该温度下在体积均为1L的甲、乙两个恒容密闭容器中,投入CO(g)和H2O(g)的起始浓度及5min时的浓度如表所示。甲 | 乙 | |||
| 起始浓度 | 5min时浓度 | 起始浓度 | 5min时浓度 | |
| c(CO)/mol/L | 0.1 | 0.08 | 0.2 | x |
| c(H2O)/mol/L | 0.1 | 0.08 | 0.2 | y |
下列判断不正确的是( )
| A.x=y=0.16 |
| B.反应开始时,乙中反应速率快 |
| C.甲中0~5min平均反应速率υ(CO)=0.004mol•L-1•min-1 |
| D.平衡时,乙中的转化率是50%,c(CO)是甲中的2倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在一定温度下,将气体X和气体Y各0.32mol充入10L恒容密闭容器中,发生反应x(g)+ Y(g)  2Z(g)AH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g)AH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是
 2Z(g)AH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g)AH<0,一段时间后达到平衡。反应过程中测定的数据如下表:t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.24 | 0.22 | 0.20 | 0.20 |
| A.反应前2min 的平均速率 v(Z)=4.0×10-3mol/(L·min) |
| B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) |
| C.该温度下此反应的平衡常数k=1.44 |
| D.其他条件不变,再充入0.2molZ,平衡时X的体积分数减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
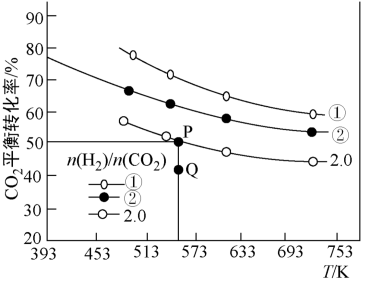
【推荐1】在三个容积均为1L的密闭容器中以不同的氢碳比[ ]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率与温度的关系如图所示。下列说法正确的是
C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率与温度的关系如图所示。下列说法正确的是
 ]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率与温度的关系如图所示。下列说法正确的是
C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率与温度的关系如图所示。下列说法正确的是
| A.该反应的ΔH>0 |
| B.氢碳比:①<② |
| C.在氢碳比为2.0时,Q点v(正)<v(逆) |
D.在氢碳比为2.0时,P点存在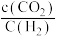 =1 =1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】乙醇-水催化重整可获得H2.其主要反应为
反应1: ,
,
反应2: 。
。
在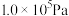 、
、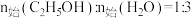 时,若仅考虑上述反应,平衡时CO2和CO的选择性及H2的产率随温度的变化如图所示。
时,若仅考虑上述反应,平衡时CO2和CO的选择性及H2的产率随温度的变化如图所示。

CO的选择性 ,下列说法正确的是
,下列说法正确的是
反应1:
 ,
,反应2:
 。
。在
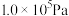 、
、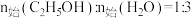 时,若仅考虑上述反应,平衡时CO2和CO的选择性及H2的产率随温度的变化如图所示。
时,若仅考虑上述反应,平衡时CO2和CO的选择性及H2的产率随温度的变化如图所示。
CO的选择性
 ,下列说法正确的是
,下列说法正确的是A.C2H5OH(g)+H2O(g) 2CO(g)+4H2(g) ΔH=214.5kJ·mol-1 2CO(g)+4H2(g) ΔH=214.5kJ·mol-1 |
| B.升高温度,平衡时CO2的选择性增大 |
C.反应1在一定温度下,增大 ,乙醇平衡转化率减小 ,乙醇平衡转化率减小 |
| D.反应2在一定温度下,加入CaO(S)或选用高效催化剂,均能提高平衡时H2的转化率 |
您最近一年使用:0次

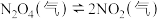 ,将装有
,将装有 和
和 混合气体的密闭烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论能说明该反应已经达到化学平衡状态的是
混合气体的密闭烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论能说明该反应已经达到化学平衡状态的是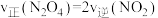
 、
、 和
和 。反应相同的时间,
。反应相同的时间, 转化率随温度的变化关系如图所示。下列说法正确的是
转化率随温度的变化关系如图所示。下列说法正确的是




