高炉炼铁过程中发生的主要反应为 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应正反应是_______ 热反应(填“吸”或“放”);
(2)欲提高反应中CO的平衡转化率,可采取的措施是_______ ;
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.加入合适的催化剂 E.增大容器的容积
(3)在一个容积为1L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各2.0mol,反应经过5min后达到平衡.求该时间范围内反应的平均反应速率:v(CO2)=_______ 、CO的平衡转化率=_______ 。如果此时向密闭容器中加入CO和CO2各2mol,平衡_______ (填“向正方向”、“向逆方向”、“不”)移动。
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应正反应是
(2)欲提高反应中CO的平衡转化率,可采取的措施是
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.加入合适的催化剂 E.增大容器的容积
(3)在一个容积为1L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各2.0mol,反应经过5min后达到平衡.求该时间范围内反应的平均反应速率:v(CO2)=
更新时间:2022-10-22 08:45:41
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】碘是国防、工业、农业、医药等部门和行业所依赖的重要原料,海水提碘是从海藻中提取元素碘的技术。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)
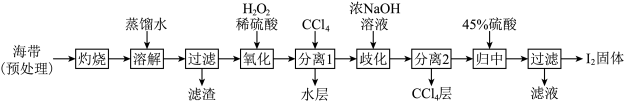
(1)“氧化”过程涉及到的离子方程式是________ ,请设计一种检验氧化后所得溶液含I2的方法:________ 。
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为________ ;向分离得到的含I-和 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为________ 。
Ⅱ.获取重要的还原剂-HI
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为________ kJ。

(4)Bodensteins研究了反应: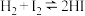 。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
前40min的平均速率v(HI)=________ 。
Ⅲ.生命延续-心脏起搏器中的Li-I2电池
(5)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为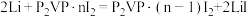 ,其工作原理如图所示:
,其工作原理如图所示:
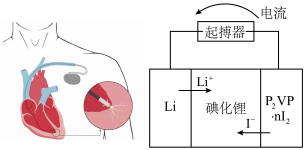
①正极发生的电极反应式为________ ;
②放电时,转移0.6×6.02×1023个电子,负极质量减少________ g。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)

(1)“氧化”过程涉及到的离子方程式是
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为
 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为Ⅱ.获取重要的还原剂-HI
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为

(4)Bodensteins研究了反应:
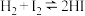 。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:| 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 |
| 1molH2(g)、1molI2(g) | n(H2)mol | 1 | 0.5 | 0.32 | 0.24 | 0.20 |
Ⅲ.生命延续-心脏起搏器中的Li-I2电池
(5)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为
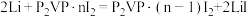 ,其工作原理如图所示:
,其工作原理如图所示:
①正极发生的电极反应式为
②放电时,转移0.6×6.02×1023个电子,负极质量减少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ﹒在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为4 mol,B为6 mol,5 min末时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。
3C(g)+nD(g),开始时A为4 mol,B为6 mol,5 min末时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。
计算:
(1)5 min末A的物质的量浓度为___________ ,A的转化率为___________ 。
(2)前5 min内用B表示的化学反应速率v(B)为___________ 。
(3)化学方程式中n=___________ 。
(4)此反应在四种不同情况下的反应速率分别为:
①v(A)=5 mol·L-1·min-1 ②v(B)=6 mol·L-1·min-1
③v(C)=0.2 mol·L-1·s-1 ④v(D)=8 mol·L-1·min-1
其中反应速率最快的是___________ (填序号)。
Ⅱ.H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。

(1)若利用图甲装置,可通过观察___________ 现象,从而定性比较得出结论。
(2)有同学提出将0.1 mol·L-1 FeCl3改为___________ mol·L-1 Fe2(SO4)3更为合理,其理由是___________ 。
(3)若利用乙实验可进行定量分析,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是___________ 。
(4)将0.1 mol MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示

解释反应速率变化的原因:___________ 。
 3C(g)+nD(g),开始时A为4 mol,B为6 mol,5 min末时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。
3C(g)+nD(g),开始时A为4 mol,B为6 mol,5 min末时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。计算:
(1)5 min末A的物质的量浓度为
(2)前5 min内用B表示的化学反应速率v(B)为
(3)化学方程式中n=
(4)此反应在四种不同情况下的反应速率分别为:
①v(A)=5 mol·L-1·min-1 ②v(B)=6 mol·L-1·min-1
③v(C)=0.2 mol·L-1·s-1 ④v(D)=8 mol·L-1·min-1
其中反应速率最快的是
Ⅱ.H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。

(1)若利用图甲装置,可通过观察
(2)有同学提出将0.1 mol·L-1 FeCl3改为
(3)若利用乙实验可进行定量分析,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
(4)将0.1 mol MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示

解释反应速率变化的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甲烷是优质气体燃料,也是制造合成气和许多化工产品的重要原料。请根据所学知识回答下列问题:
(1)某些常见化学键的键能(将 气体分子
气体分子 断裂为中性气态原子
断裂为中性气态原子 和
和 所需的能量或
所需的能量或 和
和 合成
合成 气体所放出的能量)数据如下表:
气体所放出的能量)数据如下表:
 完全燃烧生成
完全燃烧生成 和气态水放出的能量为
和气态水放出的能量为___________  。该反应中反应物的总能量
。该反应中反应物的总能量___________ (填“>”“<”或“=”)生成物的总能量。
(2)一定条件下,通过 加氢可以制备
加氢可以制备 ,反应方程式为
,反应方程式为 。在一定温度下,将
。在一定温度下,将 和
和 放入
放入 恒容密闭容器中,测得反应过程中
恒容密闭容器中,测得反应过程中 的浓度随时间的变化如表所示:
的浓度随时间的变化如表所示:
① 内,
内,
___________  ,
,
___________  。
。
②平衡时的压强为起始压强的___________ 倍。
③平衡时, 的转化率为
的转化率为___________ %。
④下列条件能判断该反应达到化学平衡状态的是___________ (填标号)。
a.
b.容器内气体的密度保持不变
c.容器中气体的平均摩尔质量不变
d. 与
与 的浓度相等
的浓度相等
(1)某些常见化学键的键能(将
 气体分子
气体分子 断裂为中性气态原子
断裂为中性气态原子 和
和 所需的能量或
所需的能量或 和
和 合成
合成 气体所放出的能量)数据如下表:
气体所放出的能量)数据如下表:| 化学键 |  |  |  |  |
键能 | 414 | 803 | 463 | 498 |
 完全燃烧生成
完全燃烧生成 和气态水放出的能量为
和气态水放出的能量为 。该反应中反应物的总能量
。该反应中反应物的总能量(2)一定条件下,通过
 加氢可以制备
加氢可以制备 ,反应方程式为
,反应方程式为 。在一定温度下,将
。在一定温度下,将 和
和 放入
放入 恒容密闭容器中,测得反应过程中
恒容密闭容器中,测得反应过程中 的浓度随时间的变化如表所示:
的浓度随时间的变化如表所示: | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
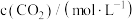 | 1 | 0.5 | 0.3 | 0.25 | 0.2 | 0.2 | 0.2 |
 内,
内,
 ,
,
 。
。②平衡时的压强为起始压强的
③平衡时,
 的转化率为
的转化率为④下列条件能判断该反应达到化学平衡状态的是
a.

b.容器内气体的密度保持不变
c.容器中气体的平均摩尔质量不变
d.
 与
与 的浓度相等
的浓度相等
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题。
(1)合成氨是工业上的重要反应: △H<0,下列说法错误的是
△H<0,下列说法错误的是_______ 。
A.增大压强既加快反应速率,又有利于平衡向合成氨方向移动
B.反应达平衡状态后,单位时间内生成1mol N2的同时消耗3mol H2
C.铁作催化剂既加快反应速率,又有利于平衡向合成氨方向移动
(2)合成氨工业中: △H<0,其化学平衡常数K与温度t的关系如表:
△H<0,其化学平衡常数K与温度t的关系如表:
完成下列填空:
①试比较K1、K2的大小,K1___________ K2(填写“>”、“=”或“<”)。
②400℃时,该反应的化学平衡常数的表达式_______ 。当测得NH3和N2、H2的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则此时平衡___________ (填“正向移动”或“逆向移动”或“不移动”),此时
___________  (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)
③已知

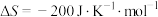 ,则该反应在温度低于
,则该反应在温度低于___________ K时能自发,但工业上选择反应温度在400℃~500℃是为了___________ 。
(1)合成氨是工业上的重要反应:
 △H<0,下列说法错误的是
△H<0,下列说法错误的是A.增大压强既加快反应速率,又有利于平衡向合成氨方向移动
B.反应达平衡状态后,单位时间内生成1mol N2的同时消耗3mol H2
C.铁作催化剂既加快反应速率,又有利于平衡向合成氨方向移动
(2)合成氨工业中:
 △H<0,其化学平衡常数K与温度t的关系如表:
△H<0,其化学平衡常数K与温度t的关系如表:| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②400℃时,该反应的化学平衡常数的表达式

 (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)③已知


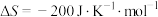 ,则该反应在温度低于
,则该反应在温度低于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】CO可用于合成甲醇,化学方程式为:CO(g)+2H2(g)  CH3OH(g)。
CH3OH(g)。

(1)图1是反应CO(g)+2H2(g) CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。
①该反应的焓变ΔH___________ (填“>”“<”或“=”)0。
②T1和T2温度下的平衡常数大小关系是K1___________ (填“>”“<”或“=”)K2.在T1温度下,往体积为1 L的密闭容器中,充入1 mol CO和2 mol H2,经测得CO和CH3OH(g)的浓度随时间变化如图2所示。则该条件下CO的平衡转化率为___________ 。

③若容器容积不变,下列措施可增加CO转化率的是___________ (填字母)。
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
(2)在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线z对应的温度是___________ ℃;该温度下上述反应的化学平衡常数为___________ 。
 CH3OH(g)。
CH3OH(g)。
(1)图1是反应CO(g)+2H2(g)
 CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。①该反应的焓变ΔH
②T1和T2温度下的平衡常数大小关系是K1

③若容器容积不变,下列措施可增加CO转化率的是
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
(2)在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线z对应的温度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】水溶液是中学化学的重点研究对象。
(1)水是极弱的电解质,常温下某电解质溶解在水中后,溶液中的 mol·L
mol·L ,则该电解质可能是___________(填字母)。
,则该电解质可能是___________(填字母)。
(2)已知次氯酸是比碳酸还弱的酸,要使新制稀氯水中的 增大,可以采取的措施为___________(填字母)。
增大,可以采取的措施为___________(填字母)。
(3)强酸制弱酸是水溶液中的重要经验规律。若HA、 是两种弱酸,存在以下关系:
是两种弱酸,存在以下关系: (少量)
(少量) ,则
,则 、
、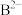 、
、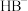 结合
结合 的难易顺序为
的难易顺序为___________ 。
(4)常温下,为证明 是弱电解质,某同学取出10 mL 0.10 mol⋅L
是弱电解质,某同学取出10 mL 0.10 mol⋅L 氨水,用pH试纸测其pH为a;用蒸馏水稀释至1000 mL,再用pH试纸测其pH为b.只要a、b满足关系
氨水,用pH试纸测其pH为a;用蒸馏水稀释至1000 mL,再用pH试纸测其pH为b.只要a、b满足关系___________ (用等式或不等式表示),就可确认 是弱电解质。
是弱电解质。
(5)已知:25℃时,两种常见弱酸的电离平衡常数:
①25℃时,10 mL 0.10 mol⋅L
 溶液与10 mL 0.10 mol⋅L
溶液与10 mL 0.10 mol⋅L
 溶液中,离子总数大小关系:
溶液中,离子总数大小关系: 溶液
溶液___________  溶液(填“>”、“<”或“=”)。
溶液(填“>”、“<”或“=”)。
②向 溶液中通入过量
溶液中通入过量 反应的离子方程式为
反应的离子方程式为___________ 。
(1)水是极弱的电解质,常温下某电解质溶解在水中后,溶液中的
 mol·L
mol·L ,则该电解质可能是___________(填字母)。
,则该电解质可能是___________(填字母)。A. | B.HCl | C. | D.NaOH |
 增大,可以采取的措施为___________(填字母)。
增大,可以采取的措施为___________(填字母)。A.再通入 | B.加碳酸钙粉末 | C.加氯酸钠溶液 | D.加NaOH |
 是两种弱酸,存在以下关系:
是两种弱酸,存在以下关系: (少量)
(少量) ,则
,则 、
、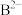 、
、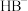 结合
结合 的难易顺序为
的难易顺序为(4)常温下,为证明
 是弱电解质,某同学取出10 mL 0.10 mol⋅L
是弱电解质,某同学取出10 mL 0.10 mol⋅L 氨水,用pH试纸测其pH为a;用蒸馏水稀释至1000 mL,再用pH试纸测其pH为b.只要a、b满足关系
氨水,用pH试纸测其pH为a;用蒸馏水稀释至1000 mL,再用pH试纸测其pH为b.只要a、b满足关系 是弱电解质。
是弱电解质。(5)已知:25℃时,两种常见弱酸的电离平衡常数:
| 酸 | 电离平衡常数 |
 |   |
 | 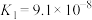 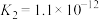 |

 溶液与10 mL 0.10 mol⋅L
溶液与10 mL 0.10 mol⋅L
 溶液中,离子总数大小关系:
溶液中,离子总数大小关系: 溶液
溶液 溶液(填“>”、“<”或“=”)。
溶液(填“>”、“<”或“=”)。②向
 溶液中通入过量
溶液中通入过量 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:
①反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=
CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=________ (用ΔH1和ΔH2表示),K=________ (用K1和K2表示)。
②能判断CO2(g)+H2(g) CO(g)+H2O(g)达到化学平衡状态的依据是
CO(g)+H2O(g)达到化学平衡状态的依据是____ (填字母)。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。

①该条件下反应的平衡常数为________ ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为________ mol·L-1。
②下列措施中能使平衡时 增大的是
增大的是________ (填字母)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
 FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:| 700 ℃ | 900 ℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
 CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=
CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=②能判断CO2(g)+H2(g)
 CO(g)+H2O(g)达到化学平衡状态的依据是
CO(g)+H2O(g)达到化学平衡状态的依据是A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
①该条件下反应的平衡常数为
②下列措施中能使平衡时
 增大的是
增大的是A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)在一定条件下,xA+yB zC的反应达到平衡。
zC的反应达到平衡。
①已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是________ ;
②已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则平衡一定向______ (填“正反应方向”或“逆反应方向”)移动;
③若加热后C的质量分数减少,则正反应是_______ (填“放热”或“吸热”)反应。
(2)二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。硫酸生产中,SO2催化氧化生成SO3的原理为:2SO2(g)+O2(g)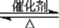 2SO3(g)。某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。
2SO3(g)。某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。
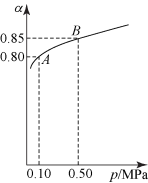
根据图示回答下列问题:平衡状态由A变到B时,平衡常数K(A)_______ K(B)(填“>”、“<”或“=”)。
 zC的反应达到平衡。
zC的反应达到平衡。①已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是
②已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则平衡一定向
③若加热后C的质量分数减少,则正反应是
(2)二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。硫酸生产中,SO2催化氧化生成SO3的原理为:2SO2(g)+O2(g)
 2SO3(g)。某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。
2SO3(g)。某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。
根据图示回答下列问题:平衡状态由A变到B时,平衡常数K(A)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】 是一种很好的消毒剂,具有高效、洁净、方便、经济等优点,
是一种很好的消毒剂,具有高效、洁净、方便、经济等优点, 可溶于水,在水中易分解,产生的
可溶于水,在水中易分解,产生的 为游离氧原子,有很强的杀菌消毒能力,能杀灭新冠肺炎病毒。已知常温常压下发生的反应如下:
为游离氧原子,有很强的杀菌消毒能力,能杀灭新冠肺炎病毒。已知常温常压下发生的反应如下:
反应① ,平衡常数为
,平衡常数为 (反应进行的程度较小)
(反应进行的程度较小)
反应② ,平衡常数为
,平衡常数为 (反应进行的程度较大)
(反应进行的程度较大)
总反应: ,平衡常数为
,平衡常数为
(1)你能比较 和
和 的大小吗?
的大小吗? _______
(2)降低压强,总反应平衡向哪个方向移动?此时 如何变化?
如何变化? _______
(3)升高温度, 如何变化?
如何变化? _______
(4) 与
与 有何数量关系?
有何数量关系? _______
 是一种很好的消毒剂,具有高效、洁净、方便、经济等优点,
是一种很好的消毒剂,具有高效、洁净、方便、经济等优点, 可溶于水,在水中易分解,产生的
可溶于水,在水中易分解,产生的 为游离氧原子,有很强的杀菌消毒能力,能杀灭新冠肺炎病毒。已知常温常压下发生的反应如下:
为游离氧原子,有很强的杀菌消毒能力,能杀灭新冠肺炎病毒。已知常温常压下发生的反应如下:反应①
 ,平衡常数为
,平衡常数为 (反应进行的程度较小)
(反应进行的程度较小)反应②
 ,平衡常数为
,平衡常数为 (反应进行的程度较大)
(反应进行的程度较大)总反应:
 ,平衡常数为
,平衡常数为
(1)你能比较
 和
和 的大小吗?
的大小吗? (2)降低压强,总反应平衡向哪个方向移动?此时
 如何变化?
如何变化? (3)升高温度,
 如何变化?
如何变化? (4)
 与
与 有何数量关系?
有何数量关系?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】 已知3A(g)+B(g)⇌xC(g)+2D(g),将等物质的量的A、B混合于2 L的密闭容器中,经5 min后达到化学平衡,此时测得D的浓度为0.5 mol/L,且c(A)∶c(B)=3∶5.又知5 min 内用C表示的平均反应速率为0.1 mol/(L·min)。求:
(1)反应开始前容器中的A、B的物质的量:n(A)=n(B)=______ mol;
(2)5min内用B表示的平均反应速率v(B)=______ mol/(L·min);
(3)此时A的转化率为______ ,x的值为______ 。
(1)反应开始前容器中的A、B的物质的量:n(A)=n(B)=
(2)5min内用B表示的平均反应速率v(B)=
(3)此时A的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在体积为1 L的恒温密闭容器中,充入1 mol  和3 mol
和3 mol  ,一定条件下反应:
,一定条件下反应: ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
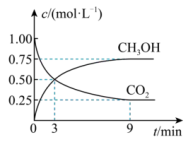
(1)从3 min到9 min,
_______  。
。
(2)第4 min时,正、逆反应速率的大小关系为
_______ (填“>”“<”“=”) 。
。
(3)平衡时 的转化率为
的转化率为_______ 。
(4)反应达到平衡,此时体系内压强与开始时的压强之比为_______ 。
 和3 mol
和3 mol  ,一定条件下反应:
,一定条件下反应: ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
(1)从3 min到9 min,

 。
。(2)第4 min时,正、逆反应速率的大小关系为

 。
。(3)平衡时
 的转化率为
的转化率为(4)反应达到平衡,此时体系内压强与开始时的压强之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】994 K,当H2缓慢通过过量的块状固体CoO时,部分CoO被还原为固体Co。在流出的平衡气体中H2的物质的量分数为2.50%; 在同一温度,若用CO还原固体CoO时平衡气体中CO的物质的量分数为1.92%。 如果994 K时物质的量比为1:2的一氧化碳和水蒸气的混合物在一定条件下反应,问:
(1)一氧化碳的平衡转化率大约是多少___________ ?
(2)欲获得较纯的H2,请简要说明在生产工艺上应采取的措施___________ 。
(3)994 K,当H2缓慢通过过量的纳米CoO固体粉末时,部分CoO被还原为固体Co。在相同的反应时间内,与块状固体CoO相比,采用纳米固体CoO时流出的平衡气体中H2的物质的量分数将怎样变化___________ ?为什么___________ ?
(1)一氧化碳的平衡转化率大约是多少
(2)欲获得较纯的H2,请简要说明在生产工艺上应采取的措施
(3)994 K,当H2缓慢通过过量的纳米CoO固体粉末时,部分CoO被还原为固体Co。在相同的反应时间内,与块状固体CoO相比,采用纳米固体CoO时流出的平衡气体中H2的物质的量分数将怎样变化
您最近一年使用:0次



