北京冬奥会上采用二氧化碳跨临界制冰,使人们再次看到了二氧化碳综合化利用的巨大前景。
(1)国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2 (g) +4H2(g) CH4(g)+2H2O(g) △H
CH4(g)+2H2O(g) △H
①已知H2的燃烧热△H1= - 285. 8 kJ·mol-1,CH4的燃烧热△H2= - 890.3 kJ·mol-1,H2O(g)=H2O(l) △H3= -44 kJ·mol-1,则上述反应的△H=_______ kJ·mol-1。
②相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
a、b、c、d与m、n、x、y之间的关系式为_______ 。
(2)二氧化碳加氢合成甲醇是人工合成淀粉的重要步骤之一,涉及的主要反应如下:
I.CO2(g) + 3H2(g) CH3OH(g)+ H2O(g) △H= -49.5 kJ·mol-1
CH3OH(g)+ H2O(g) △H= -49.5 kJ·mol-1
II.CO(g) +2H2 (g) CH3OH(g) △H= -90.4 kJ·mol-1
CH3OH(g) △H= -90.4 kJ·mol-1
III.CO2(g)+ H2(g) CO(g)+ H2O(g) △H=+40.9 kJ·mol-1
CO(g)+ H2O(g) △H=+40.9 kJ·mol-1
①设 为相对压力平衡常数,是用相对分压(气体分压除以100kPa)代替浓度计算的平衡常数。如下图为反应
为相对压力平衡常数,是用相对分压(气体分压除以100kPa)代替浓度计算的平衡常数。如下图为反应_______ (填“II”或“III”)的lg 随示
随示 (n>m)的变化关系。
(n>m)的变化关系。
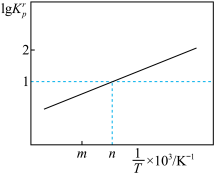
②在上图中n点对应温度下、原料组成为n(CO2): n(H2)=1:3、初始总压为100 kPa的恒容密闭容器中进行反应,体系达到平衡时CO的分压为10kPa,CH3OH的分压为9kPa,H2的平衡转化率为_______ 。
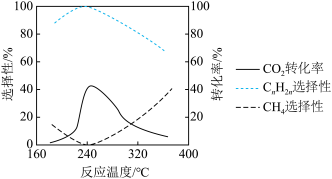
(3)在催化剂的作用下,二氧化碳还可以和氢气发生反应生成甲烷和低级烯烃CnH2n(n=2~4)。其它条件一定时,反应温度对CO2转化率CH4选择性、CnH2n选择性的影响如图所示,从生产低级烯烃的角度考虑,最合适的反应温度是_______ 。资料显示原料气中 >1时,随着
>1时,随着 的增大,低级烯烃的选择性会逐渐降低,但氢气的总转化率不发生明显变化,原因可能是
的增大,低级烯烃的选择性会逐渐降低,但氢气的总转化率不发生明显变化,原因可能是_______ 。
(1)国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2 (g) +4H2(g)
 CH4(g)+2H2O(g) △H
CH4(g)+2H2O(g) △H①已知H2的燃烧热△H1= - 285. 8 kJ·mol-1,CH4的燃烧热△H2= - 890.3 kJ·mol-1,H2O(g)=H2O(l) △H3= -44 kJ·mol-1,则上述反应的△H=
②相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
| c(CO2)/mol·L-1 | c(H2)/ mol·L-1 | c(CH4)/ mol·L-1 | c(H2O)/ mol·L-1 | |
| 平衡I | a | b | c | d |
| 平衡II | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为
(2)二氧化碳加氢合成甲醇是人工合成淀粉的重要步骤之一,涉及的主要反应如下:
I.CO2(g) + 3H2(g)
 CH3OH(g)+ H2O(g) △H= -49.5 kJ·mol-1
CH3OH(g)+ H2O(g) △H= -49.5 kJ·mol-1II.CO(g) +2H2 (g)
 CH3OH(g) △H= -90.4 kJ·mol-1
CH3OH(g) △H= -90.4 kJ·mol-1III.CO2(g)+ H2(g)
 CO(g)+ H2O(g) △H=+40.9 kJ·mol-1
CO(g)+ H2O(g) △H=+40.9 kJ·mol-1①设
 为相对压力平衡常数,是用相对分压(气体分压除以100kPa)代替浓度计算的平衡常数。如下图为反应
为相对压力平衡常数,是用相对分压(气体分压除以100kPa)代替浓度计算的平衡常数。如下图为反应 随示
随示 (n>m)的变化关系。
(n>m)的变化关系。
②在上图中n点对应温度下、原料组成为n(CO2): n(H2)=1:3、初始总压为100 kPa的恒容密闭容器中进行反应,体系达到平衡时CO的分压为10kPa,CH3OH的分压为9kPa,H2的平衡转化率为
(3)在催化剂的作用下,二氧化碳还可以和氢气发生反应生成甲烷和低级烯烃CnH2n(n=2~4)。其它条件一定时,反应温度对CO2转化率CH4选择性、CnH2n选择性的影响如图所示,从生产低级烯烃的角度考虑,最合适的反应温度是
 >1时,随着
>1时,随着 的增大,低级烯烃的选择性会逐渐降低,但氢气的总转化率不发生明显变化,原因可能是
的增大,低级烯烃的选择性会逐渐降低,但氢气的总转化率不发生明显变化,原因可能是
更新时间:2022-11-21 23:28:58
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】每到冬季,雾霾天气肆虐京津冀等地区。其中,燃煤和汽车尾气是造成空气污染的原因之一。
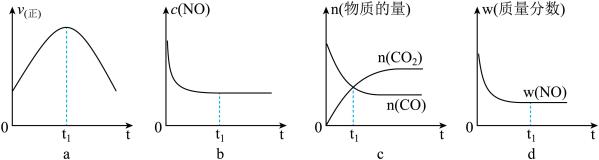
(l)汽车尾气净化的主要原理为:2NO(g)+2CO(g) 2CO2(g)+N2(g)△H<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是
2CO2(g)+N2(g)△H<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________________ (填代号)。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol ①
2NO2(g)⇌N2O4(g) △H=-56.9 kJ/mol ②
H2O(g)=H2O(l) △H=-44.0 kJ/mol ③
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式__________________ 。
(3)甲烷燃料电池可以提升能量利用率。
①碱性介质中甲烷燃料电池的负极反应式_________________________ 。
②如果电路上有0.1mol电子通过,理论上消耗标准状况下氧气的体积为_______ 。
(4)已知燃料电池的比能量与单位质量的燃料失去的电子数成正比。理论上,氢气、甲烷、甲醇燃料电池的比能量从大到小的顺序是_________ 。
(l)汽车尾气净化的主要原理为:2NO(g)+2CO(g)
 2CO2(g)+N2(g)△H<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是
2CO2(g)+N2(g)△H<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol ①
2NO2(g)⇌N2O4(g) △H=-56.9 kJ/mol ②
H2O(g)=H2O(l) △H=-44.0 kJ/mol ③
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式
(3)甲烷燃料电池可以提升能量利用率。
①碱性介质中甲烷燃料电池的负极反应式
②如果电路上有0.1mol电子通过,理论上消耗标准状况下氧气的体积为
(4)已知燃料电池的比能量与单位质量的燃料失去的电子数成正比。理论上,氢气、甲烷、甲醇燃料电池的比能量从大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】氮的氧化物的催化还原是环保研究热点。
(1)常在催化条件下用 还原
还原 来消除氮氧化物的污染。已知:a、b都大于0。
来消除氮氧化物的污染。已知:a、b都大于0。
①
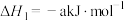
②



___________  (用含a、b的代数式表示)
(用含a、b的代数式表示)
(2)铜还原NO生成 可将NO转化为无污染物质:
可将NO转化为无污染物质:
 。向恒容密闭容器中充入NO和足量Cu,发生上述反应。
。向恒容密闭容器中充入NO和足量Cu,发生上述反应。
①达到平衡后,升高温度,NO的正反应速率___________ (填“大于”“小于”或“等于”)NO的逆反应速率。
②达到平衡后,增大Cu的质量,平衡___________ (填“向左”“向右”或“不”)移动。
(3)CO还原NO的反应为
 。向体积均为
。向体积均为 的甲、乙两个恒容密闭容器中分别充入
的甲、乙两个恒容密闭容器中分别充入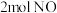 和
和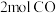 ,分别在绝热、恒温条件下发生上述反应。两反应体系中的压强随时间的变化曲线如图所示。
,分别在绝热、恒温条件下发生上述反应。两反应体系中的压强随时间的变化曲线如图所示。

①
___________ 0(填“>”“<”或“=”)。乙容器在___________ (填“绝热”或“恒温”)条件下进行。
②CO的转化率:a___________ b(填“>”“<”或“=”),判断依据是___________ 。
③a点
___________ 。b点平衡常数K___________ a点浓度商Q(填“>”“<”或“=”)。
(1)常在催化条件下用
 还原
还原 来消除氮氧化物的污染。已知:a、b都大于0。
来消除氮氧化物的污染。已知:a、b都大于0。①

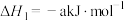
②




 (用含a、b的代数式表示)
(用含a、b的代数式表示)(2)铜还原NO生成
 可将NO转化为无污染物质:
可将NO转化为无污染物质:
 。向恒容密闭容器中充入NO和足量Cu,发生上述反应。
。向恒容密闭容器中充入NO和足量Cu,发生上述反应。①达到平衡后,升高温度,NO的正反应速率
②达到平衡后,增大Cu的质量,平衡
(3)CO还原NO的反应为

 。向体积均为
。向体积均为 的甲、乙两个恒容密闭容器中分别充入
的甲、乙两个恒容密闭容器中分别充入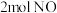 和
和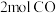 ,分别在绝热、恒温条件下发生上述反应。两反应体系中的压强随时间的变化曲线如图所示。
,分别在绝热、恒温条件下发生上述反应。两反应体系中的压强随时间的变化曲线如图所示。
①

②CO的转化率:a
③a点

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】(Ⅰ)丙烷是一种优良的燃料。试回答下列问题:
(1)已知丙烷完全燃烧生成CO2和1 mol H2O(l)放出553.75kJ的热量,写出表示丙烷标准燃烧热的热化学方程式:_____________ 。
(2)二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol 二甲醚完全燃烧生成CO2和液态水放出1 455 kJ的热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1 645 kJ的热量,则混合气体中,丙烷和二甲醚的物质的量之比为________ 。
(Ⅱ)CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式为:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活,甲烷细菌使1 mol甲烷生成CO2气体与液态水,放出的能量____________ (填“>”“<”或“=”)890.3 kJ。
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2=2CO+2H2,1 g CH4完全反应可释放15.46 kJ的热量,则:
①能表示该反应过程中能量变化的是____________ (填字母)。

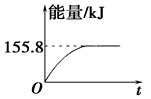
②若将物质的量均为1 mol的CH4与CO2充入某恒容密闭容器中,体系放出的热量随着时间的变化如图所示,则CH4的转化率为____________ (用小数表示,保留2位小数)。
(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)=CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)=CH4(g) 的反应热ΔH=____________ 。
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是_______________ (填字母)。
A.寻找优质催化剂,使CO2与H2O反应生成CH4与O2,并放出热量
B.寻找优质催化剂,在常温常压下使CO2分解生成碳与O2
C.寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2)
D.将固态碳合成为C60,以C60作为燃料
(1)已知丙烷完全燃烧生成CO2和1 mol H2O(l)放出553.75kJ的热量,写出表示丙烷标准燃烧热的热化学方程式:
(2)二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol 二甲醚完全燃烧生成CO2和液态水放出1 455 kJ的热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1 645 kJ的热量,则混合气体中,丙烷和二甲醚的物质的量之比为
(Ⅱ)CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式为:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活,甲烷细菌使1 mol甲烷生成CO2气体与液态水,放出的能量
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2=2CO+2H2,1 g CH4完全反应可释放15.46 kJ的热量,则:
①能表示该反应过程中能量变化的是

②若将物质的量均为1 mol的CH4与CO2充入某恒容密闭容器中,体系放出的热量随着时间的变化如图所示,则CH4的转化率为

(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)=CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)=CH4(g) 的反应热ΔH=
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是
A.寻找优质催化剂,使CO2与H2O反应生成CH4与O2,并放出热量
B.寻找优质催化剂,在常温常压下使CO2分解生成碳与O2
C.寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2)
D.将固态碳合成为C60,以C60作为燃料
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】碳、硫氧化物的综合利用是目前研究的热点之一。已知:
Ⅰ.2SO2(g)+O2(g) 2SO3(g)△H1=-196.6kJ•mol-1
2SO3(g)△H1=-196.6kJ•mol-1
Ⅱ.C(s)+2H2O(g) CO2(g)+2H2(g)△H2=+90.1kJ•mol-1
CO2(g)+2H2(g)△H2=+90.1kJ•mol-1
Ⅲ.2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ•mol-1
回答下列问题:
(1) 2SO2(g)+C(s)+2O2(g) 2SO3(g)+CO2(g)△H=
2SO3(g)+CO2(g)△H=___ 。
(2)研究发现细小炭粒能将O2转化为活性氧而加快SO2的氧化速率,在干燥和潮湿两种环境中的反应历程如图1所示。
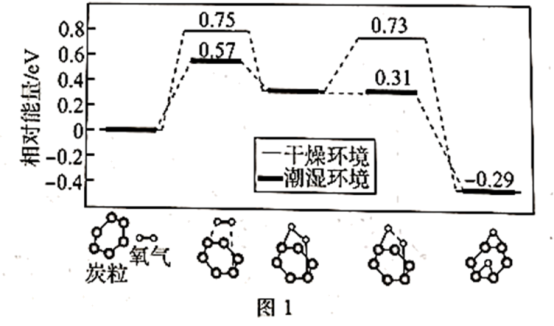
①活化氧的过程适宜在___ (填“干燥”或“潮湿”)环境中进行,理由为___ 。
②反应Ⅰ的速率方程为v=kp-1(SO2)p(O2)(k为与温度有关的常数)。一定可以加快反应Ⅰ速率的措施有__ (答出一点即可)。
(3)一定温度下,向起始容积为5L的恒压密闭容器中加入2molC(s)和2molH2O(g),发生反应Ⅱ。实验测得CO2的平衡物质的量为0.6mol。

①H2O(g)的平衡转化率为__ 。
②反应的平衡常数Kc=__ (保留两位有效数字)。
③H2O(g)的平衡转化率与温度、压强的关系如图2所示。则x表示的物理量为_ (填“温度”或“压强”);y1__ y2(填“>”或“<”)。
Ⅰ.2SO2(g)+O2(g)
 2SO3(g)△H1=-196.6kJ•mol-1
2SO3(g)△H1=-196.6kJ•mol-1Ⅱ.C(s)+2H2O(g)
 CO2(g)+2H2(g)△H2=+90.1kJ•mol-1
CO2(g)+2H2(g)△H2=+90.1kJ•mol-1Ⅲ.2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ•mol-1
回答下列问题:
(1) 2SO2(g)+C(s)+2O2(g)
 2SO3(g)+CO2(g)△H=
2SO3(g)+CO2(g)△H=(2)研究发现细小炭粒能将O2转化为活性氧而加快SO2的氧化速率,在干燥和潮湿两种环境中的反应历程如图1所示。

①活化氧的过程适宜在
②反应Ⅰ的速率方程为v=kp-1(SO2)p(O2)(k为与温度有关的常数)。一定可以加快反应Ⅰ速率的措施有
(3)一定温度下,向起始容积为5L的恒压密闭容器中加入2molC(s)和2molH2O(g),发生反应Ⅱ。实验测得CO2的平衡物质的量为0.6mol。

①H2O(g)的平衡转化率为
②反应的平衡常数Kc=
③H2O(g)的平衡转化率与温度、压强的关系如图2所示。则x表示的物理量为
您最近一年使用:0次
【推荐2】硅是信息产业、太阳能电池光电转化的基础材料。
(1)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
硅与碳同族,但硅烷在种类和数量上都远不如烷烃多,原因是_______ 。
(2)锌还原四氯化硅是一种有着良好应用前景的制备硅的方法。 还原
还原 的反应如下:
的反应如下:
反应1: ,
,
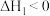
反应2: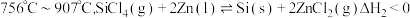
反应3: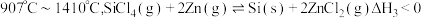
①对于上述三个反应,下列说法合理的是_______ 。
a.升高温度会提高 的转化率 b.还原过程需在无氧的气氛中进行
的转化率 b.还原过程需在无氧的气氛中进行
c.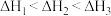 d.Na、Mg可以代替
d.Na、Mg可以代替 还原
还原
②实际制备过程选择“反应3”,选择的理由是_______ 。
(3)工业上也可用 制备高纯硅。
制备高纯硅。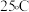 时,
时, 相关反应的热化学方程式和平衡常数如表:
相关反应的热化学方程式和平衡常数如表:
①则该温度下, =
= _______________  ;K3=
;K3=_______ (用K1和K2表示)。
②对于反应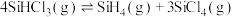 ,采用大孔弱碱性阴离子交换树脂催化剂,在
,采用大孔弱碱性阴离子交换树脂催化剂,在 和
和 时
时 的转化率随时间变化的结果如图所示。则T1
的转化率随时间变化的结果如图所示。则T1_____________ T2(填“大于”“小于”或“等于”), 时平衡常数K=
时平衡常数K=_______ (保留2位小数)。 下,要提高
下,要提高 转化率,可采取的措施是
转化率,可采取的措施是_______ 。
(1)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 |  |  |  |  |
键能 | 356 | 413 | 226 | 318 |
(2)锌还原四氯化硅是一种有着良好应用前景的制备硅的方法。
 还原
还原 的反应如下:
的反应如下:反应1:
 ,
,
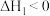
反应2:
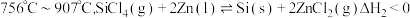
反应3:
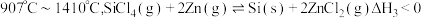
①对于上述三个反应,下列说法合理的是
a.升高温度会提高
 的转化率 b.还原过程需在无氧的气氛中进行
的转化率 b.还原过程需在无氧的气氛中进行c.
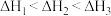 d.Na、Mg可以代替
d.Na、Mg可以代替 还原
还原
②实际制备过程选择“反应3”,选择的理由是
(3)工业上也可用
 制备高纯硅。
制备高纯硅。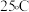 时,
时, 相关反应的热化学方程式和平衡常数如表:
相关反应的热化学方程式和平衡常数如表:| 热化学方程式 | 平衡常数 |
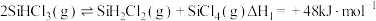 | K1 |
 | K2 |
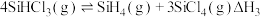 | K3 |
 =
=  ;K3=
;K3=②对于反应
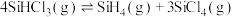 ,采用大孔弱碱性阴离子交换树脂催化剂,在
,采用大孔弱碱性阴离子交换树脂催化剂,在 和
和 时
时 的转化率随时间变化的结果如图所示。则T1
的转化率随时间变化的结果如图所示。则T1 时平衡常数K=
时平衡常数K=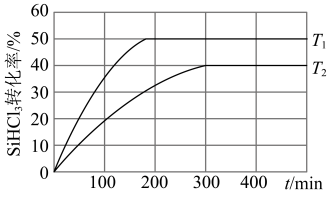
 下,要提高
下,要提高 转化率,可采取的措施是
转化率,可采取的措施是
您最近一年使用:0次
【推荐3】合成气是一种重要的化工原料气,可以合成甲醇、甲酸甲酯、二甲醚等化工产品。
I.甲烷、二氧化碳自热重整制取合成气的反应如下:
①CH4(g) +CO2(g) 2CO(g) +2H2(g) ∆H 1=+250kJ· mol-1
2CO(g) +2H2(g) ∆H 1=+250kJ· mol-1
②CH4(g)+H2O(g) CO(g)+3H2(g) ∆H2>0
CO(g)+3H2(g) ∆H2>0
③CO2(g) +H2(g) CO(g)+H2O(g) ∆H3
CO(g)+H2O(g) ∆H3
(1)反应①的正反应活化能为Ea kJ· mol-1,则逆反应的活化能为_______ kJ·mol-1
(2)不同温度下,向VL密闭容器中按照n(CO2) :n(CH4) :n(H2O)=1:1:1投料,实验测得平衡时n(H2):n(CO)随温度的变化关系如图所示:
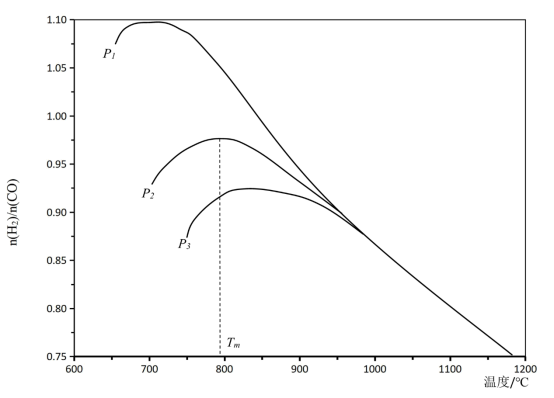
①压强P1、P2、P3由大到小的顺序为_______ 。
②压强为P2时,随着温度升高,n(H2) : n(CO)先增大后减小,可推测∆H_______ 0 (填“>”或“<”),判断依据是_______
II.利用合成气制取甲醇:
(3)在容积为1L的密闭容器中加入1mol CO2和1.4mol H2,在催化剂的作用下,发生反应如下:
④CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H
CH3OH(g)+H2O(g) ∆H
⑤CO2(g)+H2(g) CO(g)+H2O(g) ∆H
CO(g)+H2O(g) ∆H
10min后体系达到平衡,此时CO2的转化率为20%,CH3OH的选择性[CH3OH 的选择性=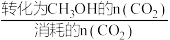 ×100%] 为50%,则反应④的平衡常数K=
×100%] 为50%,则反应④的平衡常数K=_______ 。
III.某甲醇燃料电池的工作原理如图所示,质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol/LH2SO4溶液。

(4)a极的电极反应式为_______ 当导线中有6mol e- 发生转移时,左右两侧溶液的质量差为_______ g ( 假设反应物耗尽,忽略气体的溶解)。
I.甲烷、二氧化碳自热重整制取合成气的反应如下:
①CH4(g) +CO2(g)
 2CO(g) +2H2(g) ∆H 1=+250kJ· mol-1
2CO(g) +2H2(g) ∆H 1=+250kJ· mol-1②CH4(g)+H2O(g)
 CO(g)+3H2(g) ∆H2>0
CO(g)+3H2(g) ∆H2>0③CO2(g) +H2(g)
 CO(g)+H2O(g) ∆H3
CO(g)+H2O(g) ∆H3(1)反应①的正反应活化能为Ea kJ· mol-1,则逆反应的活化能为
(2)不同温度下,向VL密闭容器中按照n(CO2) :n(CH4) :n(H2O)=1:1:1投料,实验测得平衡时n(H2):n(CO)随温度的变化关系如图所示:

①压强P1、P2、P3由大到小的顺序为
②压强为P2时,随着温度升高,n(H2) : n(CO)先增大后减小,可推测∆H
II.利用合成气制取甲醇:
(3)在容积为1L的密闭容器中加入1mol CO2和1.4mol H2,在催化剂的作用下,发生反应如下:
④CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H
CH3OH(g)+H2O(g) ∆H⑤CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H
CO(g)+H2O(g) ∆H10min后体系达到平衡,此时CO2的转化率为20%,CH3OH的选择性[CH3OH 的选择性=
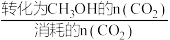 ×100%] 为50%,则反应④的平衡常数K=
×100%] 为50%,则反应④的平衡常数K=III.某甲醇燃料电池的工作原理如图所示,质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol/LH2SO4溶液。

(4)a极的电极反应式为
您最近一年使用:0次
【推荐1】用活性炭还原法处理氮氧化物,有关反应为C(s)+2NO(g) N2(g)+CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1 ℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
N2(g)+CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1 ℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
(1)10~20 min的时间段内,以CO2表示的反应速率为____________ 。
(2)写出该反应的平衡常数的表达式K=_________ 。
(3)下列各项能作为判断该反应达到平衡状态的是 。(填序号字母)
(4)30 min时改变某一条件,反应重新达到平衡,则改变的条件可能是_____________ 。
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率______ (填“增大”“不变”或“减小”)。
 N2(g)+CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1 ℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
N2(g)+CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1 ℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:物 质 浓度/mol·L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
(2)写出该反应的平衡常数的表达式K=
(3)下列各项能作为判断该反应达到平衡状态的是 。(填序号字母)
| A.容器内压强保持不变 |
| B.2v正(NO)=v逆(N2) |
| C.容器内CO2的体积分数不变 |
| D.混合气体的密度保持不变 |
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】I.依据题中所给信息完成指定问题:
(1)地康法制氯气可按下列催化过程进行:
CuCl2(s)=CuCl(s)+ Cl2(g) ΔH1=+83kJ•mol-1
Cl2(g) ΔH1=+83kJ•mol-1
CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=-20kJ•mol-1
Cl2(g) ΔH2=-20kJ•mol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121kJ•mol-1
则反应4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=________ kJ•mol-1。
(2)用50mL0.50mol•L-1盐酸和50mL0.55mol•L-1NaOH溶液反应测定中和热,实验中测得起始平均温度为20.4℃,反应后最高温度为23.4℃,反应后溶液的比热容为4.2J•g-1•℃-1,盐酸和NaOH溶液的密度都近似认为是1g•cm-3,则中和热ΔH=________ 。
II.Cu2O与ZnO组成的催化剂可用于工业上合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH=akJ•mol-1。按n(H2)/n(CO)=2将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g) ΔH=akJ•mol-1。按n(H2)/n(CO)=2将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如图所示。
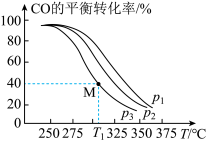
(3)该反应的ΔH________ (填“<”或“>”)0,图中p1、p2、p3由大到小的顺序是________ 。
(4)起始时,甲容器中c(H2)=0.20mol•L-1,c(CO)=0.10mol•L-1,在p3及T1℃下反应达到平衡,此时反应的平衡常数为________ 。起始时,乙容器中c(H2)=0.40mol•L-1,c(CO)=0.20mol•L-1,T1℃下反应达到平衡,CO的平衡转化率________ 。
A.大于40% B.小于40% C.等于40% D.等于80%
(1)地康法制氯气可按下列催化过程进行:
CuCl2(s)=CuCl(s)+
 Cl2(g) ΔH1=+83kJ•mol-1
Cl2(g) ΔH1=+83kJ•mol-1CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=-20kJ•mol-1
Cl2(g) ΔH2=-20kJ•mol-1CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121kJ•mol-1
则反应4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=
(2)用50mL0.50mol•L-1盐酸和50mL0.55mol•L-1NaOH溶液反应测定中和热,实验中测得起始平均温度为20.4℃,反应后最高温度为23.4℃,反应后溶液的比热容为4.2J•g-1•℃-1,盐酸和NaOH溶液的密度都近似认为是1g•cm-3,则中和热ΔH=
II.Cu2O与ZnO组成的催化剂可用于工业上合成甲醇:CO(g)+2H2(g)
 CH3OH(g) ΔH=akJ•mol-1。按n(H2)/n(CO)=2将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g) ΔH=akJ•mol-1。按n(H2)/n(CO)=2将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如图所示。
(3)该反应的ΔH
(4)起始时,甲容器中c(H2)=0.20mol•L-1,c(CO)=0.10mol•L-1,在p3及T1℃下反应达到平衡,此时反应的平衡常数为
A.大于40% B.小于40% C.等于40% D.等于80%
您最近一年使用:0次
【推荐3】我国力争2030年前实现碳达峰,2060年前实现碳中和。CO2的综合利用是实现碳中和的措施之一。
Ⅰ.CO2和CH4在催化剂表面可以合成CH3COOH,该反应势能图如下(*指微粒吸附在催化剂表面,H#指H吸附在催化剂载体上的氧原子上,TS表示过渡态):

(1)写出控速步的基元反应:_______________________________
(2)下列说法正确的有___________ 。
a.增大催化剂表面积可提高CO2在催化剂表面的吸附速率
b.从图中可看出催化效果更好的是催化剂2
c.从图中可看出CH3COOH(g)*比CH3COOH(g)能量低
d.使用高活性催化剂可降低反应焓变,加快反应速率
Ⅱ.CO2和H2一定条件下也可以合成甲醇,该过程存在副反应二。
反应一:CO2(g) + 3H2(g) CH3OH(g) + H2O(g) △H1 = - 49.3kJ/mol
CH3OH(g) + H2O(g) △H1 = - 49.3kJ/mol
反应二:CO2(g) + H2(g) CO(g) + H2O(g) △H2
CO(g) + H2O(g) △H2
(3)已知25℃和101kPa下,H2(g)、CO(g)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1,H2O(l)= H2O(g) △H=+44kJ•mol-1,则△H2=_______ kJ/mol。
(4)在某密闭容器中充入n(CO2):n(H2)=5:17的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。
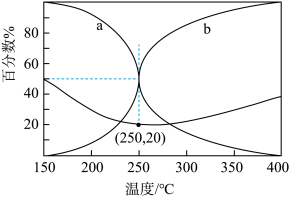
①表示平衡时 CH3OH在含碳产物中物质的量百分数的曲线是_________ (填“a”或“b”)。
②CO2平衡转化率随温度的升高先减小后增大,增大的原因可能是_______ 。
③250℃时副反应CO2(g)+H2(g) CO(g)+H2O(g)的Kp=
CO(g)+H2O(g)的Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
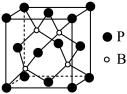
(5)我国科学家研究出一种磷化硼纳米颗粒作为高选择性CO2 电化学还原为甲醇的非金属电催化剂,磷化硼结构与金刚石结构相似,其晶胞如图所示。其中磷化硼晶体中“普通共价键”与配位键的数目之比___________ ;已知阿伏加德罗常数的值为NA,晶胞参数为a pm,则磷化硼晶体的密度为_________ g·pm−3(结果用含a、NA的最简分数表达式表示)。
Ⅰ.CO2和CH4在催化剂表面可以合成CH3COOH,该反应势能图如下(*指微粒吸附在催化剂表面,H#指H吸附在催化剂载体上的氧原子上,TS表示过渡态):

(1)写出控速步的基元反应:
(2)下列说法正确的有
a.增大催化剂表面积可提高CO2在催化剂表面的吸附速率
b.从图中可看出催化效果更好的是催化剂2
c.从图中可看出CH3COOH(g)*比CH3COOH(g)能量低
d.使用高活性催化剂可降低反应焓变,加快反应速率
Ⅱ.CO2和H2一定条件下也可以合成甲醇,该过程存在副反应二。
反应一:CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) △H1 = - 49.3kJ/mol
CH3OH(g) + H2O(g) △H1 = - 49.3kJ/mol反应二:CO2(g) + H2(g)
 CO(g) + H2O(g) △H2
CO(g) + H2O(g) △H2(3)已知25℃和101kPa下,H2(g)、CO(g)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1,H2O(l)= H2O(g) △H=+44kJ•mol-1,则△H2=
(4)在某密闭容器中充入n(CO2):n(H2)=5:17的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。

①表示平衡时 CH3OH在含碳产物中物质的量百分数的曲线是
②CO2平衡转化率随温度的升高先减小后增大,增大的原因可能是
③250℃时副反应CO2(g)+H2(g)
 CO(g)+H2O(g)的Kp=
CO(g)+H2O(g)的Kp=(5)我国科学家研究出一种磷化硼纳米颗粒作为高选择性CO2 电化学还原为甲醇的非金属电催化剂,磷化硼结构与金刚石结构相似,其晶胞如图所示。其中磷化硼晶体中“普通共价键”与配位键的数目之比

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氢气是一种重要的工业原料和清洁能源,可用作合成氨、合成甲醇、合成盐酸的原料,冶金用还原剂等。
(1)工业合成氨的反应原理为N2(g)+3H2(g) 2NH3(g) ΔH=−92.4 kJ·mol−1。
2NH3(g) ΔH=−92.4 kJ·mol−1。
①该反应中的H2制取成本较高,工业生产中往往追求H2的转化率。增大H2的平衡转化率的措施有______________ (填字母代号)。
a.增大压强 b.升高温度 c.增大N2浓度
d.及时移走生成物NH3 e.使用高效催化剂
②某温度下,把10 mol N2与28 mol H2置于容积为10 L的恒容密闭容器内,10 min时反应达到平衡状态,测得平均速率v(NH3)=0.12 mol·L−1·min−1,H2的平衡转化率为______________ (保留三位有效数字),则该温度下反应的平衡常数K=_______________ 。
(2)为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:
2CO(g)+O2(g)═2CO2(g) △H=﹣566 kJ·mol-1
2H2(g)+O2(g)═2H2O(g) △H=﹣483.6 kJ·mol-1
H2O(g)═H2O(l) △H=﹣44.0 kJ·mol-1
①1 mol氢气生成液态水放出的热量为_________ kJ。
②写出CO和H2O(g)作用生成CO2和H2的热化学方程式_________ 。
(1)工业合成氨的反应原理为N2(g)+3H2(g)
 2NH3(g) ΔH=−92.4 kJ·mol−1。
2NH3(g) ΔH=−92.4 kJ·mol−1。①该反应中的H2制取成本较高,工业生产中往往追求H2的转化率。增大H2的平衡转化率的措施有
a.增大压强 b.升高温度 c.增大N2浓度
d.及时移走生成物NH3 e.使用高效催化剂
②某温度下,把10 mol N2与28 mol H2置于容积为10 L的恒容密闭容器内,10 min时反应达到平衡状态,测得平均速率v(NH3)=0.12 mol·L−1·min−1,H2的平衡转化率为
(2)为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:
2CO(g)+O2(g)═2CO2(g) △H=﹣566 kJ·mol-1
2H2(g)+O2(g)═2H2O(g) △H=﹣483.6 kJ·mol-1
H2O(g)═H2O(l) △H=﹣44.0 kJ·mol-1
①1 mol氢气生成液态水放出的热量为
②写出CO和H2O(g)作用生成CO2和H2的热化学方程式
您最近一年使用:0次
【推荐2】将煤炭转化为烯烃(乙烯、丙烯等)既可以减少CO2的排放,又可以制备重要的化工原料。该过程先转化为二甲醚CH3OCH3,再转化为烯烃。
(1)制备二甲醚的主要反应:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ: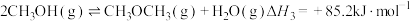
①“反应Ⅰ”能自发进行的条件是_______ (填“高温”“低温”或“任意温度”)。
②某反应X的平衡常数表达式为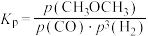 ,则反应X的热化学方程式为
,则反应X的热化学方程式为_______ 。
(2)二甲醚制备烯烃的主要反应:
反应Ⅳ:
反应Ⅴ: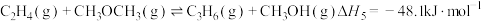
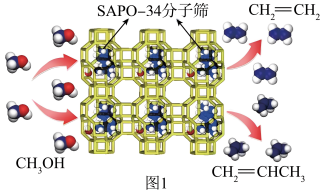
①该反应过程常用的催化剂有两种,ZSM-5以及SAPO-34,它们都是多孔笼状结构,ZSM-5笼状孔径约为0.55nm,SAPO-34约为0.4nm。相同条件下,催化剂SAPO-34反应(如图1)获得的产物中,n(C2H4):n(C3H6)更大的原因是_______ 。
②一定温度下,在体积为1L的密闭容器中投入2mol CH3OCH3发生“反应Ⅳ”和“反应Ⅴ”,初始总压为po,反应到达平衡时总压为1.2po,且n(C2H4):n(C3H6)=1:1。则平衡时体系CH3OCH3转化率α(CH3OCH3)=_______ 。“反应Ⅴ”的平衡常数Kp=_______ 。
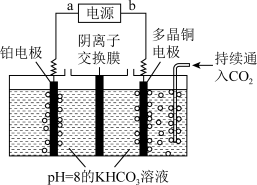
(3)用下图装置电解二氧化碳可制取甲醇,控制在一定温度左右,持续通入二氧化碳,电解过程中 物质的量基本不变。a是电源的
物质的量基本不变。a是电源的_______ 极,阴极电极反应式为_______ 。
(1)制备二甲醚的主要反应:
反应Ⅰ:

反应Ⅱ:

反应Ⅲ:
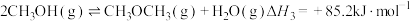
①“反应Ⅰ”能自发进行的条件是
②某反应X的平衡常数表达式为
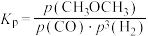 ,则反应X的热化学方程式为
,则反应X的热化学方程式为(2)二甲醚制备烯烃的主要反应:
反应Ⅳ:

反应Ⅴ:
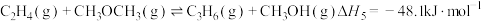
①该反应过程常用的催化剂有两种,ZSM-5以及SAPO-34,它们都是多孔笼状结构,ZSM-5笼状孔径约为0.55nm,SAPO-34约为0.4nm。相同条件下,催化剂SAPO-34反应(如图1)获得的产物中,n(C2H4):n(C3H6)更大的原因是

②一定温度下,在体积为1L的密闭容器中投入2mol CH3OCH3发生“反应Ⅳ”和“反应Ⅴ”,初始总压为po,反应到达平衡时总压为1.2po,且n(C2H4):n(C3H6)=1:1。则平衡时体系CH3OCH3转化率α(CH3OCH3)=
(3)用下图装置电解二氧化碳可制取甲醇,控制在一定温度左右,持续通入二氧化碳,电解过程中
 物质的量基本不变。a是电源的
物质的量基本不变。a是电源的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】研究碳及其化合物的相互转化对能源的充分利用、低碳经济有着重要的作用。
(1)已知:①CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+206.1kJ·mol-1
CO(g)+3H2(g) △H1=+206.1kJ·mol-1
②2H2(g)+CO(g) CH3OH(l) △H2=-128.3kJ·mol-1
CH3OH(l) △H2=-128.3kJ·mol-1
③2H2(g)+O2(g) 2H2O(g) △H3=-483.6kJ·mol-1
2H2O(g) △H3=-483.6kJ·mol-1
25℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为_________ 。
(2)利用反应①来制备氢气,为了探究温度、压强对反应①速率、转化率的影响,某同学设计了以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa)。
①实验2和实验3相比,其平衡常数关系是K2______ K3(填“>”、“<”或“=”)。
②将等物质的量的CH4和水蒸气充入1L恒容密闭容器中,发生上述反应,在400℃下达到平衡,平衡常数K=27,此时容器中CO物质的量为0.10mol,则CH4的转化率为________ 。
(3)科学家提出由CO2制取C的太阳能工艺如图1所示。
①“重整系统”发生的反应中n(FeO):n(CO2)=6:1,则FexOy的化学式为______________ 。
②“热分解系统”中每分解lmolFexOy,转移电子的物质的量为________ 。

(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值。若某溶液中溶质的浓度为1×10-3mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。如图2为25℃时H2CO3溶液的pC-pH图。请回答下列问题(若离子浓度小于10-5mol/L,可认为该离子不存在):
①在同一溶液中,H2CO3、HCO3-、CO32-_____________ (填“能”或“不能”)大量共存。
②求H2CO3一级电离平衡常数的数值Ka1=________________ 。
③人体血液里主要通过碳酸氢盐缓冲体系c(H2CO3)/c(HCO3-)可以抵消少量酸或碱,维持pH=7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将_______ 。
A.变大 B.变小 C.基本不变 D.无法判断
(1)已知:①CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+206.1kJ·mol-1
CO(g)+3H2(g) △H1=+206.1kJ·mol-1②2H2(g)+CO(g)
 CH3OH(l) △H2=-128.3kJ·mol-1
CH3OH(l) △H2=-128.3kJ·mol-1③2H2(g)+O2(g)
 2H2O(g) △H3=-483.6kJ·mol-1
2H2O(g) △H3=-483.6kJ·mol-125℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为
(2)利用反应①来制备氢气,为了探究温度、压强对反应①速率、转化率的影响,某同学设计了以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa)。
| 实验序号 | 温度℃ | 压强/kPa | CH4初始浓度/mol·L-1 | H2O初始浓度/mol·L-1 |
| 1 | 400 | P | 3.0 | 7.0 |
| 2 | T | 101 | 3.0 | 7.0 |
| 3 | 400 | 101 | 3.0 | 7.0 |
①实验2和实验3相比,其平衡常数关系是K2
②将等物质的量的CH4和水蒸气充入1L恒容密闭容器中,发生上述反应,在400℃下达到平衡,平衡常数K=27,此时容器中CO物质的量为0.10mol,则CH4的转化率为
(3)科学家提出由CO2制取C的太阳能工艺如图1所示。
①“重整系统”发生的反应中n(FeO):n(CO2)=6:1,则FexOy的化学式为
②“热分解系统”中每分解lmolFexOy,转移电子的物质的量为

(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值。若某溶液中溶质的浓度为1×10-3mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。如图2为25℃时H2CO3溶液的pC-pH图。请回答下列问题(若离子浓度小于10-5mol/L,可认为该离子不存在):
①在同一溶液中,H2CO3、HCO3-、CO32-
②求H2CO3一级电离平衡常数的数值Ka1=
③人体血液里主要通过碳酸氢盐缓冲体系c(H2CO3)/c(HCO3-)可以抵消少量酸或碱,维持pH=7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将
A.变大 B.变小 C.基本不变 D.无法判断
您最近一年使用:0次



