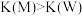在容积一定的密闭容器中,置入一定量的NO(g)和足量C(s),发生反应C(s)+2NO(g) CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示。则下列说法中正确的是
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示。则下列说法中正确的是
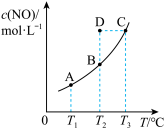
 CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示。则下列说法中正确的是
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示。则下列说法中正确的是
| A.该反应的ΔH > 0 |
| B.若该反应在T1、T2时的平衡常数分别为K1、K2 ,则K1 > K2 |
C.在T2时,若反应体系处于状态D,则此时一定有 正< 正< 逆 逆 |
| D.在T3时,若混合气体的平均摩尔质量不再变化,则可以判断反应达到平衡状态 |
更新时间:2022-11-28 17:13:04
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】在一定温度下,将等物质的量的A和B两种气体混合于2L恒容密闭容器中,发生如下反应: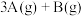
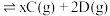 。2min末该反应达平衡,生成0.8
。2min末该反应达平衡,生成0.8 D,
D,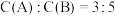 ,C的平均反应速率是0.1
,C的平均反应速率是0.1 。下列判断正确的是
。下列判断正确的是
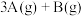
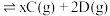 。2min末该反应达平衡,生成0.8
。2min末该反应达平衡,生成0.8 D,
D,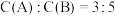 ,C的平均反应速率是0.1
,C的平均反应速率是0.1 。下列判断正确的是
。下列判断正确的是A. |
B.2min内B的反应速率为0.2 |
| C.A的转化率为50% |
| D.混合气体的密度不变或平均相对分子质量不变,都可以表明该反应已达到平衡状态 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下,在某恒容的密闭容器中,发生可逆反应N2(g)+3H2(g) 2NH3(g),下列有关该反应的说法正确的是
2NH3(g),下列有关该反应的说法正确的是
 2NH3(g),下列有关该反应的说法正确的是
2NH3(g),下列有关该反应的说法正确的是| A.每转移0.6mol电子,同时消耗2.24LN2(g) |
| B.加入合适的催化剂,正反应速率增大,逆反应速率也增大 |
| C.每形成1molH﹣H键,同时形成2molN﹣H键,则该反应达到平衡 |
| D.反应达到平衡后,保持其他条件不变,仅通入少量的稀有气体,正、逆反应速率均增大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】可逆反应2SO2+O2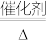 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
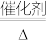 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是| A.升高温度平衡向正反应方向移动 |
| B.增大压强SO2的转化率增大 |
| C.加入催化剂平衡不发生移动,但反应速率加快 |
| D.只增大SO2浓度平衡不移动 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
下列说法正确的是
 Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A.升高温度,CO的平衡转化率增大 |
B.80℃时反应Ni(CO)4(g) Ni(s)+4CO(g)的平衡常数为0.5 Ni(s)+4CO(g)的平衡常数为0.5 |
| C.在80℃达到平衡时,充入一定量的Ni(CO)4气体再次平衡后,CO的体积分数增大,平衡常数减小 |
| D.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L |
您最近一年使用:0次
【推荐1】在恒温条件下,向盛有食盐的2L恒容密闭容器中加入 和
和 ,发生两个反应:
,发生两个反应:
①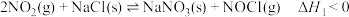 平衡常数
平衡常数
②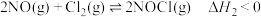 平衡常数
平衡常数
10min时反应达到平衡测得容器内体系的压强减少20%,10min内用NOCl(g)表示的平均反应速率 。下列说法不正确的是
。下列说法不正确的是
 和
和 ,发生两个反应:
,发生两个反应:①
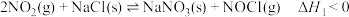 平衡常数
平衡常数
②
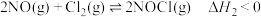 平衡常数
平衡常数
10min时反应达到平衡测得容器内体系的压强减少20%,10min内用NOCl(g)表示的平均反应速率
 。下列说法不正确的是
。下列说法不正确的是A.反应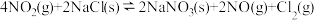 的平衡常数为 的平衡常数为 |
B.平衡后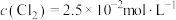 |
C.其他条件保持不变,反应在恒压条件下进行,则平衡常数 增大 增大 |
D.平衡时 的转化率为60% 的转化率为60% |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】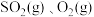 和
和 起始的物质的量分数分别为30%、28.4%和41.6%分别在
起始的物质的量分数分别为30%、28.4%和41.6%分别在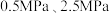 和
和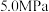 下发生反应:
下发生反应: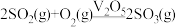 ,
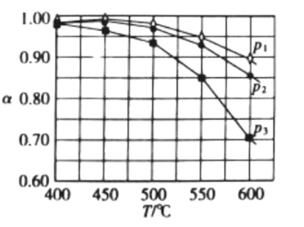
, 平衡转化率(α)随温度的变化如图所示。下列说法正确的是
平衡转化率(α)随温度的变化如图所示。下列说法正确的是
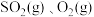 和
和 起始的物质的量分数分别为30%、28.4%和41.6%分别在
起始的物质的量分数分别为30%、28.4%和41.6%分别在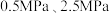 和
和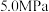 下发生反应:
下发生反应: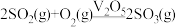 ,
, 平衡转化率(α)随温度的变化如图所示。下列说法正确的是
平衡转化率(α)随温度的变化如图所示。下列说法正确的是
A.压强大小顺序: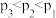 |
B.在600℃、0.5MPa下,反应达到平衡时, 的物质的量分数为20% 的物质的量分数为20% |
C.恒容条件下,增加 初始用量,α增大 初始用量,α增大 |
D.其他条件不变,若将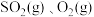 初始用量调整为 初始用量调整为 ,则平衡常数K减小 ,则平衡常数K减小 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
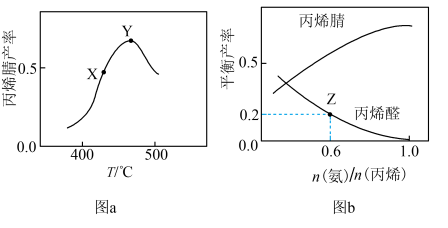
【推荐1】以CH3CH=CH2、NH3、O2为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的化学方程式分别为:反应Ⅰ.2C3H6+2NH3+3O2 2C3H3N(g)+6H2O(g);反应Ⅱ.C3H6+O2
2C3H3N(g)+6H2O(g);反应Ⅱ.C3H6+O2 C3H4O(g)+H2O(g)。反应相同时间,丙烯腈产率与反应温度的关系如图a所示,丙烯腈和丙烯醛的平衡产率与
C3H4O(g)+H2O(g)。反应相同时间,丙烯腈产率与反应温度的关系如图a所示,丙烯腈和丙烯醛的平衡产率与 的关系如图b所示。下列说法正确的是(丙烯腈的选择性=
的关系如图b所示。下列说法正确的是(丙烯腈的选择性=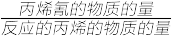 ×100%)( )
×100%)( )
 2C3H3N(g)+6H2O(g);反应Ⅱ.C3H6+O2
2C3H3N(g)+6H2O(g);反应Ⅱ.C3H6+O2 C3H4O(g)+H2O(g)。反应相同时间,丙烯腈产率与反应温度的关系如图a所示,丙烯腈和丙烯醛的平衡产率与
C3H4O(g)+H2O(g)。反应相同时间,丙烯腈产率与反应温度的关系如图a所示,丙烯腈和丙烯醛的平衡产率与 的关系如图b所示。下列说法正确的是(丙烯腈的选择性=
的关系如图b所示。下列说法正确的是(丙烯腈的选择性=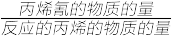 ×100%)( )
×100%)( )
| A.其他条件不变,增大压强有利于提高丙烯腈平衡产率 |
| B.图a中X点所示条件下,延长反应时间能提高丙烯腈产率 |
| C.图a中Y点所示条件下,改用对丙烯腈选择性更好的催化剂能提高丙烯腈产率 |
D.由图b中Z点可知,该温度下反应Ⅱ的平衡常数为K= |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列图示与对应的叙述正确的是()


A.a表示反应4CO(g)+2NO2(g) N2(g)+4CO2(g)保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况,由图可知,NO2的转化率:cba N2(g)+4CO2(g)保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况,由图可知,NO2的转化率:cba |
| B.b表示25℃时,分别加水稀释体积均为100mL、pH=2的CH3COOH溶液和HX溶液,则25℃时HX的电离平衡常数大于CH3COOH的电离平衡常数 |
| C.c是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1p2 |
| D.d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图象 |
您最近一年使用:0次

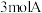 气体和
气体和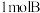 气体混合于固定容积为
气体混合于固定容积为 的密闭容器中,发生反应:
的密闭容器中,发生反应: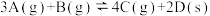 。
。 末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是
末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是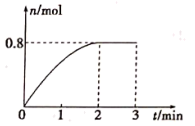


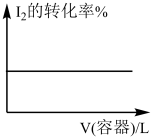 I2(g)+H2(g)
I2(g)+H2(g) 2HI(g) (恒温)
2HI(g) (恒温)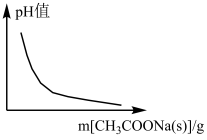 CH3COOH
CH3COOH FeCl3+3KSCN
FeCl3+3KSCN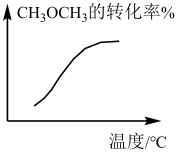 CH3OCH(g)+3H2O(g)
CH3OCH(g)+3H2O(g)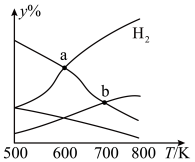
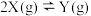 ,在温度
,在温度 、
、 下X的物质的量浓度
下X的物质的量浓度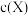 随时间t变化的曲线如图所示,下列叙述正确的是
随时间t变化的曲线如图所示,下列叙述正确的是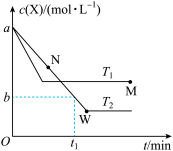
 内,
内,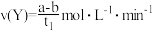
 大于W点的逆反应速率
大于W点的逆反应速率