硫及其化合物在生产生活中具有广泛应用。由自然界的硫磺和金属硫化物矿通过化学反应可得到SO2,SO2催化氧化生成SO3,其热化学方程式为2SO2(g)+O2(g) 2SO3(g) △H=-198 kJ/mol。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有SO2,用NaOH等碱性溶液吸收尾气中的SO2,可得到NaHSO3、Na2SO3等化工产品。对于反应2SO2(g)+O2(g)
2SO3(g) △H=-198 kJ/mol。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有SO2,用NaOH等碱性溶液吸收尾气中的SO2,可得到NaHSO3、Na2SO3等化工产品。对于反应2SO2(g)+O2(g) 2SO3(g),下列有关说法正确的是
2SO3(g),下列有关说法正确的是
 2SO3(g) △H=-198 kJ/mol。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有SO2,用NaOH等碱性溶液吸收尾气中的SO2,可得到NaHSO3、Na2SO3等化工产品。对于反应2SO2(g)+O2(g)
2SO3(g) △H=-198 kJ/mol。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有SO2,用NaOH等碱性溶液吸收尾气中的SO2,可得到NaHSO3、Na2SO3等化工产品。对于反应2SO2(g)+O2(g) 2SO3(g),下列有关说法正确的是
2SO3(g),下列有关说法正确的是| A.工业生产使用V2O5作催化剂,能降低该反应的活化能,同时降低该反应的焓变 |
| B.工业生产通入稍过量的氧气,能提高O2的转化率 |
| C.工业生产采用常压操作,可能是因为常压下SO2的转化率已经很高了 |
| D.工业生产采用450-500℃,可能是为了使平衡正向移动,提高SO2平衡转化率 |
22-23高二上·江苏扬州·期中 查看更多[3]
江苏省扬州市高邮市2022-2023学年高二上学期11月阶段测试化学试题(已下线)第08讲 化学反应的调控-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)江苏省扬州市广陵区红桥高级中学2023-2024学年高二上学期期中化学(选修)试卷
更新时间:2022-11-28 15:21:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】 、
、 和
和 合成
合成 的反应历程如图所示。下列说法错误的是
的反应历程如图所示。下列说法错误的是
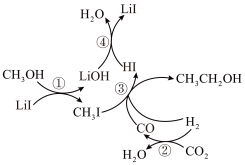
 、
、 和
和 合成
合成 的反应历程如图所示。下列说法错误的是
的反应历程如图所示。下列说法错误的是
| A.该历程一共有4种中间产物 |
| B.该历程中只有反应②是氧化还原反应 |
| C.该历程涉及极性键和非极性键的断裂 |
D.总反应方程式可表示为: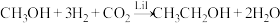 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】据文献报道,某反应的反应历程如图所示,下列有关该历程的说法正确的是
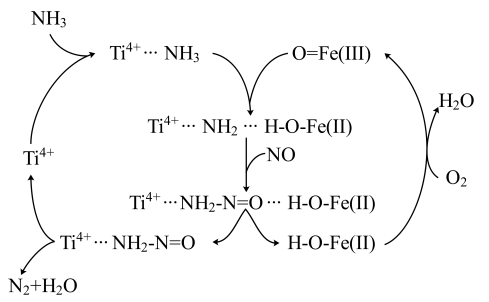

| A.Ti4+…NH2—N=O是中间产物 |
| B.Ti4+…NH3是催化剂 |
C.总反应化学方程式为:4NH3+3O2 2N2+6H2O 2N2+6H2O |
| D.Ti4+…NH2—N=O→Ti4++N2+H2O的反应过程中没有非极性键的形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】液态N2O4是火箭推进系统的有效氧化剂。实验室制备少量N2O4的流程如下:
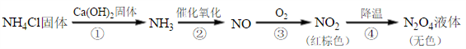
下列分析正确的是
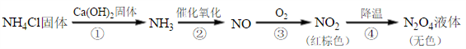
下列分析正确的是
| A.反应①、③中氮元素的化合价发生了变化 |
| B.反应②利用了NH3的氧化性 |
| C.反应④的颜色变化是由化学平衡移动引起的 |
D.反应①可由图所示装置实现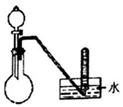 |
您最近一年使用:0次
【推荐2】298 K时, γ-羟基丁酸水溶液发生如下反应,生成
γ-羟基丁酸水溶液发生如下反应,生成 丁内酯: HOCH2CH2CH2COOH
丁内酯: HOCH2CH2CH2COOH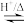
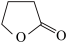 +H2O
+H2O
 丁内酯的浓度如下表。
丁内酯的浓度如下表。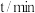 | 20 | 50 | 80 | 100 | 120 | 160 | 220 | ∞ |
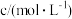 | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
| A.增大γ-羟基丁酸的浓度可提高γ-丁内酯的产率 |
| B.298 K时,该反应的平衡常数为2.75 |
| C.反应至120 min时,γ-羟基丁酸的转化率<50% |
| D.80~120 min的平均反应速率:v(γ-丁内酯) >1.2×10-3 mol ∙ L-1∙min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】关节炎首次发作一般在寒冷的季节,原因是关节滑液中形成了尿酸钠晶体( ),易诱发关节疼痛,其化学机理:①
),易诱发关节疼痛,其化学机理:①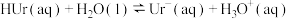 ;②
;②
 。下列叙述正确的是
。下列叙述正确的是
 ),易诱发关节疼痛,其化学机理:①
),易诱发关节疼痛,其化学机理:①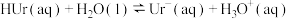 ;②
;②
 。下列叙述正确的是
。下列叙述正确的是| A.反应①是尿酸的水解方程式 |
B.反应②的 |
C.增大关节滑液中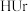 和 和 含量是治疗关节疼痛的方法之一 含量是治疗关节疼痛的方法之一 |
| D.关节保暖可以缓解疼痛,原理是平衡②逆向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,反应CH2=CH2(g)+H2O(g) CH3CH2OH(g)在密闭容器中达到平衡,下列说法正确的是
CH3CH2OH(g)在密闭容器中达到平衡,下列说法正确的是
 CH3CH2OH(g)在密闭容器中达到平衡,下列说法正确的是
CH3CH2OH(g)在密闭容器中达到平衡,下列说法正确的是A.增大压强,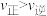 ,平衡常数增大 ,平衡常数增大 |
B.加入催化剂,平衡时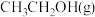 的浓度增大 的浓度增大 |
C.恒容下,充入一定量的 ,平衡向正反应方向移动 ,平衡向正反应方向移动 |
D.恒容下,充入一定量的 , , 的平衡转化率增大 的平衡转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】二甲醚(CH3OCH3)是制冷剂、局部麻醉药和燃料。工业上可利用CO2催化加氢合成二甲醚,其过程中主要发生下列反应:
反应I:CO2(g)+H2(g) CO(g)+H2O(g) △H1>0
CO(g)+H2O(g) △H1>0
反应II:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H2<0
CH3OCH3(g)+3H2O(g) △H2<0
一定条件下,于密闭容器中投入一定量CO2和H2发生上述反应。下列说法正确的是
反应I:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1>0
CO(g)+H2O(g) △H1>0反应II:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H2<0
CH3OCH3(g)+3H2O(g) △H2<0一定条件下,于密闭容器中投入一定量CO2和H2发生上述反应。下列说法正确的是
| A.其他条件不变,升高温度CO2的平衡转化率降低 |
| B.其他条件不变,缩小容器体积能提高CH3OCH3平衡产率 |
| C.其他条件不变,增大H2投入量一定能提高CH3OCH3平衡产率 |
| D.其他条件不变,使用不同催化剂对CH3OCH3的平衡产率不产生影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】合成气(CO、 )可用于制备甲烷:
)可用于制备甲烷:
 。向1 L某恒容密闭容器中通入0.2 mol
。向1 L某恒容密闭容器中通入0.2 mol  和m mol
和m mol 发生上述反应,测得
发生上述反应,测得 的平衡转化率与投料比
的平衡转化率与投料比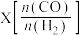 以及温度的关系如图所示(a点对应体系经2min达到平衡)。下列说法正确的是
以及温度的关系如图所示(a点对应体系经2min达到平衡)。下列说法正确的是
 )可用于制备甲烷:
)可用于制备甲烷:
 。向1 L某恒容密闭容器中通入0.2 mol
。向1 L某恒容密闭容器中通入0.2 mol  和m mol
和m mol 发生上述反应,测得
发生上述反应,测得 的平衡转化率与投料比
的平衡转化率与投料比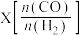 以及温度的关系如图所示(a点对应体系经2min达到平衡)。下列说法正确的是
以及温度的关系如图所示(a点对应体系经2min达到平衡)。下列说法正确的是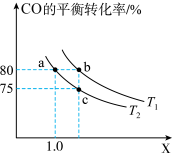
A. |
| B.正反应速率:c>b |
C.a、b点对应的平衡常数 |
D.a点反应从开始到平衡,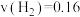 mol⋅L mol⋅L ⋅min ⋅min |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某可逆反应平衡常数表达式为K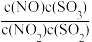 。达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是
。达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是
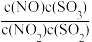 。达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是
。达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是A.该反应的化学方程式为NO(g)+SO3(g) NO2(g)+SO2(g) NO2(g)+SO2(g) |
| B.升高温度K增大 |
| C.升高温度,正反应速率增大,逆反应速率减小 |
| D.一定条件下达到平衡后,缩小容器体积,使体系压强增大,气体颜色加深 |
您最近一年使用:0次

 与
与 在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如图(图中只画出了HAP的部分结构)。下列说法
在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如图(图中只画出了HAP的部分结构)。下列说法
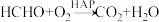
 Y(g),在温度T1、T2下,X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),在温度T1、T2下,X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是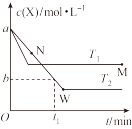
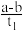 mol·L-1·min-1
mol·L-1·min-1

