常温下,下列说法正确的是
| A.等体积、等物质的量浓度的氨水和氢氧化钠溶液,分别通入氯化氢气体至溶液呈中性,氨水消耗的氯化氢更少 |
B.浓度均为0.1mol•L-1的氨水和盐酸等体积混合后,溶液中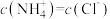 |
| C.pH相等的盐酸和氯化铵溶液中,c(Cl-)相同 |
| D.浓度均为0.1mol•L-1的盐酸和醋酸溶液,导电能力不同 |
更新时间:2022-11-12 18:56:31
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】已知25℃时有关弱酸的电离平衡常数:则下列有关说法正确的是
| 弱酸化学 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0 -11 |
| A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B.a mol·L-1HCN溶液与b mol·L-1NaOH溶液等体积混合后,所得溶液中 c(CN-)>c(Na+),则a一定大于b |
| C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小 |
| D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+ c(H+)=c(OH-)+ c(HCO3-) +2c(CO32-) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
A.常温下,将0.1 mol·L-1NH4Cl溶液与0.05 mol·L-1NaOH溶液等体积混合, c(Cl-)>c(Na+)>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
B.常温下,物质的量浓度相等的①NH4HSO4②CH3COONH4③NH4Cl三种溶液中c( ):①>③>② ):①>③>② |
| C.常温下,0.1mol·L-1NaHA溶液的pH=8,则溶液中:c(HA-)>c(OH-)>c(H2A) >c(A2-) |
| D.常温下,NaB溶液的pH=8,c(Na+)-c(B-)= 9.9×10-9mol·L-1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】室温下,向20mL0.2mol•L-1K2A(H2A:Ka1=1.64×10-3,Ka2=1.0×10-7)溶液中滴加0.2mol•L-1的HCl溶液,混合溶液pH与所加HCl溶液体积的关系。下列叙述正确的是
| A.a点溶液加水稀释后,促进A2-的水解,pH增大 |
| B.b点溶液存在关系式:c(K+)<c(Cl-)+c(HA-)+2c(A2-) |
| C.c点溶液中pH最小,所以水的电离程度最大 |
D.a、b、c三点溶液存在关系式:c(H2A)+c(HA-)+c(A2-)= c(K+) c(K+) |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】常温下,向20.00mL0.100mol/L的醋酸溶液中逐滴滴加0.100mol/L的NaOH溶液,溶液pH随加入NaOH溶液体积的变化如下表所示:
下列说法正确地是
| 编号 | ① | ② | ③ |
| 加入NaOH溶液的体积 | 10.00 | X | 20.00 |
| 溶液pH | 4.76 | 7.00 | 8.72 |
| A.①中存在c(CH3COO-)=c(CH3COOH)>c(Na+) |
| B.②中存在c(Na+)=c(CH3COO-)=c(H+)=c(OH-) |
C.③中存在c(Na+)+c(H+) c(OH-)+c(CH3COOH)=0.05mol/L c(OH-)+c(CH3COOH)=0.05mol/L |
| D.从①到③溶液中水的电离度一直增大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
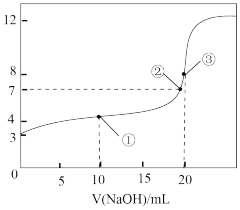
【推荐3】常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 HA溶液所得滴定曲线如图。下列说法正确的是

| A.HA是一种强酸 |
| B.点①所示溶液中:c(Na+)>c(A-)>c(HA) >c(H+)>c(OH-) |
| C.点②所示溶液中:c(Na+)=c(A-) |
| D.点③所示溶液中:c(Na+)+c(H+)=c(A-)+c(OH-) |
您最近一年使用:0次

 溶液中滴加
溶液中滴加 溶液,有白色胶状沉淀生成
溶液,有白色胶状沉淀生成 结合氢离子能力比
结合氢离子能力比 强
强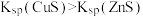
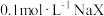 溶液和
溶液和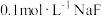 溶液的pH,前者小于后者
溶液的pH,前者小于后者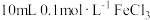 溶液和
溶液和 溶液混合,充分反应后,一份滴加淀粉溶液,一份滴加KSCN溶液,前者变为蓝色,后者变为红色
溶液混合,充分反应后,一份滴加淀粉溶液,一份滴加KSCN溶液,前者变为蓝色,后者变为红色


