西北工业大学曾华强课题组借用足球烯核心,成功实现了高效且选择性可精准定制的离子跨膜运输,如图甲所示。
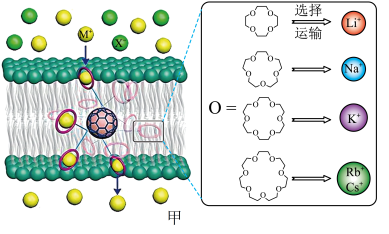
已知:图甲中的有机物为“冠醚”,命名规则是“环上原子个数-冠醚-氧原子个数”。
请回答下列问题:
(1)基态Cs原子的价层电子排布式为___________ 。基态K原子的核外电子云有___________ 个伸展方向。
(2)运输Cs+的冠醚名称是___________ 。冠醚分子中氧原子的杂化类型是___________ ,冠醚与碱金属离子之间存在微弱的配位键,配位原子是___________ (填元素符号)。
(3)几种冠醚与识别的碱金属离子的有关数据如下表所示:
18-冠醚-6不能识别和运输Na+和Cs+的原因是___________ 。观察图甲,冠醚不能识别和运输X-的主要原因可能是___________ 。
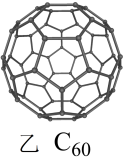
(4)足球烯的结构如图乙所示。1mol足球烯含___________ molσ键。
(5)铷晶胞为体心立方堆积,如图丙所示。
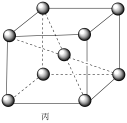
铷晶胞的原子空间利用率为___________ (用含π的式子表示)。
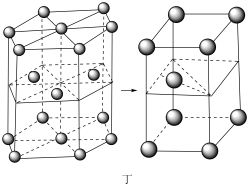
(6)锂晶胞为六方最密堆积,如图丁所示。锂晶胞中底边长为a pm,高为b pm,设NA为阿伏加德罗常数的值,则锂晶胞的密度为___________ g· cm-3(用含字母的式子表示)。

已知:图甲中的有机物为“冠醚”,命名规则是“环上原子个数-冠醚-氧原子个数”。
请回答下列问题:
(1)基态Cs原子的价层电子排布式为
(2)运输Cs+的冠醚名称是
(3)几种冠醚与识别的碱金属离子的有关数据如下表所示:
| 冠醚 | 冠醚空腔直径/pm | 适合的粒子直径/pm |
| 12冠醚- 4 | 120~ 150 | Li+ (152) |
| 15 -冠醚-5 | 170~ 220 | Na+ (204) |
| 18 -冠醚- 6 | 260~ 320 | K+ (276) |
| ___________ | 340~ 430 | Rb+ (304) |
| Cs+ (334) |
(4)足球烯的结构如图乙所示。1mol足球烯含

(5)铷晶胞为体心立方堆积,如图丙所示。

铷晶胞的原子空间利用率为
(6)锂晶胞为六方最密堆积,如图丁所示。锂晶胞中底边长为a pm,高为b pm,设NA为阿伏加德罗常数的值,则锂晶胞的密度为

2023·河南·一模 查看更多[3]
河南省湘豫名校2023届高三下学期第一次模拟考试理科综合化学试题(已下线)2022年重庆高考真题化学试题变式题(结构与性质)(已下线)河南省湘豫名校2023届高三下学期第一次模拟化学试题变式题(结构与性质)
更新时间:2023-03-08 22:30:52
|
相似题推荐
【推荐1】回答下列问题
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(2)Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
(3)Cu2+基态核外电子排布式为___________ 。
(4)Fe位于元素周期表中第四周期___________ 族,基态Fe原子核外未成对电子有___________ 个。
(5)下列Li原子电子排布图表示的状态中,能量最高和最低的分别为___________(填标号)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A.[Ne]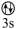 | B.[Ne]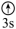 | C.[Ne] | D.[Ne] |
(3)Cu2+基态核外电子排布式为
(4)Fe位于元素周期表中第四周期
(5)下列Li原子电子排布图表示的状态中,能量最高和最低的分别为___________(填标号)。
A.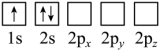 | B.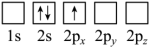 |
C.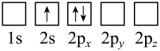 | D. |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】铝和硅在地壳中含量丰富,其单质和化合物具有广泛的应用价值。请回答下列问题:
(1)①基态Si原子的价电子排布式为______ 。
②Si所在周期中的非金属元素(Si、P、S、Cl),其第一电离能由小到大的顺序为______ 。
(2) 的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物
的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物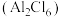 ,结构如图所示。
,结构如图所示。
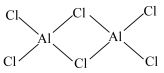
①基态Al原子核外电子的空间运动状态有______ 种,
②二聚物中Al原子的杂化轨道类型为______ 杂化。
(3)Al—空气—海水原电池的正极反应式为________________________ 。
(4)铝和白磷在一定条件下可以制备磷化铝(AlP),其晶胞如图所示:
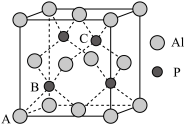
①晶胞中A1的配位数是______ ,
②若晶胞参数为apm, 为阿伏加德罗常数,则该晶胞的密度为
为阿伏加德罗常数,则该晶胞的密度为______  (列出表达式)。
(列出表达式)。
(5)以高硫铝土矿(主要成分为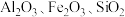 ,少量
,少量 和金属硫酸盐)为原料,获得
和金属硫酸盐)为原料,获得 的部分工艺流程如下:
的部分工艺流程如下:

①焙烧过程均会产生 ,用
,用 溶液吸收过量
溶液吸收过量 的离子方程式为
的离子方程式为__________________ 。
②“过滤”得到的滤渣中含大量的 。
。 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
______ 。
(1)①基态Si原子的价电子排布式为
②Si所在周期中的非金属元素(Si、P、S、Cl),其第一电离能由小到大的顺序为
(2)
 的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物
的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物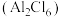 ,结构如图所示。
,结构如图所示。
①基态Al原子核外电子的空间运动状态有
②二聚物中Al原子的杂化轨道类型为
(3)Al—空气—海水原电池的正极反应式为
(4)铝和白磷在一定条件下可以制备磷化铝(AlP),其晶胞如图所示:

①晶胞中A1的配位数是
②若晶胞参数为apm,
 为阿伏加德罗常数,则该晶胞的密度为
为阿伏加德罗常数,则该晶胞的密度为 (列出表达式)。
(列出表达式)。(5)以高硫铝土矿(主要成分为
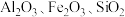 ,少量
,少量 和金属硫酸盐)为原料,获得
和金属硫酸盐)为原料,获得 的部分工艺流程如下:
的部分工艺流程如下:
①焙烧过程均会产生
 ,用
,用 溶液吸收过量
溶液吸收过量 的离子方程式为
的离子方程式为②“过滤”得到的滤渣中含大量的
 。
。 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】重水是含有较多 和
和 的水,重水对工农业生成有很大危害,其中含有
的水,重水对工农业生成有很大危害,其中含有 和
和 的重水叫暂时硬水,含有
的重水叫暂时硬水,含有 、
、 、
、 和
和 等的重水叫永久硬水,回答下面问题:
等的重水叫永久硬水,回答下面问题:
(1)画出Ca原子的原子结构示意图___________ ,硫元素在元素周期表的位置___________ ,属于___________ 区。
(2)写出基态N原子的电子排布式___________ ,画出基态O原子的价电子排布图___________ 。基态N原子的第一电离能比O原子的要大的原因是___________ 。
(3)若将基态镁原子最高能级的电子排布图表示为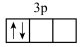 ,则它违背的电子排布规律是
,则它违背的电子排布规律是___________ 、___________ ,基态硫原子核外电子所处最高能级轨道的形状为___________ 。
(4)EDTA是硬水软化常用的化学试剂,与镁离子结合为
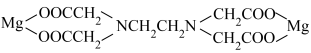
其中C、N、O、Mg四种元素的电负性由大到小的顺序是___________ ,原子半径最大的是___________ (填元素符号,下同),四种元素中基态原子核外单电子数最多的是___________ 。
(5)钙元素与铬元素、铜元素位于同一周期,写出铬、铜基态原子的价电子排布式___________ 、___________ 。
 和
和 的水,重水对工农业生成有很大危害,其中含有
的水,重水对工农业生成有很大危害,其中含有 和
和 的重水叫暂时硬水,含有
的重水叫暂时硬水,含有 、
、 、
、 和
和 等的重水叫永久硬水,回答下面问题:
等的重水叫永久硬水,回答下面问题:(1)画出Ca原子的原子结构示意图
(2)写出基态N原子的电子排布式
(3)若将基态镁原子最高能级的电子排布图表示为
 ,则它违背的电子排布规律是
,则它违背的电子排布规律是(4)EDTA是硬水软化常用的化学试剂,与镁离子结合为
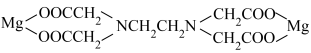
其中C、N、O、Mg四种元素的电负性由大到小的顺序是
(5)钙元素与铬元素、铜元素位于同一周期,写出铬、铜基态原子的价电子排布式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】【化学一选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大。A 是原子半径最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态。试回答下列问题:
(1)基态E原子核外电子的排布式为___________________ 。
(2)B、C、D三种元素的电负性由大到小的顺序是____________ (填元素符号)。A、C、D三种元素形成的常见离子化合物中阳离子的空间构型为_____________ ,阴离子的中心原子轨道采用______________ 杂化。
(3)E(CA3) 离子的颜色是
离子的颜色是___________ ;含有化学键类型是_____________ ;离子中C原子杂化轨道类型是__________________ 。
(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为_________ ;在一定条件下,甲和C2A4反应生成乙,同时生成在常温下分别为气体和液体的另外两种常见无污染物质。该化学反应方程式为______________________ 。
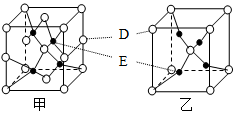
(5)若甲的密度为ρ g/cm3,NA表示阿伏伽德罗常数,则甲晶胞的边长可表示为_________ cm。
(1)基态E原子核外电子的排布式为
(2)B、C、D三种元素的电负性由大到小的顺序是
(3)E(CA3)
 离子的颜色是
离子的颜色是(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为

(5)若甲的密度为ρ g/cm3,NA表示阿伏伽德罗常数,则甲晶胞的边长可表示为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】人体血红蛋白中含有Fe2+一卟啉环配合物,结合O2后,其基本结构如图(烃基略去)。回答下列问题:
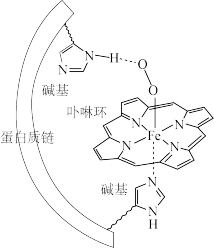
(1)Fe、N、C、H四种元素中电负性最大的是____ (填写元素符号);血红蛋白结合O2前后的中心Fe均为正二价,其基态时3d轨道中电子数为____ 。
(2)卟啉环中所有原子共平面,其中N的杂化方式为____ ,C-Nσ键有____ 个。
(3)图中Fe2+的配位数为__________ ;其中一个碱基通过 ____ 作用与O2分子结合,另一碱基的N原子提供____ 与Fe2+配位。
(4)已知气态O2的氧氧间距比图中更短。判断血红蛋白结合O2后O2活性更___ (填“高”或“低”),说明理由____ 。
(5)从298K升温到1200K时,体心立方型的δ -Fe变化为面心立方最密堆积,配位数____ (填“变大”、“不变”或“变小”)。假定升温时Fe原子半径不变,体积变为低温时的___ %(已知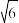 =2.45,结果保留两位有效数字)。
=2.45,结果保留两位有效数字)。

(1)Fe、N、C、H四种元素中电负性最大的是
(2)卟啉环中所有原子共平面,其中N的杂化方式为
(3)图中Fe2+的配位数为
(4)已知气态O2的氧氧间距比图中更短。判断血红蛋白结合O2后O2活性更
(5)从298K升温到1200K时,体心立方型的δ -Fe变化为面心立方最密堆积,配位数
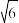 =2.45,结果保留两位有效数字)。
=2.45,结果保留两位有效数字)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】氮族元素可以形成多种多样的化合物,回答下列问题:
(1)基态As原子的价电子的轨道表示式是______ 。
(2)叠氮酸(HN3)常用于引爆剂,可用联氨( )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
______ 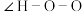 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: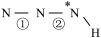 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①______ ②。
(3)乙胺( )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是______ 。
(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是______ 。

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是______ ,n原子的分数坐标是______ ,若阿伏加德罗常数值为 ,该晶体密度是
,该晶体密度是______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态As原子的价电子的轨道表示式是
(2)叠氮酸(HN3)常用于引爆剂,可用联氨(
 )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
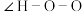 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: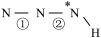 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①(3)乙胺(
 )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为
 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是 ,该晶体密度是
,该晶体密度是 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】钛元素形成的单质及其化合物有重要的应用。请回答:
(1)钛位于元素周期表中___________ 区;与钛位于同一周期且含有相同未成对电子数的过渡元素为___________ (填元素符号)。
(2)钛形成的 试剂常用作有机反应的烯化试剂,其结构如图所示。
试剂常用作有机反应的烯化试剂,其结构如图所示。
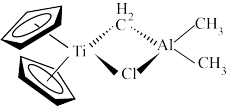
其中氯原子和铝原子的杂化方式分别为___________ 。
(3)钛形成的 是一种储氢材料。
是一种储氢材料。 的立体构型为
的立体构型为___________ 。
(4)钛形成的不同卤化物熔沸点数据如表所示。
三种卤化物熔沸点数据呈现表中变化规律的原因为___________ 。
(5)向紫色的 溶液中加入无水乙醚并通入
溶液中加入无水乙醚并通入 至饱和,则可得到绿色的
至饱和,则可得到绿色的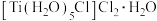 晶体。
晶体。
①晶体中所有元素的电负性由大到小的顺序为___________ 。
②晶体中配位原子为___________ ;晶体中粒子间存在的作用力有___________ (填选项字母)。
a.离子键 b.σ键 c. 键 d.金属键 e.配位键
键 d.金属键 e.配位键
(6)钛酸钡具有压电性,可用于留声机和水下侦察设备等。钛酸钡立方晶胞结构如图所示( 、
、 都分别与
都分别与 相互接触),其晶胞参数
相互接触),其晶胞参数 。
。 的配位数为12;若
的配位数为12;若 半径为140
半径为140 ,则
,则 的半径为
的半径为___________  。
。

(1)钛位于元素周期表中
(2)钛形成的
 试剂常用作有机反应的烯化试剂,其结构如图所示。
试剂常用作有机反应的烯化试剂,其结构如图所示。
其中氯原子和铝原子的杂化方式分别为
(3)钛形成的
 是一种储氢材料。
是一种储氢材料。 的立体构型为
的立体构型为(4)钛形成的不同卤化物熔沸点数据如表所示。
 |  |  | |
| 熔点/℃ | -24.1 | 38.25 | 155 |
| 沸点/℃ | 136.45 | 233.45 | 377 |
三种卤化物熔沸点数据呈现表中变化规律的原因为
(5)向紫色的
 溶液中加入无水乙醚并通入
溶液中加入无水乙醚并通入 至饱和,则可得到绿色的
至饱和,则可得到绿色的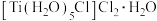 晶体。
晶体。①晶体中所有元素的电负性由大到小的顺序为
②晶体中配位原子为
a.离子键 b.σ键 c.
 键 d.金属键 e.配位键
键 d.金属键 e.配位键(6)钛酸钡具有压电性,可用于留声机和水下侦察设备等。钛酸钡立方晶胞结构如图所示(
 、
、 都分别与
都分别与 相互接触),其晶胞参数
相互接触),其晶胞参数 。
。 的配位数为12;若
的配位数为12;若 半径为140
半径为140 ,则
,则 的半径为
的半径为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】[化学一一选修3:物质结构与性质]碳族元素的单质和化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)锗是重要半导体材料,基态Ge原子中,核外电子占据最高能级的符号是__________ ,该能级的电子云轮廓图为______________ 。金属Ge晶胞结构与金刚石类似,质地硬而脆,沸点2830℃,锗晶体属于__________ 晶体。
(2)①(CH3)3C+是有机合成重要中间体,该中间体中碳原子杂化方式为______________ ,(CH3)3C+中碳骨架的几何构型为____________________ 。
②治疗铅中毒可滴注依地酸钠钙,使Pb2+转化为依地酸铅盐。下列说法正确的是_______ (填标号)

A.形成依地酸铅离子所需n(Pb2+):n(EDTA)=1:4
B.依地酸中各元素的电负性从大到小的顺序为O>N>C>H
C.依地酸铅盐中含有离子键和配位键
D.依地酸具有良好的水溶性是由于其分子间能形成氢键
(3)下表列出了碱土金属碳酸盐的热分解温度和阳离子半径:
碱土金属碳酸盐同主族由上到下的热分解温度逐渐升高,原因是:__________________________ 。
(4)有机卤化铅晶体具有独特的光电性能,下图为其晶胞结构示意图:

①若该晶胞的边长为anm,则Cl-间的最短距离是____________________ 。
②在该晶胞的另一种表达方式中,若图中Pb2+处于顶点位置,则Cl-处于_________ 位置。原子坐标参数B为(0,0,0);A1为(1/2,1/2,1/2),则X2为_________________ 。
(1)锗是重要半导体材料,基态Ge原子中,核外电子占据最高能级的符号是
(2)①(CH3)3C+是有机合成重要中间体,该中间体中碳原子杂化方式为
②治疗铅中毒可滴注依地酸钠钙,使Pb2+转化为依地酸铅盐。下列说法正确的是

A.形成依地酸铅离子所需n(Pb2+):n(EDTA)=1:4
B.依地酸中各元素的电负性从大到小的顺序为O>N>C>H
C.依地酸铅盐中含有离子键和配位键
D.依地酸具有良好的水溶性是由于其分子间能形成氢键
(3)下表列出了碱土金属碳酸盐的热分解温度和阳离子半径:
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
碱土金属碳酸盐同主族由上到下的热分解温度逐渐升高,原因是:
(4)有机卤化铅晶体具有独特的光电性能,下图为其晶胞结构示意图:

①若该晶胞的边长为anm,则Cl-间的最短距离是
②在该晶胞的另一种表达方式中,若图中Pb2+处于顶点位置,则Cl-处于
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】Al、Cr、Co、Ni的合金及其相关化合物用途非常广泛,如锂离子电池的正极材料为LiCoO2,电解质溶液为LiBF4溶液。
(1)Co2+的基态核外电子排布式为__ ,BF 的空间构型为
的空间构型为___ 。
(2)钴元素可形成种类繁多的配合物。三氯五氨合钴的化学式为Co(NH3)5Cl3,是一种典型的维尔纳配合物,具有反磁性。0.01molCo(NH3)5Cl3与足量硝酸银溶液反应时生成2.87g白色沉淀。Co(NH3)5Cl3中Co3+的配位数为___ ,该配合物中的配位原子为___ 。
(3)1951年Tsao最早报道了用LiAlH4还原腈: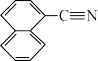

 。
。
①LiAlH4中三种元素的电负性从大到小的顺序为__ (用元素符号表示)。
② 中碳原子的轨道杂化类型为
中碳原子的轨道杂化类型为__ ,1mol该分子中含σ键的物质的量为__ 。
(4)全惠斯勒合金CrxCoyAlz的晶胞结构如图甲所示,其化学式为__ 。

(5)NiO的晶胞结构如图乙所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为___ 。一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图丙),已知O2-的半径为apm,设阿伏加德罗常数的值为NA,每平方米的面积上具有该晶体的质量为__ (用含a、NA的代数式表示)g。
(1)Co2+的基态核外电子排布式为
 的空间构型为
的空间构型为(2)钴元素可形成种类繁多的配合物。三氯五氨合钴的化学式为Co(NH3)5Cl3,是一种典型的维尔纳配合物,具有反磁性。0.01molCo(NH3)5Cl3与足量硝酸银溶液反应时生成2.87g白色沉淀。Co(NH3)5Cl3中Co3+的配位数为
(3)1951年Tsao最早报道了用LiAlH4还原腈:


 。
。①LiAlH4中三种元素的电负性从大到小的顺序为
②
 中碳原子的轨道杂化类型为
中碳原子的轨道杂化类型为(4)全惠斯勒合金CrxCoyAlz的晶胞结构如图甲所示,其化学式为

(5)NiO的晶胞结构如图乙所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为
您最近一年使用:0次
【推荐1】核电荷数依次增大的A、B、C、D、E、F都是周期表中前四周期的元素,其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,AC2为非极性分子,B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,E原子的一种核素的质量数为49,中子数为27。F元素是第四周期元素中未成对电子数最多的元素,FCl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,1mol配合物与足量的AgNO3溶液反应能立即生成3molAgCl。请根据以上情况,回答下列问题:(答题时需用元素符号表示)
(1)B氢化物与HCl反应生成的含有B元素粒子的空间构型是___________ ;F元素原子的最外层电子数为________ 个。
(2)B3-离子分别与AC2及由B、C组成的气态化合物互为等电子体,则B、C组成的化合物化学式为_______________ ;B3-离子还可以和某一价阴离子互为等电子体,该阴离子电子式为_________ ,这种阴离子常用于检验日常生活中的一种金属阳离子,则金属阳离子符号为_________ 。
(3)B元素与同周期相邻元素的第一电离能由小到大的顺序为_______________ 。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应中氧化剂与还原剂的物质的量之比是_______________ 。
(5)F3+的核外电子排布式是_________________________ ,FCl3形成的六配位的配合物化学式为________________________ 。

(6)E的一种氧化物晶胞结构(长方体)如图所示,该氧化物的化学式为__________ ;若该晶胞的三个晶胞参数分别为:apm、bpm、cpm。则该氧化物的密度为____________ g/cm3。(写出表达式即可)
(1)B氢化物与HCl反应生成的含有B元素粒子的空间构型是
(2)B3-离子分别与AC2及由B、C组成的气态化合物互为等电子体,则B、C组成的化合物化学式为
(3)B元素与同周期相邻元素的第一电离能由小到大的顺序为
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应中氧化剂与还原剂的物质的量之比是
(5)F3+的核外电子排布式是

(6)E的一种氧化物晶胞结构(长方体)如图所示,该氧化物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】金属铜在电力工业和科研领域中的应用广泛,科学家对于铜元素的研究不断深入。请回答下列问题:
(1)基态Cu原子的价电子排布式为_______ 。
(2)已知:高温下Cu2O比CuO稳定。从核外电子排布角度解释高温下Cu2O更稳定的原因为_______ 。
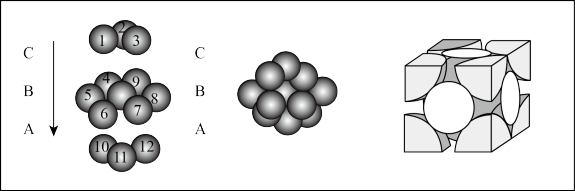
(3)铜晶体中铜原子的堆积方式如图所示,则晶体铜原子的堆积方式为_______ 。
(4)当黄铜受到氨腐蚀时,会生成四氨合铜络合物,出现“龟裂”现象。
①[Cu(NH3)4]2+中各元素电负性由大到小的顺序为_____ ,其中N原子的杂化轨道类型为_____ 。
②[Cu(NH3)4]2+中NH3的键角比独立存在的NH3分子结构中的键角_______ (填“大”或“小”)。
③1mol[Cu(NH3)4]2+中存在_______ 个σ键(用阿伏加德罗常数的数值用NA表示)。
(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(白球代表铜原子)。
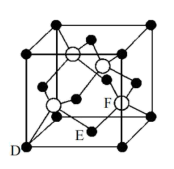
①该晶体的化学式为_______ 。
②已知该晶体的密度为ρg/cm3,阿伏加德罗常数的值为NA,则该晶体中Cu原子和M原子之间的最短距离为_______ pm(写出计算式)。
(1)基态Cu原子的价电子排布式为
(2)已知:高温下Cu2O比CuO稳定。从核外电子排布角度解释高温下Cu2O更稳定的原因为
(3)铜晶体中铜原子的堆积方式如图所示,则晶体铜原子的堆积方式为

(4)当黄铜受到氨腐蚀时,会生成四氨合铜络合物,出现“龟裂”现象。
①[Cu(NH3)4]2+中各元素电负性由大到小的顺序为
②[Cu(NH3)4]2+中NH3的键角比独立存在的NH3分子结构中的键角
③1mol[Cu(NH3)4]2+中存在
(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(白球代表铜原子)。

①该晶体的化学式为
②已知该晶体的密度为ρg/cm3,阿伏加德罗常数的值为NA,则该晶体中Cu原子和M原子之间的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】镍及其化合物在工农业生产中有着广泛应用,回答下列问题:
 基态镍原子的价电子排布式为
基态镍原子的价电子排布式为_________ ;元素镍的第二电离能比铜的小,其原因为_________________ 。
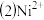 的检验可通过如下反应进行:
的检验可通过如下反应进行:

 丁二肟中碳原子的杂化轨道类型为
丁二肟中碳原子的杂化轨道类型为___________ 。
 二丁二肟合镍
二丁二肟合镍 Ⅱ
Ⅱ 中存在的作用力有
中存在的作用力有_________  填选项字母
填选项字母 。
。
A. 键
键  键
键 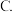 配位键
配位键  氢键
氢键
 四羰基镍
四羰基镍 为无色挥发性剧毒液体。熔点
为无色挥发性剧毒液体。熔点 ,沸点
,沸点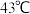 。不溶于水,易溶于乙醇等有机溶剂,呈四面体构型。四羰基镍的晶体类型是
。不溶于水,易溶于乙醇等有机溶剂,呈四面体构型。四羰基镍的晶体类型是__________ 。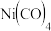 可通过如下反应合成:
可通过如下反应合成: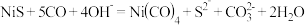 。反应中涉及所有元素的电负性由大到小的顺序为
。反应中涉及所有元素的电负性由大到小的顺序为______________ :与 互为等电子体的分子有
互为等电子体的分子有__________  任写1种
任写1种 。
。
 和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
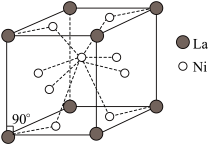
 该晶体的化学式为
该晶体的化学式为_____________ 。
 已知该晶体的摩尔质量为
已知该晶体的摩尔质量为 ,密度为
,密度为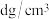 。设
。设 为阿伏加 德罗常数的值,则该晶胞的体积是
为阿伏加 德罗常数的值,则该晶胞的体积是___________  用含M、d、
用含M、d、 的代数式表示
的代数式表示 。
。
 基态镍原子的价电子排布式为
基态镍原子的价电子排布式为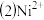 的检验可通过如下反应进行:
的检验可通过如下反应进行:
 丁二肟中碳原子的杂化轨道类型为
丁二肟中碳原子的杂化轨道类型为 二丁二肟合镍
二丁二肟合镍 Ⅱ
Ⅱ 中存在的作用力有
中存在的作用力有 填选项字母
填选项字母 。
。A.
 键
键  键
键  配位键
配位键  氢键
氢键 四羰基镍
四羰基镍 为无色挥发性剧毒液体。熔点
为无色挥发性剧毒液体。熔点 ,沸点
,沸点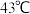 。不溶于水,易溶于乙醇等有机溶剂,呈四面体构型。四羰基镍的晶体类型是
。不溶于水,易溶于乙醇等有机溶剂,呈四面体构型。四羰基镍的晶体类型是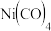 可通过如下反应合成:
可通过如下反应合成: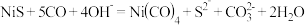 。反应中涉及所有元素的电负性由大到小的顺序为
。反应中涉及所有元素的电负性由大到小的顺序为 互为等电子体的分子有
互为等电子体的分子有 任写1种
任写1种 。
。 和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
 该晶体的化学式为
该晶体的化学式为 已知该晶体的摩尔质量为
已知该晶体的摩尔质量为 ,密度为
,密度为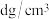 。设
。设 为阿伏加 德罗常数的值,则该晶胞的体积是
为阿伏加 德罗常数的值,则该晶胞的体积是 用含M、d、
用含M、d、 的代数式表示
的代数式表示 。
。
您最近一年使用:0次



