砷化镓(GaAs)是优良的半导体材料,其晶体结构与单晶硅相似。
(1)基态Ga原子的价电子排布式为___________ ,其同周期元素中未成对电子数最多的是___________ (填元素符号)。
(2)GaAs可用Ga(CH3)3(常温下为无色液体)和AsH3高温反应制得,同时生成另一种产物,写出反应方程式___________ ,另一种产物中心原子的杂化类型为___________ 。
(3)沸点AsH3_________ NH3(填“>”、“<”、“=”),原因是_________ 。
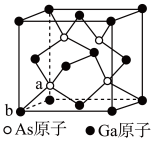
(4)GaAs的晶胞结构如图所示,As的配位数___________ ,若晶胞中距离最近的两个Ga原子距离为anm,阿伏加德罗常数的值为,则GaAs的密度为________ 。
(1)基态Ga原子的价电子排布式为
(2)GaAs可用Ga(CH3)3(常温下为无色液体)和AsH3高温反应制得,同时生成另一种产物,写出反应方程式
(3)沸点AsH3
(4)GaAs的晶胞结构如图所示,As的配位数

更新时间:2023-04-26 12:00:19
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
【推荐1】北京化工大学杨占旭教授合成了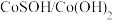 复合催化剂,其在低温条件下能催化水分解制氢,有利于拯救能源危机和缓解环境恶化,其工作原理如图所示。
复合催化剂,其在低温条件下能催化水分解制氢,有利于拯救能源危机和缓解环境恶化,其工作原理如图所示。
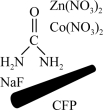
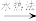
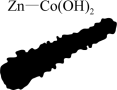

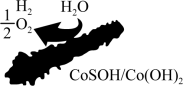
回答下列问题:
(1)基态Co原子的电子排布式为___________ ,其能量最高的能级是___________
(2)Cu的第三电离能比Zn的小,其原因是___________ ;C、N、O、F的电负性由大到小的顺序为___________ 。
(3)尿素可看作是氨基甲酰胺,有一定的弱碱性,其与 、
、 等作用时,生成难溶于水的盐:
等作用时,生成难溶于水的盐: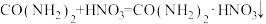 。
。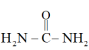 中碳原子的杂化方式是
中碳原子的杂化方式是___________ ,该分子中含有___________ 个σ键。
(4) 的键角
的键角___________ (填“大于”或“小于”) 的键角,其原因为
的键角,其原因为___________ 。
(5)金属锌的晶胞结构如图所示。

①Zn原子的配位数为___________ ;
②该晶体的密度为___________ g/cm3 (列出算式)。
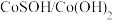 复合催化剂,其在低温条件下能催化水分解制氢,有利于拯救能源危机和缓解环境恶化,其工作原理如图所示。
复合催化剂,其在低温条件下能催化水分解制氢,有利于拯救能源危机和缓解环境恶化,其工作原理如图所示。
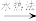



回答下列问题:
(1)基态Co原子的电子排布式为
(2)Cu的第三电离能比Zn的小,其原因是
(3)尿素可看作是氨基甲酰胺,有一定的弱碱性,其与
 、
、 等作用时,生成难溶于水的盐:
等作用时,生成难溶于水的盐: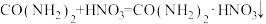 。
。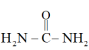 中碳原子的杂化方式是
中碳原子的杂化方式是(4)
 的键角
的键角 的键角,其原因为
的键角,其原因为(5)金属锌的晶胞结构如图所示。

①Zn原子的配位数为
②该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】钛硅分子筛是一种新型固体催化剂,可催化合成重要有机合成活性试剂甲乙酮肟(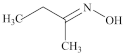 )。回答下列问题:
)。回答下列问题:
(1)基态硅原子的核外电子空间运动状态有___________ 种。
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为___________ ,氮原子的杂化方式为___________ ,C=N与C-C键夹角___________ (填“<”“>”或“=”)C=N与N-O键夹角。
(3) 和
和 均是制备钛硅分子筛的重要中间体。
均是制备钛硅分子筛的重要中间体。
① 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为___________ ,其空间构型为___________ 。
② 与金属
与金属 在高温条件下可反应生成
在高温条件下可反应生成 ,
, 中
中 极易被氧化,还原性很强。试解释
极易被氧化,还原性很强。试解释 还原性强的原因
还原性强的原因___________ 。
 )。回答下列问题:
)。回答下列问题:(1)基态硅原子的核外电子空间运动状态有
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为
(3)
 和
和 均是制备钛硅分子筛的重要中间体。
均是制备钛硅分子筛的重要中间体。①
 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为②
 与金属
与金属 在高温条件下可反应生成
在高温条件下可反应生成 ,
, 中
中 极易被氧化,还原性很强。试解释
极易被氧化,还原性很强。试解释 还原性强的原因
还原性强的原因
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
基态氮原子的轨道表示式为_____ ,占据最高能级电子的电子云轮廓图为_____ 形。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中 区的元素是
区的元素是_____ (填元素符号)。
② 的第一电离能小于
的第一电离能小于 ,原因是
,原因是_____ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明 的常见化合价为+2价的原因:
的常见化合价为+2价的原因:_____ 。
(3)我国科研人员研制出了“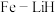 ”催化剂,温度、压强分别降到了
”催化剂,温度、压强分别降到了 、
、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。
①基态 原子的核外电子排布式为
原子的核外电子排布式为_____ 。
②比较 与
与 的半径大小关系:
的半径大小关系: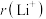
_____  (填“>”或“<”)。
(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
基态氮原子的轨道表示式为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。①上述氧化物所涉及的元素中,处于元素周期表中
 区的元素是
区的元素是②
 的第一电离能小于
的第一电离能小于 ,原因是
,原因是③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 |  |  |  |
| 电离能/(kJmol-1) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
 的常见化合价为+2价的原因:
的常见化合价为+2价的原因:(3)我国科研人员研制出了“
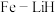 ”催化剂,温度、压强分别降到了
”催化剂,温度、压强分别降到了 、
、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。①基态
 原子的核外电子排布式为
原子的核外电子排布式为②比较
 与
与 的半径大小关系:
的半径大小关系: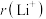
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】碳是形成单质和化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图1、图2所示。
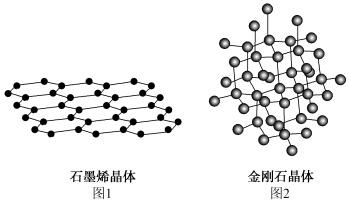
①石墨烯是石墨分离出的单独一层,石墨烯非常稳定,属于厚度只有一个直径大小的“二维材料”,写出一个石墨烯所拥有的特性_____ 。
②求出12g金刚石中含σ键数目为_____ 。
(2)碳的主要氧化物有CO,能与金属Fe形成一种浅黄色液体Fe(CO)5,Fe(CO)5是配合物其熔点为−20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:
①该化合物的晶体中涉及的作用力有_____ 。
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②算出1molFe(CO)5配合物中含有σ键数目_____ 。
(3)CH 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为______ 。
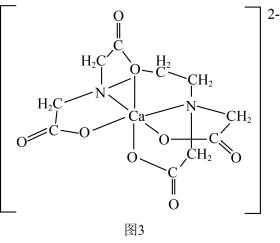
(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图3所示。配位体中碳原子的杂化方式有______ 。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图1、图2所示。

①石墨烯是石墨分离出的单独一层,石墨烯非常稳定,属于厚度只有一个直径大小的“二维材料”,写出一个石墨烯所拥有的特性
②求出12g金刚石中含σ键数目为
(2)碳的主要氧化物有CO,能与金属Fe形成一种浅黄色液体Fe(CO)5,Fe(CO)5是配合物其熔点为−20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:
①该化合物的晶体中涉及的作用力有
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②算出1molFe(CO)5配合物中含有σ键数目
(3)CH
 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图3所示。配位体中碳原子的杂化方式有

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,Q的核电荷数是X与Z的核电荷数之和, E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为___________ 、____________ ;
(2)XZ2与YZ2分子的立体结构分别是___________ 和___________ ,在水中溶解度较大的是________ (填化学式);
(3)Q元素的价电子排布图为___________ ,在形成化合物时它的最高化合价为_____ ;
(4)Z与E形成的化合物中,各原子最外层都达到8电子结构,该化合物中心原子采用的轨道杂化方式是____________ 。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分子的立体结构分别是
(3)Q元素的价电子排布图为
(4)Z与E形成的化合物中,各原子最外层都达到8电子结构,该化合物中心原子采用的轨道杂化方式是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
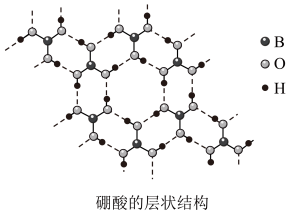
【推荐3】硼(B)及其化合物在化学中有重要的地位,请回答下列问题: 是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
①硼酸中B原子的杂化轨道类型为______ 。
②加热时,硼酸的溶解度增大,主要原因是______ 。
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的 而呈酸性、硼酸的电离方程式:
而呈酸性、硼酸的电离方程式:______ 。
(2)立方氮化硼的结构与金刚石相似,晶胞结构如图所示。______ 。
②已知晶胞边长为361.5pm,则立方氮化硼的密度是______  。(只要求列算式,不必计算出数值,阿伏加德罗常数用
。(只要求列算式,不必计算出数值,阿伏加德罗常数用 表示)
表示)
 是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。①硼酸中B原子的杂化轨道类型为
②加热时,硼酸的溶解度增大,主要原因是
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的
 而呈酸性、硼酸的电离方程式:
而呈酸性、硼酸的电离方程式:(2)立方氮化硼的结构与金刚石相似,晶胞结构如图所示。

②已知晶胞边长为361.5pm,则立方氮化硼的密度是
 。(只要求列算式,不必计算出数值,阿伏加德罗常数用
。(只要求列算式,不必计算出数值,阿伏加德罗常数用 表示)
表示)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】短周期的5种非金属元素,其中A、B、C的特征电子排布可表示为A:asa,B:bsbbpb,C:csccp2c,D与B同主族,E在C的下一周期,且是同周期元素中电负性最大的元素。回答下列问题:
(1)由A、B、C、E四种元素中的两种元素可形成多种分子,下列分子①BC2②BA4③A2C2④BE4,其中属于极性分子的是___ (填序号);分子BC2中含σ键__ 个,含π键__ 个。
(2)C的氢化物比下一周期同族元素的氢化物沸点还要高,其原因是__ 。
(3)B、C两元素都能和A元素组成两种常见的溶剂,其分子式为___ 、__ 。DE4在前者中的溶解度__ (填“大于”或“小于”)在后者中的溶解度。
(4)BA4、BE4和DE4的沸点从高到低的顺序为__ (填化学式)。
(1)由A、B、C、E四种元素中的两种元素可形成多种分子,下列分子①BC2②BA4③A2C2④BE4,其中属于极性分子的是
(2)C的氢化物比下一周期同族元素的氢化物沸点还要高,其原因是
(3)B、C两元素都能和A元素组成两种常见的溶剂,其分子式为
(4)BA4、BE4和DE4的沸点从高到低的顺序为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)1mol乙醛分子中含有σ键的数目为_____ ,乙酸的沸点明显高于乙醛,其主要原因是_____ 。
(2)短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p能级与所有s能级电子总数相等,D元素原子的L层的p能级中有3个未成对电子。
①C元素原子基态时的电子排布式为_____ ,若A元素为非金属元素,A与C形成的化合物中的共价键属于_____ (填“σ”或“π”)键。
②当n=2时,B的最简单气态氢化物的分子空间结构为_____ ,中心原子的杂化方式为_____ ,BC2属于_____ (填“极性”或“非极性”)分子。
(3)已知苯酚(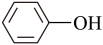 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_____ (水杨酸)Ka(苯酚)(填“>”或“<”),其原因是_____ 。
(1)1mol乙醛分子中含有σ键的数目为
(2)短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p能级与所有s能级电子总数相等,D元素原子的L层的p能级中有3个未成对电子。
①C元素原子基态时的电子排布式为
②当n=2时,B的最简单气态氢化物的分子空间结构为
(3)已知苯酚(
 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
您最近一年使用:0次
【推荐3】甲醇的结构决定了其性质及其应用。请按要求回答下列问题。
(1)甲醇、乙烷沸点分别为65℃、-89℃,对比分析推测乙醇比丙烷沸点____ (填“高很多”或“低很多”或“等于”),你的推测依据是____ 。
(2)甲醇结构式如图,其分子中含a、b、c三种化学键。
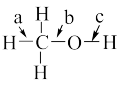
①甲醇的官能团名称为____ 。
②甲醇分子中较易断裂的化学键是____ (填字母)。从原子结构的视角分析得出此结论的依据是____ 。
③写出甲醇与钠反应的化学方程式____ 。
④在铜催化加热条件下,甲醇发生反应的化学方程式为____ 。
(3)甲醇燃料电池装置示意图如图所示:
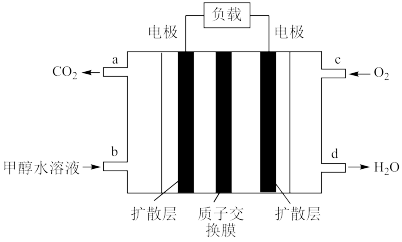
它可将化学能转变为电能,可作为笔记本电脑等能量的来源。在催化剂作用下甲醇转化为H2O和CO2。写出该电池工作时负极电极反应式:____ 。
(1)甲醇、乙烷沸点分别为65℃、-89℃,对比分析推测乙醇比丙烷沸点
(2)甲醇结构式如图,其分子中含a、b、c三种化学键。

①甲醇的官能团名称为
②甲醇分子中较易断裂的化学键是
③写出甲醇与钠反应的化学方程式
④在铜催化加热条件下,甲醇发生反应的化学方程式为
(3)甲醇燃料电池装置示意图如图所示:

它可将化学能转变为电能,可作为笔记本电脑等能量的来源。在催化剂作用下甲醇转化为H2O和CO2。写出该电池工作时负极电极反应式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。回答下列问题:
(1)镍元素在周期表中的位置为___________ ,基态镍原子未成对电子数为___________ 。
(2)区分晶体和非晶体最可靠的科学方法为___________ ;配合物Ni(CO)4熔点−19.3℃,沸点42.1℃,难溶于水,易溶于有机溶剂,结构见下图,则固态Ni(CO)4属于___________ 晶体,1mol Ni(CO)4含有___________ mol配位键。
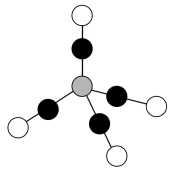
(3)NiO的晶体结构类型与NaCl相似,离子半径如下表所示:NiO晶胞中Ni2+的配位数为____ ,NiO的熔点比NaCl高的原因是______ 。
(4)某铬镍合金晶胞如图所示,Cr、Ni原子个数比为__ ,该晶胞中Cr、Ni原子最近距离为__ pm(用含a、c的代数式表示)。
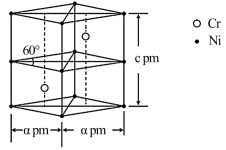
(1)镍元素在周期表中的位置为
(2)区分晶体和非晶体最可靠的科学方法为

(3)NiO的晶体结构类型与NaCl相似,离子半径如下表所示:NiO晶胞中Ni2+的配位数为
| Na+ | 102pm | Cl- | 181pm |
| Ni2+ | 69pm | O2− | 140pm |

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电于排布图为_______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4内界的配体中配位原子的VSEPR构型是_______ 。
②在[Ni(NH3)6]2+中H-N-H比NH3中H-N-H的键角_______ (选填“大”、“小”、“相等”或“无法判断”),原因是_______ 。
(3)镍白铜晶体中存在相互作用的微粒是_______ ,其作用是_______ 。
(4)某镍白铜合金的立方晶体结构如图所示:
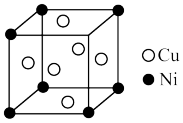
①晶胞中镍原子与铜原子的个数比为_______ 。
②若该合金的晶胞参数a pm,其密度为=_______ g/cm3。
(1)镍元素基态原子的价电于排布图为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4内界的配体中配位原子的VSEPR构型是
②在[Ni(NH3)6]2+中H-N-H比NH3中H-N-H的键角
(3)镍白铜晶体中存在相互作用的微粒是
(4)某镍白铜合金的立方晶体结构如图所示:

①晶胞中镍原子与铜原子的个数比为
②若该合金的晶胞参数a pm,其密度为=
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】氟化镁( )晶体广泛应用在光学、冶金、国防、医疗等领域。
)晶体广泛应用在光学、冶金、国防、医疗等领域。
(1)镁元素位于元素周期表_______ 区(填“s”“p”“d或“ds”)。
(2) 晶胞示意图中:a.○表示
晶胞示意图中:a.○表示_______ (填离子符号)。b.离子半径: 结合离子结构示意图解释原因:
结合离子结构示意图解释原因:______________ 。
(3)已知 晶胞体积为
晶胞体积为 啊伏伽德罗常数的值为
啊伏伽德罗常数的值为 ,则其晶体密度=
,则其晶体密度=_______  (用代数式表示)。
(用代数式表示)。
Ⅱ.一种由 制备
制备 的工艺流程如下
的工艺流程如下
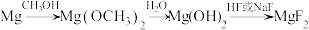
已知:i.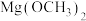 易溶于甲醇;
易溶于甲醇;
ii. ,
,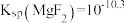 ,
,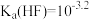
(4)上述流程中,可循环利用的物质是_______ 。
(5)比较相同条件下化学反应速率的大小:① 与
与 ;②
;② 与
与 。
。
a.小组同学预测化学反应速率:①<②,理由是甲基为_______ 基团,导致 键极性:
键极性: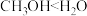 。
。
b.实验表明化学反应速率:①>②,分析其原因可能是:______________ 。
(6)上述流程中 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:__________ 。
 )晶体广泛应用在光学、冶金、国防、医疗等领域。
)晶体广泛应用在光学、冶金、国防、医疗等领域。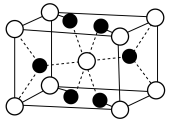
(1)镁元素位于元素周期表
(2)
 晶胞示意图中:a.○表示
晶胞示意图中:a.○表示 结合离子结构示意图解释原因:
结合离子结构示意图解释原因:(3)已知
 晶胞体积为
晶胞体积为 啊伏伽德罗常数的值为
啊伏伽德罗常数的值为 ,则其晶体密度=
,则其晶体密度= (用代数式表示)。
(用代数式表示)。Ⅱ.一种由
 制备
制备 的工艺流程如下
的工艺流程如下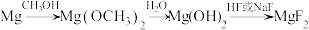
已知:i.
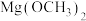 易溶于甲醇;
易溶于甲醇;ii.
 ,
,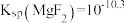 ,
,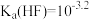
(4)上述流程中,可循环利用的物质是
(5)比较相同条件下化学反应速率的大小:①
 与
与 ;②
;② 与
与 。
。a.小组同学预测化学反应速率:①<②,理由是甲基为
 键极性:
键极性: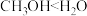 。
。b.实验表明化学反应速率:①>②,分析其原因可能是:
(6)上述流程中
 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:
您最近一年使用:0次



