25℃时,向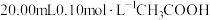 溶液中滴入
溶液中滴入 溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
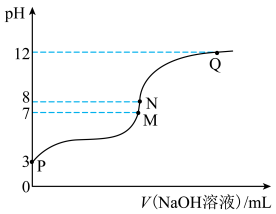
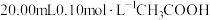 溶液中滴入
溶液中滴入 溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
A.25℃时, 的电离平衡常数 的电离平衡常数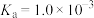 |
| B.M点对应的NaOH溶液体积为20.0mL |
| C.N点与Q点所示溶液中水的电离程度:N>Q |
D.N点所示溶液中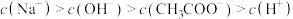 |
2017·宁夏石嘴山·三模 查看更多[12]
陕西省西安市阎良区关山中学2023-2024学年高二上学期第三次质量检测化学试题2023年广东省广州市高三化学冲刺训练题(二)广东省珠海市第一中学2023届高三5月模拟预测二化学试题广东省珠海市第一中学2023届高三下学期5月月考化学试题河南省周口市太康县2022-2023学年高二上学期1月期末考试化学试题(已下线)题型135 酸溶液与碱溶液互滴图像分析福建泉州城东中学、南安华侨中学、惠安高级中学、泉港第二中学2021-2022高三上学期期中考试化学试题广东省广州市2022届高三10月调研考化学试题山东省泰安市2020届高三第二次模拟考试化学试题江西省上饶中学2019-2020学年高二上学期期中考试(特零班)化学试题2018届广东省揭阳市高三上学期第一次月考化学试题宁夏石嘴山市第三中学2017届高三下学期第三次模拟考试理综化学试题
更新时间:2023-04-22 17:05:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
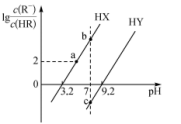
【推荐1】HX和HY均为一元弱酸,25℃条件下,分别向1 L1 mol·L-1HX溶液和HY溶液中缓慢加入NaOH固体(假设溶液温度及体积变化忽略不计),溶液的pH与lg 的关系如图所示(R代表X或Y),下列说法中正确的是
的关系如图所示(R代表X或Y),下列说法中正确的是
 的关系如图所示(R代表X或Y),下列说法中正确的是
的关系如图所示(R代表X或Y),下列说法中正确的是
| A.25℃时,HX电离常数的数量级为10-3 |
| B.溶液中Na+的浓度:b点>c点 |
| C.a点水电离出的氢离子浓度大于10-7 mol·L-1 |
| D.常温下,等浓度的NaY和HY等体积混合,所得溶液的pH<7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某溶液中有SO 、CO
、CO 、NH
、NH 、M,且SO
、M,且SO 、CO
、CO 、NH
、NH 的个数之比为1:2:4,离子M可能是
的个数之比为1:2:4,离子M可能是
 、CO
、CO 、NH
、NH 、M,且SO
、M,且SO 、CO
、CO 、NH
、NH 的个数之比为1:2:4,离子M可能是
的个数之比为1:2:4,离子M可能是| A.H+ | B.K+ | C.Cl- | D.Ba2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】草酸(H2C2O4)是一种二元弱酸。常温下向草酸溶液中滴加NaOH溶液,混合溶液中lgX[x表示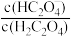 或
或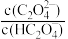 ]随pH的变化如图。下列说法中错误的是
]随pH的变化如图。下列说法中错误的是
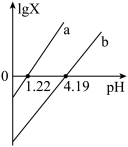
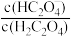 或
或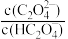 ]随pH的变化如图。下列说法中错误的是
]随pH的变化如图。下列说法中错误的是
| A.NaHC2O4溶液呈酸性 |
| B.H2C2O4第二步电离常数数量级是10-5 |
C.pH=7时,c(Na+)=c( )+2c( )+2c( ) ) |
D.1.22<pH<4.19时,c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,磷酸的Ka1=7.6×10-3、Ka2=6.3×10-8、Ka3=4.4×10-13。通过下列实验探究含磷化合物的性质。下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 蘸取0.1mol/LNaH2PO4溶液点在pH试纸上,pH<7;蘸取0.1mol/LNa2HPO4溶液点在pH试纸上,pH>7 |
| 2 | 向0.1mol/LNa2HPO4溶液中加入足量0.2mol/LCaCl2溶液,生成白色沉淀,蘸取上层清液点在pH试纸上,pH<7 |
| 3 | 将等浓度等体积的Na2HPO4、Na3HPO4溶液混合,pH>7 |
| 4 | 向0.1mol/LH3PO4溶液中滴加0.1mol/LNaOH溶液至pH=6 |
| A.实验1中,0.1mol/LNaH2PO4溶液中存在:Ka1•Ka2<Kw |
B.实验2中发生反应的离子方程式为2HPO +3Ca2+=Ca3(PO4)2↓+2H+ +3Ca2+=Ca3(PO4)2↓+2H+ |
C.实验3中存在5c(Na+)=2[c(H2PO )+c(HPO )+c(HPO )+c(H3PO4)+c(PO )+c(H3PO4)+c(PO )] )] |
D.实验4的过程中可能存在c(H2PO )>c(PO )>c(PO )>c(HPO )>c(HPO ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
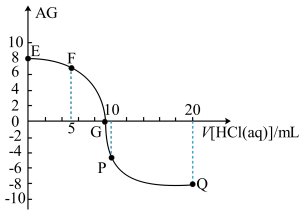
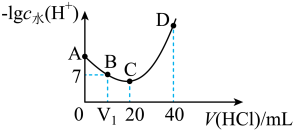
【推荐3】羟胺的电离方程式为:NH2OH+H2O NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL0.lmol/L胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(已知:lg3=0.5)。下列说法错误的是()
NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL0.lmol/L胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(已知:lg3=0.5)。下列说法错误的是()
 NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL0.lmol/L胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(已知:lg3=0.5)。下列说法错误的是()
NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL0.lmol/L胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(已知:lg3=0.5)。下列说法错误的是()
| A.图中V1<10 |
| B.A点对应溶液的pH=9.5 |
| C.A、B、C、D四点中酸性最强的点为C点 |
| D.E点对应溶液中存在:c(H+)=c(OH-)+c(NH3OH+)+2c(NH2OH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】证据推理是化学学科核心素养之一。下列基于反应事实的推理正确的是
| 酸的电离常数 | 反应事实(常温) |
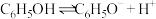  | ① ② 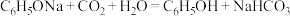 ③  |
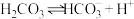 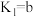  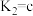 | |
  |
| A.a>b>c>d | B.d>b>c>a | C.b>c>d>a | D.d>b>a>c |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。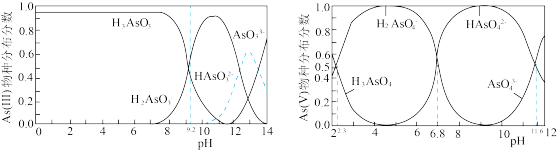 下列说法
下列说法不正确 的是
 下列说法
下列说法| A.常温下,酸性:H3AsO4>H3AsO3 |
B.常温下,H2AsO +H2AsO +H2AsO  HAsO HAsO +H3AsO3 K=102.4 +H3AsO3 K=102.4 |
C.常温下,pH=8时,溶液中c(H3AsO4):c(H2AsO ):c(HAsO ):c(HAsO ): c(AsO ): c(AsO )=1:105.7:106.9:103.3 )=1:105.7:106.9:103.3 |
| D.常温下,同浓度的Na3AsO4溶液与Na2HAsO3溶液,前者碱性强 |
您最近一年使用:0次


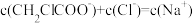
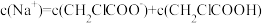
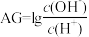 )与盐酸体积(V)之间的关系如图所示
)与盐酸体积(V)之间的关系如图所示