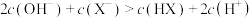25 ℃时,下列叙述中错误的是
A.0.1 mol·L-1NH4HS溶液中:c <c <c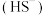 +c +c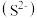 +c +c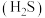 |
B.将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合后,c =c =c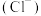 ,则NH3·H2O的电离常数为 ,则NH3·H2O的电离常数为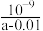 |
| C.10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20 mL |
D.pH相等的① 2SO4溶液,②NH4HSO4溶液,③NH4Cl溶液中,c 2SO4溶液,②NH4HSO4溶液,③NH4Cl溶液中,c 的大小关系:①>③>② 的大小关系:①>③>② |
更新时间:2023-08-15 09:12:44
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】常温下, 相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )
相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )
 相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )
相等的氨水、氯化铵、硫酸铵、硫酸氢铵四种溶液,溶液浓度最大的是( )| A.氨水 | B.氯化铵 | C.硫酸铵 | D.硫酸氢铵 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,在含有0.10
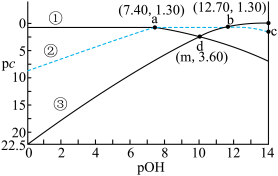
 的溶液中,所有含磷元素的微粒pc随pOH的变化关系如图所示。已知
的溶液中,所有含磷元素的微粒pc随pOH的变化关系如图所示。已知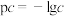 ,
,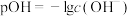 ,下列有关说法中正确的是
,下列有关说法中正确的是

 的溶液中,所有含磷元素的微粒pc随pOH的变化关系如图所示。已知
的溶液中,所有含磷元素的微粒pc随pOH的变化关系如图所示。已知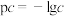 ,
,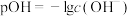 ,下列有关说法中正确的是
,下列有关说法中正确的是
A.曲线①代表 |
B. 溶液显碱性的原因是 溶液显碱性的原因是 的水解程度大于电离 的水解程度大于电离 |
C. 的 的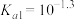 |
D.c点对应的溶液中: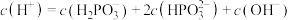 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,在特制容器中加入20mL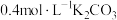 溶液,用
溶液,用 HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
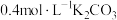 溶液,用
溶液,用 HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
A.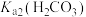 的数量级为 的数量级为 |
| B.滴定过程中,水的电离程度始终在减小 |
C.cd段反应的离子方程式为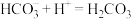 |
D.f点对应的溶液中存在: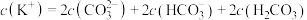 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】化学上常用AG表示溶液的酸碱度,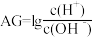 。25℃时用0.100mol·L-1NaOH溶液滴定20.00 mL 0.100mol·L-1HB溶液,AG与所加NaOH溶液的体积关系如图所示。下列说法正确的是
。25℃时用0.100mol·L-1NaOH溶液滴定20.00 mL 0.100mol·L-1HB溶液,AG与所加NaOH溶液的体积关系如图所示。下列说法正确的是
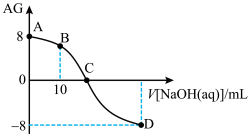
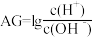 。25℃时用0.100mol·L-1NaOH溶液滴定20.00 mL 0.100mol·L-1HB溶液,AG与所加NaOH溶液的体积关系如图所示。下列说法正确的是
。25℃时用0.100mol·L-1NaOH溶液滴定20.00 mL 0.100mol·L-1HB溶液,AG与所加NaOH溶液的体积关系如图所示。下列说法正确的是
| A.C点时,加入NaOH溶液的体积为20.00 mL |
| B.B点溶液中存在c(H+)+c(HB) =c(B-)+c(OH-) |
| C.D点溶液中的pH=11 |
| D.25℃时,HB的电离平衡常数Ka=1.0×10-6 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】25℃时,向20mL浓度均为0.1mol•L-1的盐酸和醋酸的混合溶液中逐滴加入0.1mol•L-1的NaOH溶液(醋酸的Ka=1.8×10-5;用0.1mol•L-1的NaOH溶液滴定20mL等浓度的盐酸,滴定终点的pH突跃范围4.3~9.7)。下列说法不正确的是
| A.恰好中和时,溶液中醋酸根离子浓度为a,向其中加入0.002mol的醋酸钠固体,醋酸根离子浓度大于2a |
| B.滴加NaOH溶液至pH=4.3的过程中,发生反应的离子方程式为:H++OH-=H2O |
| C.滴定过程中,c(Cl-)=c(Ac-)+c(HAc) |
| D.pH=7时,c(Na+)>c(Cl-)>c(Ac-)>c(HAc) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】工业生产中,向Na2CO3溶液中通入SO2气体制备无水Na2SO3,水溶液中H2SO3、HSO3-、SO32-粒子的物质的量分数随pH的分布、Na2SO3的溶解度曲线如图所示:
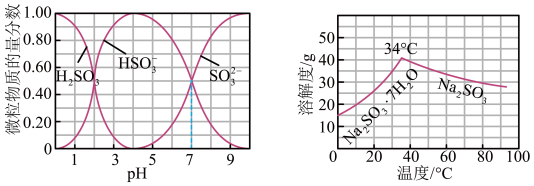
下列说法不正确 的是:

下列说法
| A.溶液pH=4时,溶质为NaHSO3 |
B.溶液pH=10时,c (Na+)+ c(H+)= c(OH–)+ c(SO32–)+ c(HSO3–) (Na+)+ c(H+)= c(OH–)+ c(SO32–)+ c(HSO3–) |
| C.溶液pH=7时, c(SO32–)= c(HSO3–) |
| D.溶液pH=10时,停止通入SO2,将溶液加热浓缩至有大量晶体析出,在高于34℃趁热过滤、洗涤、干燥得到无水Na2SO3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 是三元弱酸。室温下,向
是三元弱酸。室温下,向 的
的 溶液中滴加
溶液中滴加 溶液调节pH。混合溶液中
溶液调节pH。混合溶液中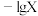 [表示
[表示 、
、 、
、 ]随溶液
]随溶液 的变化如图所示。下列说法不正确的是
的变化如图所示。下列说法不正确的是
 是三元弱酸。室温下,向
是三元弱酸。室温下,向 的
的 溶液中滴加
溶液中滴加 溶液调节pH。混合溶液中
溶液调节pH。混合溶液中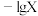 [表示
[表示 、
、 、
、 ]随溶液
]随溶液 的变化如图所示。下列说法不正确的是
的变化如图所示。下列说法不正确的是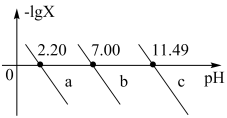
A.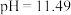 时, 时,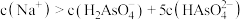 |
B.溶液中存在关系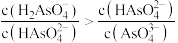 |
C.随着 的增大, 的增大, 保持不变 保持不变 |
D.常温下, 的 的 的数量级为 的数量级为 |
您最近一年使用:0次

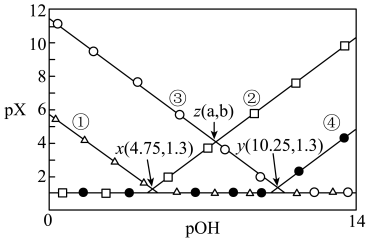
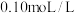 的
的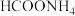 溶液中,
溶液中,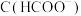 、
、 、
、 、
、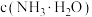 四种微粒的
四种微粒的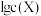 随
随 的变化关系如图,
的变化关系如图,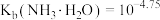 ,即当
,即当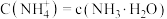 时,
时, 。
。
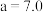
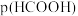 随
随 的变化关系
的变化关系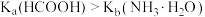
 和
和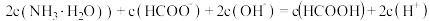
 的NaOH溶液分别滴定浓度均为
的NaOH溶液分别滴定浓度均为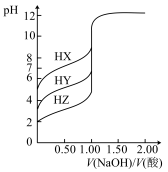
 的HZ溶液
的HZ溶液
 时,
时,