22号元素钛(Ti)的单质被誉为未来金属。工业冶炼Ti后的废渣中有SiO2和含Ti、Ca、Fe、Cu、Mg的化合物,从该废渣中回收Ti,并获得高附加值化工产品(MgF2、活性CaCO3、K2FeO4、X)的一种生产工艺如图所示:

已知:生产条件下MgF2的溶度积为9.0×10-9;NH4+时存在时,不易生成MgCO3沉淀,固体2中有CaCO3、Cu2(OH)2CO3和某含铁化合物。
(1)写出基态Ti原子的价电子排布式:_______ 。
(2)工艺设计要准确分析物质成分,科学加入试剂,准确把握用量,离子物质的量浓度≤1.0×10-5mol/L时,一般认为该离子沉淀完全。
①选择向固体1中加入盐酸而不加入硫酸的原因是_______ 。
②“析晶”过程是向深蓝色溶液3中先加入适量70%的H2SO4中和过量的氨水,再加入适量乙醇,得到深蓝色品体X,产品X的化学式是_______ 。
③“再溶”过程中加入强碱Y的稀溶液,溶液4中加入适量强碱Y的固体,强碱Y的化学式是_______ ;写出固体3“再溶”过程的离子方程式:________ 。
④测得溶液2中c(Mg2+)=0.030mol/L,要确保Mg2+沉淀完全,1L溶液2至少需加入NaF的物质的量为_______ mol(忽略溶液体积变化)。
(3)以上生产工艺中可循环利用的物质有NH3和_______ (填化学式)。
(4)活性碳酸钙晶胞为正方体结构,晶胞结构如图所示,黑点代表Ca2+,白色小圈代表CO ,晶胞边长为anm。
,晶胞边长为anm。

①活性碳酸钙晶体中一个CO 周围与其最近且等距的Ca2+的个数为
周围与其最近且等距的Ca2+的个数为_______ 。
②最近两个Ca2+之间的距离为_______ nm(用含a的代数式表示)。

已知:生产条件下MgF2的溶度积为9.0×10-9;NH4+时存在时,不易生成MgCO3沉淀,固体2中有CaCO3、Cu2(OH)2CO3和某含铁化合物。
(1)写出基态Ti原子的价电子排布式:
(2)工艺设计要准确分析物质成分,科学加入试剂,准确把握用量,离子物质的量浓度≤1.0×10-5mol/L时,一般认为该离子沉淀完全。
①选择向固体1中加入盐酸而不加入硫酸的原因是
②“析晶”过程是向深蓝色溶液3中先加入适量70%的H2SO4中和过量的氨水,再加入适量乙醇,得到深蓝色品体X,产品X的化学式是
③“再溶”过程中加入强碱Y的稀溶液,溶液4中加入适量强碱Y的固体,强碱Y的化学式是
④测得溶液2中c(Mg2+)=0.030mol/L,要确保Mg2+沉淀完全,1L溶液2至少需加入NaF的物质的量为
(3)以上生产工艺中可循环利用的物质有NH3和
(4)活性碳酸钙晶胞为正方体结构,晶胞结构如图所示,黑点代表Ca2+,白色小圈代表CO
 ,晶胞边长为anm。
,晶胞边长为anm。
①活性碳酸钙晶体中一个CO
 周围与其最近且等距的Ca2+的个数为
周围与其最近且等距的Ca2+的个数为②最近两个Ca2+之间的距离为
更新时间:2023-09-02 11:08:35
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO等,如图是从该矿渣中回收NiSO4的工艺路线:
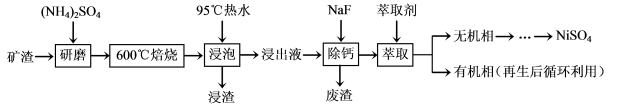
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3.锡(Sn)位于第五周期第ⅣA族。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是___________
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为___________ ,“浸渣”的成分除Fe2O3、FeO(OH)外还含有___________ (填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将Fe3+还原为Fe2+;除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式为___________ 。
(4)浸出液中c(Ca2+)=1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-)=___________ mol·L-1.[已知Ksp(CaF2)=4.0×10-11]
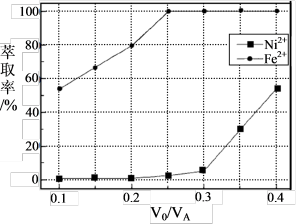
(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+萃取率的影响如图所示,V0/VA的最佳取值是___________ 。
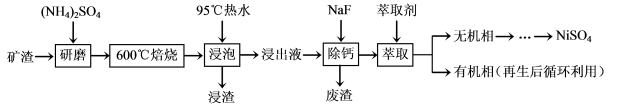
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3.锡(Sn)位于第五周期第ⅣA族。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将Fe3+还原为Fe2+;除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式为
(4)浸出液中c(Ca2+)=1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-)=
(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+萃取率的影响如图所示,V0/VA的最佳取值是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
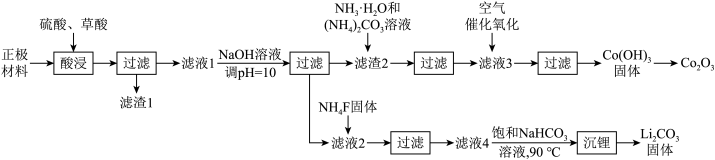
【推荐2】某化工厂利用废旧锂离子电池正极材料(含有LiCoO2以及少量Ca、Mg、Fe、Al等)制备Co2O3和Li2CO3.工艺流程如下: 如下表:
如下表:
②常温时, 的溶度积
的溶度积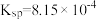 ,该数值随温度升高而减小。
,该数值随温度升高而减小。
(1)LiCoO2中Co元素的化合价为___________ ;基态Co原子的价层电子表示式为___________ 。
(2)“酸浸”时发生反应: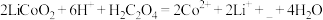 ,补充完整上述离子方程式
,补充完整上述离子方程式___________ 。
(3)已知滤渣2中含有 ,则常温下滤液2中
,则常温下滤液2中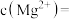
___________ mol/L。
(4)滤液3中含金属元素的离子主要是 ,通入空气发生催化氧化反应的离子方程式为
,通入空气发生催化氧化反应的离子方程式为___________ 。
(5)沉锂操作过程中的存在反应: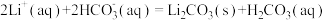 ,该操作中需将温度升高到90℃,原因是
,该操作中需将温度升高到90℃,原因是___________ 。
(6)由 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。 在晶胞中的位置为
在晶胞中的位置为___________ ;
②设阿伏加德罗常数的值为 。晶胞
。晶胞 的密度为b
的密度为b ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为___________ pm。
 如下表:
如下表:| 物质 |  |  |  |  |
 | 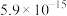 |  | 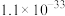 |  |
 的溶度积
的溶度积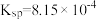 ,该数值随温度升高而减小。
,该数值随温度升高而减小。(1)LiCoO2中Co元素的化合价为
(2)“酸浸”时发生反应:
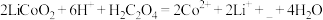 ,补充完整上述离子方程式
,补充完整上述离子方程式(3)已知滤渣2中含有
 ,则常温下滤液2中
,则常温下滤液2中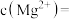
(4)滤液3中含金属元素的离子主要是
 ,通入空气发生催化氧化反应的离子方程式为
,通入空气发生催化氧化反应的离子方程式为(5)沉锂操作过程中的存在反应:
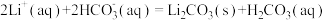 ,该操作中需将温度升高到90℃,原因是
,该操作中需将温度升高到90℃,原因是(6)由
 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。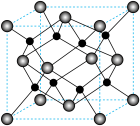
 在晶胞中的位置为
在晶胞中的位置为②设阿伏加德罗常数的值为
 。晶胞
。晶胞 的密度为b
的密度为b ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】锰的用途非常广泛,在钢铁工业中,锰的用量仅次于铁,90%的锰消耗于钢铁工业,10%的锰消耗于有色冶金、化工、电子、电池、农业等部门。以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、 钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:
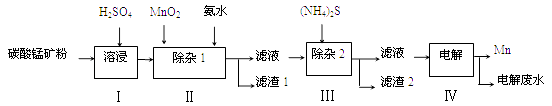
已知25℃,部分物质的溶度积常数如下:
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是_______________________ ;
(2)步骤Ⅰ中需要加入稍过量的硫酸,其目的有3点:①使矿物中的物质充分反应;②提供第Ⅱ步氧化时所需要的酸性环境;③________________ ;
(3)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+氧化为Fe3+,该反应的离子方程式是
__________________ ;加氨水调节溶液的pH为5.0~6.0,以除去Fe3+。
(4)步骤Ⅲ中,需要用到的玻璃仪器除玻璃棒、漏斗外,还有_________ ;滤渣2的主要成分是_________ ;
(5)电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降.欲使溶液中c(Mn2+)≤1.0×10-5 mol•L-1,则应保持溶液中c(S2-)≥_____ mol•L-1。

已知25℃,部分物质的溶度积常数如下:
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是
(2)步骤Ⅰ中需要加入稍过量的硫酸,其目的有3点:①使矿物中的物质充分反应;②提供第Ⅱ步氧化时所需要的酸性环境;③
(3)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+氧化为Fe3+,该反应的离子方程式是
(4)步骤Ⅲ中,需要用到的玻璃仪器除玻璃棒、漏斗外,还有
(5)电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降.欲使溶液中c(Mn2+)≤1.0×10-5 mol•L-1,则应保持溶液中c(S2-)≥
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】工业合成氨( )是人类科学技术的一项重大突破,对社会发展做出了巨大贡献。
)是人类科学技术的一项重大突破,对社会发展做出了巨大贡献。
(1)基态氮原子的价层电子排布图为______ 。
(2) 在水中的溶解度是常见气体中最大的。
在水中的溶解度是常见气体中最大的。
①下列因素与 的水溶性没有关系的是
的水溶性没有关系的是______ (填字母,下同)。
a. 和
和 都是极性分子
都是极性分子
b. 在水中易形成氢键
在水中易形成氢键
c. 溶于水建立了以下平衡:
溶于水建立了以下平衡:
d. 是一种易液化的气体
是一种易液化的气体
② 溶于水时,大部分
溶于水时,大部分 与
与 通过氢键结合形成
通过氢键结合形成 。根据氨水的性质推知
。根据氨水的性质推知 的结构式为
的结构式为______ 。
a. b.
b.
c. d.
d.
(3)肼的性质与氨气相似,易溶于水,可发生两步电离过程,第一步电离过程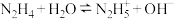 ,试写出第二步电离过程
,试写出第二步电离过程______ 。常温下,某浓度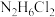 溶液的pH为4,则该溶液中水电离出的
溶液的pH为4,则该溶液中水电离出的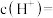
______ 。
(4)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注。

该反应历程中最大活化能对应骤的化学方程式为______ 。合成氨反应: 的
的
______ kJ/mol(用图中字母表示)
(5)合成氨反应中,正反应速率 ,逆反应速率
,逆反应速率 ,
, 、
、 为速率常数。正反应和逆反应的速率常数与温度的关系如图所示:
为速率常数。正反应和逆反应的速率常数与温度的关系如图所示:

①表示逆反应的速率常数与温度变化关系的曲线为______ (填“c”或“d”),理由为______ 。
②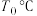 时,
时,
______
(6)用氨气研发燃料电池装置(如图所示),电池反应为 ,使用1mol/L的KOH溶液作电解质溶液,请写出通入a气体一极的电极反应式
,使用1mol/L的KOH溶液作电解质溶液,请写出通入a气体一极的电极反应式______ 。

 )是人类科学技术的一项重大突破,对社会发展做出了巨大贡献。
)是人类科学技术的一项重大突破,对社会发展做出了巨大贡献。(1)基态氮原子的价层电子排布图为
(2)
 在水中的溶解度是常见气体中最大的。
在水中的溶解度是常见气体中最大的。①下列因素与
 的水溶性没有关系的是
的水溶性没有关系的是a.
 和
和 都是极性分子
都是极性分子 b.
 在水中易形成氢键
在水中易形成氢键c.
 溶于水建立了以下平衡:
溶于水建立了以下平衡:
d.
 是一种易液化的气体
是一种易液化的气体②
 溶于水时,大部分
溶于水时,大部分 与
与 通过氢键结合形成
通过氢键结合形成 。根据氨水的性质推知
。根据氨水的性质推知 的结构式为
的结构式为a.
 b.
b.
c.
 d.
d.
(3)肼的性质与氨气相似,易溶于水,可发生两步电离过程,第一步电离过程
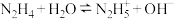 ,试写出第二步电离过程
,试写出第二步电离过程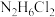 溶液的pH为4,则该溶液中水电离出的
溶液的pH为4,则该溶液中水电离出的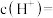
(4)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注。

该反应历程中最大活化能对应骤的化学方程式为
 的
的
(5)合成氨反应中,正反应速率
 ,逆反应速率
,逆反应速率 ,
, 、
、 为速率常数。正反应和逆反应的速率常数与温度的关系如图所示:
为速率常数。正反应和逆反应的速率常数与温度的关系如图所示:
①表示逆反应的速率常数与温度变化关系的曲线为
②
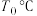 时,
时,
(6)用氨气研发燃料电池装置(如图所示),电池反应为
 ,使用1mol/L的KOH溶液作电解质溶液,请写出通入a气体一极的电极反应式
,使用1mol/L的KOH溶液作电解质溶液,请写出通入a气体一极的电极反应式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为___ 、___ 。
(2)XZ2与YZ2分子中X、Y的杂化方式分别是____ 和____ ,相同条件下两者在水中的溶解度较大的是___ (写分子式)。
(3)Q元素外围电子排布式为___ , [Q(H2O)4Br2] Br·2H2O中配位数为__ 。
(4)用氢键表示式任写一种E的氢化物溶液中存在的氢键_______________ 。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分子中X、Y的杂化方式分别是
(3)Q元素外围电子排布式为
(4)用氢键表示式任写一种E的氢化物溶液中存在的氢键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】卤族元素的化合物在科研和生产中有着重要的作用。请回答下列问题:
(1) (键角为180º)的中心Ⅰ原子价层电子对数为
(键角为180º)的中心Ⅰ原子价层电子对数为______ ;
______ (填“是”或“否”)具有极性;基态碘原子价电子排布式为______ 。
(2)物质磁性大小以磁矩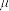 表示,
表示,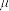 与未成对电子数之间的关系为:
与未成对电子数之间的关系为: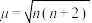 (n为未成对电子数)。配合物
(n为未成对电子数)。配合物 中配离子
中配离子 的
的 B.M(B.M磁矩单位),
B.M(B.M磁矩单位), 的杂化类型为
的杂化类型为______ 。
a. b.
b. c.
c.
配合物 中配离子
中配离子 的
的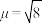 B.M,则配离子的空间构型为
B.M,则配离子的空间构型为______ 。
(3)在极高压强下,氯化钠可以和氯气化合生成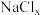 。
。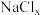 是立方系晶胞,结构如图所示,其中两个氯原子的坐标为
是立方系晶胞,结构如图所示,其中两个氯原子的坐标为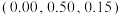 、
、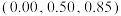 ,晶体的化学式为
,晶体的化学式为______ ;与Na距离最近的且相等的Cl有______ 个; 在晶体中键长为0.20nm,晶胞棱长为
在晶体中键长为0.20nm,晶胞棱长为______ nm(保留2位有效数字)。
(1)
 (键角为180º)的中心Ⅰ原子价层电子对数为
(键角为180º)的中心Ⅰ原子价层电子对数为
(2)物质磁性大小以磁矩
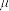 表示,
表示,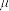 与未成对电子数之间的关系为:
与未成对电子数之间的关系为: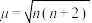 (n为未成对电子数)。配合物
(n为未成对电子数)。配合物 中配离子
中配离子 的
的 B.M(B.M磁矩单位),
B.M(B.M磁矩单位), 的杂化类型为
的杂化类型为a.
 b.
b. c.
c.
配合物
 中配离子
中配离子 的
的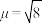 B.M,则配离子的空间构型为
B.M,则配离子的空间构型为(3)在极高压强下,氯化钠可以和氯气化合生成
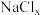 。
。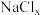 是立方系晶胞,结构如图所示,其中两个氯原子的坐标为
是立方系晶胞,结构如图所示,其中两个氯原子的坐标为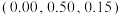 、
、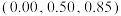 ,晶体的化学式为
,晶体的化学式为 在晶体中键长为0.20nm,晶胞棱长为
在晶体中键长为0.20nm,晶胞棱长为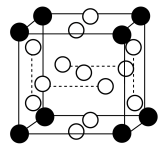
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】在庆祝中华人民共和国成立70 周年的阅兵仪式上,最后亮相的DF—31A洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了Fe、Cr、Ni、C 等多种元素。回答下列问题:
(1)基态铁原子的价电子排布式为___________ 。
(2)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表中的___________ 区。
(3)实验室常用KSCN溶液、苯酚( )检验
)检验 。其中N、O、S的第一电离能由大到小的顺序为
。其中N、O、S的第一电离能由大到小的顺序为___________ (用元素符号表示),苯酚中碳原子的杂化轨道类型为___________ 。
(4)铁元素能与CO形成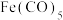 。羰基铁[
。羰基铁[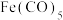 ]可用作催化剂、汽油抗爆剂等。1 mol
]可用作催化剂、汽油抗爆剂等。1 mol 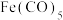 分子中含
分子中含___________ mol σ键,与CO互为等电子体的一种离子的化学式为___________ 。
(5)铬元素在地壳中含量占第21位,是一种重要的金属。根据价层电子判断铬元素中最高价态为___________ 价。已知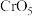 中铬元素为最高价态,画出其结构式:
中铬元素为最高价态,画出其结构式:___________ 。
(6)Ni可以形成多种氧化物,其中一种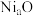 晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为
晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为 、
、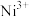 ,则晶体中
,则晶体中 与
与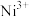 的最简整数比为
的最简整数比为___________ ,晶胞参数为428pm,则晶体密度为___________  (
( 表示阿伏加德罗常数的值,列出表达式)。
表示阿伏加德罗常数的值,列出表达式)。
(1)基态铁原子的价电子排布式为
(2)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表中的
(3)实验室常用KSCN溶液、苯酚(
 )检验
)检验 。其中N、O、S的第一电离能由大到小的顺序为
。其中N、O、S的第一电离能由大到小的顺序为(4)铁元素能与CO形成
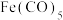 。羰基铁[
。羰基铁[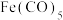 ]可用作催化剂、汽油抗爆剂等。1 mol
]可用作催化剂、汽油抗爆剂等。1 mol 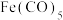 分子中含
分子中含(5)铬元素在地壳中含量占第21位,是一种重要的金属。根据价层电子判断铬元素中最高价态为
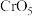 中铬元素为最高价态,画出其结构式:
中铬元素为最高价态,画出其结构式:(6)Ni可以形成多种氧化物,其中一种
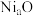 晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为
晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为 、
、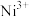 ,则晶体中
,则晶体中 与
与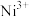 的最简整数比为
的最简整数比为 (
( 表示阿伏加德罗常数的值,列出表达式)。
表示阿伏加德罗常数的值,列出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氮、磷、钾是农作物生长的必须营养元素,磷和钙都是促成骨骼和牙齿的钙化不可缺少的营养元素。回答下列问题:
(1)基态K的核外电子排布式为____________ ,基态N的价电子排布图为____________ 。
(2)元素的第一电离能:Ca________ (填“>”或“<”)P。
(3)白磷P4在CS2中的溶解度________ (填“大于”或“小于”)在水中的溶解度,N4是氮的一种新型单质,若N4分子结构类似于白磷P4,则N的杂化方式为________ 。
(4)下表是几种碳酸盐的热分解温度和阳离子半径:
根据上表数据分析碳酸钡分解温度最高的原因是_______________________
(5)常温下PCl5是一种白色晶体,晶体结构为氯化铯型,由A、B两种离子构成。已知A、B两种离子分别与CCl4、SF6互为等电子体,则A、B两种离子的符号分别为________ 、________ 。
(6)用晶体的X射线衍射法可以测得阿伏加 德罗常数的值。已知金属钙的晶胞为面心立方(如图)晶胞,晶胞边长为d pm;又知钙的密度为ρ g/cm3,则一个钙晶胞的质量为________ (用d、ρ表示,下同)g,阿伏加 德罗常数的值为______________ (化成最简式)。

(1)基态K的核外电子排布式为
(2)元素的第一电离能:Ca
(3)白磷P4在CS2中的溶解度
(4)下表是几种碳酸盐的热分解温度和阳离子半径:
| 碳酸盐 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 900 | 1172 | 1360 |
| 阳离子半径/pm | 99 | 112 | 135 |
根据上表数据分析碳酸钡分解温度最高的原因是
(5)常温下PCl5是一种白色晶体,晶体结构为氯化铯型,由A、B两种离子构成。已知A、B两种离子分别与CCl4、SF6互为等电子体,则A、B两种离子的符号分别为
(6)用晶体的X射线衍射法可以测得阿伏加 德罗常数的值。已知金属钙的晶胞为面心立方(如图)晶胞,晶胞边长为d pm;又知钙的密度为ρ g/cm3,则一个钙晶胞的质量为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】I.以下物质中:①HF ②Cl2 ③H2O ④N2 ⑤C2H4
(1)既有极性键又有非极性键的是_______ 。
(2)只含有σ键的是_______ 。
(3)属于极性分子的是_______ 。
(4)属于非极性分子的是_______ 。
II.COCl2分子的结构式为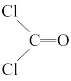
(5)COCl2分子内含有_______(填选项字母)。
III.超氧化钾的晶胞结构如图所示。

(6)则与K+等距离且最近的K+个数为_______ 。
(1)既有极性键又有非极性键的是
(2)只含有σ键的是
(3)属于极性分子的是
(4)属于非极性分子的是
II.COCl2分子的结构式为

(5)COCl2分子内含有_______(填选项字母)。
| A.4个σ键 | B.2个σ键、2个π键 |
| C.2个σ键、1个π键 | D.3个σ键、1个π键 |
III.超氧化钾的晶胞结构如图所示。

(6)则与K+等距离且最近的K+个数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】碱式硫酸锰[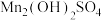 ]是一种重要的化工产品。以软锰矿烧渣(主要成分
]是一种重要的化工产品。以软锰矿烧渣(主要成分 、
、 、
、 、
、 )为原料制备碱式硫酸锰的工艺流程如下:
)为原料制备碱式硫酸锰的工艺流程如下:

已知:①“酸浸”时, 转化为
转化为
②Mn(Ⅱ)在碱性环境中易被氧化
③常温下,溶液中金属离子沉淀的pH如下表所示:
(1)为提高“酸浸”效率,可采取的措施有______ (任写一点)。
(2)“水浸”过程中, 与水反应产生了气体,写出该反应的化学方程式
与水反应产生了气体,写出该反应的化学方程式______ 。
(3)“调pH”时理论范围为______ (当溶液中离子浓度 时,认为沉淀完全)。当溶液中
时,认为沉淀完全)。当溶液中 已沉淀完全时,
已沉淀完全时,
______ mol/L( )。
)。
(4)“合成”时应先充入惰性气体的原因是______ ,“合成”过程中发生的主要反应的化学方程式为______ 。
(5)为测定粗产品中锰的含量,取1.0g粗产品于烧杯中,加入足量稀硫酸溶解,滴加过量0.1000mol/L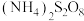 溶液,将锰元素转化为
溶液,将锰元素转化为 ,充分反应后加热一段时间,冷却后将烧杯中的溶液全部转移至250mL容量瓶中定容。取25.00mL溶液于锥形瓶中,用0.1000mol/L
,充分反应后加热一段时间,冷却后将烧杯中的溶液全部转移至250mL容量瓶中定容。取25.00mL溶液于锥形瓶中,用0.1000mol/L 标准溶液滴定,平行滴定三次,消耗
标准溶液滴定,平行滴定三次,消耗 溶液体积的平均值为25.30mL,则该产品中锰元素的质量分数为
溶液体积的平均值为25.30mL,则该产品中锰元素的质量分数为______ (保留一位小数)。
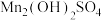 ]是一种重要的化工产品。以软锰矿烧渣(主要成分
]是一种重要的化工产品。以软锰矿烧渣(主要成分 、
、 、
、 、
、 )为原料制备碱式硫酸锰的工艺流程如下:
)为原料制备碱式硫酸锰的工艺流程如下:
已知:①“酸浸”时,
 转化为
转化为
②Mn(Ⅱ)在碱性环境中易被氧化
③常温下,溶液中金属离子沉淀的pH如下表所示:
金属离子 |
|
|
|
|
开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
(2)“水浸”过程中,
 与水反应产生了气体,写出该反应的化学方程式
与水反应产生了气体,写出该反应的化学方程式(3)“调pH”时理论范围为
 时,认为沉淀完全)。当溶液中
时,认为沉淀完全)。当溶液中 已沉淀完全时,
已沉淀完全时,
 )。
)。(4)“合成”时应先充入惰性气体的原因是
(5)为测定粗产品中锰的含量,取1.0g粗产品于烧杯中,加入足量稀硫酸溶解,滴加过量0.1000mol/L
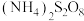 溶液,将锰元素转化为
溶液,将锰元素转化为 ,充分反应后加热一段时间,冷却后将烧杯中的溶液全部转移至250mL容量瓶中定容。取25.00mL溶液于锥形瓶中,用0.1000mol/L
,充分反应后加热一段时间,冷却后将烧杯中的溶液全部转移至250mL容量瓶中定容。取25.00mL溶液于锥形瓶中,用0.1000mol/L 标准溶液滴定,平行滴定三次,消耗
标准溶液滴定,平行滴定三次,消耗 溶液体积的平均值为25.30mL,则该产品中锰元素的质量分数为
溶液体积的平均值为25.30mL,则该产品中锰元素的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
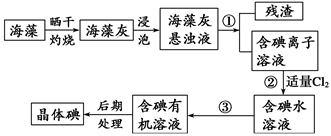
(1)实验室焙烧海带,需要下列仪器中的_______________ (填序号)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)提取碘的过程中有关的实验操作名称:①_______________ ,③_______________ 。
(3)提取碘的过程中,不能选择乙醇作有机萃取剂的原因是_____________________ 。
(4)第③步时使用的主要玻璃仪器有_______________________ 。
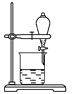
(5)小组用CCl4萃取碘水中的碘,在下图的分液漏斗中,下层液体呈______ 色;他们打开分液漏斗活塞,却未见液体流下,原因可能是_________________ 。
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
①_____________________________________________ ;
②_____________________________________________ 。
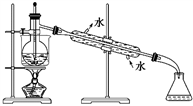
(7)进行上述蒸馏操作时,使用水浴加热的原因是_____________________________ ,
最后晶态碘在蒸馏烧瓶里聚集。证明得到的固体是碘单质的化学方法是_______________ 。

(1)实验室焙烧海带,需要下列仪器中的
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)提取碘的过程中有关的实验操作名称:①
(3)提取碘的过程中,不能选择乙醇作有机萃取剂的原因是
(4)第③步时使用的主要玻璃仪器有
(5)小组用CCl4萃取碘水中的碘,在下图的分液漏斗中,下层液体呈

(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
①
②

(7)进行上述蒸馏操作时,使用水浴加热的原因是
最后晶态碘在蒸馏烧瓶里聚集。证明得到的固体是碘单质的化学方法是
您最近一年使用:0次
【推荐3】用如下方法回收废旧CPU中的单质Au(金)、Ag和Cu。
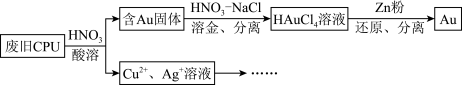
已知:①浓硝酸不能单独将Au溶解。
② 。
。
(1)酸溶后经_______ 操作,将混合物分离。
(2)浓、稀HNO3均可作酸溶试剂,浓硝酸被还原成NO2,稀硝酸被还原成NO。溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量少的反应的化学方程式:_______ 。
(3)HNO3-NaCl与王水[V(浓硝酸):V(浓盐酸)=1∶3]溶金原理相同,Cl-与Au3+形成配离子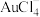 ,促进了金溶解。
,促进了金溶解。
①将溶金反应的化学方程式补充完整:_______ 。
 _______
_______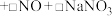
②关于溶金的下列说法正确的是_______ 。
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)若用Zn粉将溶液中的1 mol HAuCl4完全还原,则参加反应的Zn的物质的量是_____ mol。
(5)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如下方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。
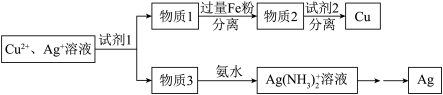
试剂1是_______ ,物质2是_______ ,物质3是_______ 。

已知:①浓硝酸不能单独将Au溶解。
②
 。
。(1)酸溶后经
(2)浓、稀HNO3均可作酸溶试剂,浓硝酸被还原成NO2,稀硝酸被还原成NO。溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量少的反应的化学方程式:
(3)HNO3-NaCl与王水[V(浓硝酸):V(浓盐酸)=1∶3]溶金原理相同,Cl-与Au3+形成配离子
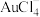 ,促进了金溶解。
,促进了金溶解。①将溶金反应的化学方程式补充完整:
 _______
_______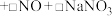
②关于溶金的下列说法正确的是
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)若用Zn粉将溶液中的1 mol HAuCl4完全还原,则参加反应的Zn的物质的量是
(5)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如下方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。

试剂1是
您最近一年使用:0次






