盐酸肼(N2H6Cl2)属于离子化合物,易溶于水,溶液呈酸性,水解原理与 类似。
类似。
(1)盐酸肼第一步水解反应的离子方程式___________ 。
(2)盐酸肼水溶液中离子浓度的排列顺序正确的是___________(选填编号)。
 类似。
类似。(1)盐酸肼第一步水解反应的离子方程式
(2)盐酸肼水溶液中离子浓度的排列顺序正确的是___________(选填编号)。
A.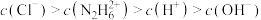 |
B. |
C. |
D.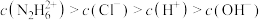 |
更新时间:2023-10-19 09:38:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有两条途径可以使重晶石(BaSO4)转化为碳酸钡,如图示:

试回答下列问题:
(1)反应1中发生的主要反应为:BaSO4+4C=BaS+4CO,若1molBaSO4完全反应,电子转移的物质的量为___ 。
(2)Na2CO3溶液的pH大于10,用离子方程式说明其主要原因___ ,其溶液中离子浓度由大到小的顺序为___ 。
(3)已知反应4中发生的反应为:BaSO4(s)+CO (g)=BaCO3(s)+SO
(g)=BaCO3(s)+SO (g),写出此反应平衡常数表达式K=
(g),写出此反应平衡常数表达式K=___ ;若Ksp(BaSO4)=1×10-10mol2·L-2,Ksp(BaCO3)=5×10-9mol2·L-2,则K的值为___ 。
(4)若每次加入1L2mol•L-1的Na2CO3溶液,至少需要___ 次可将0.2molBaSO4转化为BaCO3。

试回答下列问题:
(1)反应1中发生的主要反应为:BaSO4+4C=BaS+4CO,若1molBaSO4完全反应,电子转移的物质的量为
(2)Na2CO3溶液的pH大于10,用离子方程式说明其主要原因
(3)已知反应4中发生的反应为:BaSO4(s)+CO
 (g)=BaCO3(s)+SO
(g)=BaCO3(s)+SO (g),写出此反应平衡常数表达式K=
(g),写出此反应平衡常数表达式K=(4)若每次加入1L2mol•L-1的Na2CO3溶液,至少需要
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用所学化学反应原理,解决以下问题:
(1)KAl(SO4)2·12H2O可做净水剂,其原理是____________________________________ (用离子方程式表示)
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是__________ (填化学式)。
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式_____________ 。
(4)将AgCl分别放入①5 mL H2O ②10 mL 0.2 mol·L-1 MgCl2溶液 ③20 mL 0.5 mol·L-1 NaCl溶液④40 mL 0.1 mol·L-1 HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是______ (用序号填空)。
(5)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合:若c(K+)<c (CH3COO-),则a_____________ b(填>、<、=)。
(6)室温下,1 mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是_________________________ (用序号填空)。
(1)KAl(SO4)2·12H2O可做净水剂,其原理是
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式
(4)将AgCl分别放入①5 mL H2O ②10 mL 0.2 mol·L-1 MgCl2溶液 ③20 mL 0.5 mol·L-1 NaCl溶液④40 mL 0.1 mol·L-1 HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是
(5)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合:若c(K+)<c (CH3COO-),则a
(6)室温下,1 mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有HA、HB、HC三种一元弱酸,分析并回答下列问题:
①等PH值的三种酸,加水稀释的PH值变化如图比较三种酸的酸性强弱_________ 〉___________ 〉__________ 三种酸的物质的量浓度由大到小的顺序___________ 。

②同浓度的NaA, NaB, NaC,PH值的大小_____________ 〉_____________ 〉__________ 。
③25℃时若已知NH4B的溶液显中性,则NH4A溶液的PH值__________ 7,写出NH4C的水解的离子方程式______________________________ 。
④PH=2的HA与PH=12的NaOH等体积混合后,溶液中离子浓度由大到小的顺序是______ 。
①等PH值的三种酸,加水稀释的PH值变化如图比较三种酸的酸性强弱

②同浓度的NaA, NaB, NaC,PH值的大小
③25℃时若已知NH4B的溶液显中性,则NH4A溶液的PH值
④PH=2的HA与PH=12的NaOH等体积混合后,溶液中离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】向一定体积CaCl2和HCl的混合溶液中逐滴加入浓度为1 mol·L-1的Na2CO3溶液,反应过程中加入的Na2CO3溶液的体积与产生沉淀或气体的质量关系如图所示。

已知图中V1∶V2=1∶2;当加入V2 mL Na2CO3溶液时,所得溶液的浓度为1 mol·L-1,体积为200 mL。求:
(1)加入V2 mL Na2CO3溶液时,所得溶液的溶质是________ 。
(2)原混合溶液中CaCl2和HCl的物质的量之比n(CaCl2)∶n(HCl)=________ 。
(3)m1=________ g,m2=________ g。

已知图中V1∶V2=1∶2;当加入V2 mL Na2CO3溶液时,所得溶液的浓度为1 mol·L-1,体积为200 mL。求:
(1)加入V2 mL Na2CO3溶液时,所得溶液的溶质是
(2)原混合溶液中CaCl2和HCl的物质的量之比n(CaCl2)∶n(HCl)=
(3)m1=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某二元酸(化学式用H2B表示)在水中的电离方程式如下:H2B=H++HB−、HB−⇌H++B2−,回答下列问题:
(1)Na2B溶液显____ (填“酸性”“中性”或“碱性”),理由是___ (用离子方程式表示)。
(2)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是_____ 。
A.c(B2−)+c(HB−)+c(H2B)=0.1mol/L
B.c(Na+)+c(OH−)=c(H+)+c(HB−)
C.c(Na+)+c(H+)=c(OH−)+c(HB−)+2c(B2−)
D.c(Na+)=2c(B2−)+2c(HB−)
(3)已知0.1mol/LNaHB溶液的pH=2,则0.1mol/LH2B溶液中氢离子的物质的量浓度可能是___ 0.11mol/L(填“<”“>”或“=”)。
(4)0.1mol/LNaHB溶液中各种离子浓度由大到小的顺序是____ 。
(1)Na2B溶液显
(2)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是
A.c(B2−)+c(HB−)+c(H2B)=0.1mol/L
B.c(Na+)+c(OH−)=c(H+)+c(HB−)
C.c(Na+)+c(H+)=c(OH−)+c(HB−)+2c(B2−)
D.c(Na+)=2c(B2−)+2c(HB−)
(3)已知0.1mol/LNaHB溶液的pH=2,则0.1mol/LH2B溶液中氢离子的物质的量浓度可能是
(4)0.1mol/LNaHB溶液中各种离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】常温下,将某一元酸 HA 和 NaOH 溶液等体积混合,两种溶液的浓度和混合后所得溶液的 pH 如下表,请回答:
(1) 不考虑其它组的实验结果,单从甲组情况分析,如何用 a (混合溶液的 pH)来说明HA 是强酸还是弱酸_____ 。
(2)不考虑其它组的实验结果,单从乙组情况分析,c 是否一定等于 0.2_____ (选填“是” 或“否”),混合液中离子浓度 c(A−)与 c(Na+)的大小关系是_____ 。
(3)丙组实验结果分析,HA 是_____ 酸(选填“强”或“弱”).该混合溶液中离子浓度 由大到小的顺序是_____ 。
(4)丁组实验所得混合溶液中由水电离出的c(OH−) =_____ mol · L−1,写出该混合溶液中下列算式的精确结果(不需做近似计算).c(Na+) − c(A−) =_________ mol · L−1 ,c(OH−) − c(HA) =________ mol · L−1。
| 实验编号 | HA物质的量浓度 (mol·L-1) | NaOH物质的量浓度 (mol·L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
(1) 不考虑其它组的实验结果,单从甲组情况分析,如何用 a (混合溶液的 pH)来说明HA 是强酸还是弱酸
(2)不考虑其它组的实验结果,单从乙组情况分析,c 是否一定等于 0.2
(3)丙组实验结果分析,HA 是
(4)丁组实验所得混合溶液中由水电离出的c(OH−) =
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】相同条件下,下列五种溶液:①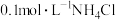 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④  氨水 ⑤
氨水 ⑤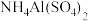 溶液,请根据要求填写下列空白:
溶液,请根据要求填写下列空白:
(1)溶液①呈_______ ,其原因是_______ (用离子方程式表示)。
(2)溶液①②③④中 由大到小的顺序是
由大到小的顺序是_______
(3) 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中 ,则溶液显
,则溶液显_______ 性(填“酸”“碱”或“中”);
(4)常温下,某水溶液M中存在的离子有 、
、 、
、 、
、 、
、 ,存在的分子有
,存在的分子有 、
、
①写出酸 的电离方程式:
的电离方程式:_______ 。
②若溶液M由 溶液与
溶液与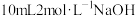 溶液混合而得,请写出溶液中各离子浓度大小关系
溶液混合而得,请写出溶液中各离子浓度大小关系_______ 。
(5)常温下,已知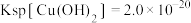 ,某
,某 溶液里
溶液里 ,如果要生成
,如果要生成  沉淀,则应调整溶液
沉淀,则应调整溶液 大于
大于 _______ 。
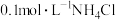 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④  氨水 ⑤
氨水 ⑤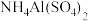 溶液,请根据要求填写下列空白:
溶液,请根据要求填写下列空白:(1)溶液①呈
(2)溶液①②③④中
 由大到小的顺序是
由大到小的顺序是(3)
 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中 ,则溶液显
,则溶液显(4)常温下,某水溶液M中存在的离子有
 、
、 、
、 、
、 、
、 ,存在的分子有
,存在的分子有 、
、
①写出酸
 的电离方程式:
的电离方程式:②若溶液M由
 溶液与
溶液与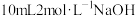 溶液混合而得,请写出溶液中各离子浓度大小关系
溶液混合而得,请写出溶液中各离子浓度大小关系(5)常温下,已知
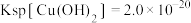 ,某
,某 溶液里
溶液里 ,如果要生成
,如果要生成  沉淀,则应调整溶液
沉淀,则应调整溶液 大于
大于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,在25mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如下图所示。

(1)该氢氧化钠溶液的物质的量浓度为___________  。
。
(2)在B点,a___________ 12.5mL(填“>”、“<”或“=”,下同)。若由体积相等的氢氧化钠溶液和醋酸溶液混合而且恰好呈中性,则混合前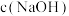
___________ 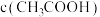 。
。
(3)在D点,溶液中离子浓度大小关系为:___________ ,还满足
___________  。
。

(1)该氢氧化钠溶液的物质的量浓度为
 。
。(2)在B点,a
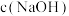
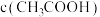 。
。(3)在D点,溶液中离子浓度大小关系为:

 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.现有常温下pH=2的HCl溶液甲和pH=2的CH3COOH溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是_____ 。
A.c(H+) B. C.c(H+)·c(OH-)
C.c(H+)·c(OH-)
(2)取10mL的乙溶液,加入等体积的水,CH3COOH的电离平衡________ (填“向左”“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中 的比值将
的比值将________ (填“增大”“减小”或“无法确定”)。
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗NaOH溶液体积的大小关系为V(甲)________ (填“>”“<”或“=”)V(乙)。
(4)已知25℃时,下列酸的电离平衡常数如下:
下列四种离子结合H+能力最强的是________ 。
A.HCO B.CO
B.CO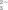 C.ClO- D.CH3COO-
C.ClO- D.CH3COO-
写出下列反应的离子方程式:HClO+Na2CO3(少量):______________________
Ⅱ.室温下,0.1 mol·L-l的KOH溶液滴10.00mL 0.10 mol·L-l H2C2O4 (二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:
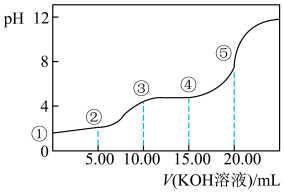
(5)点③所示溶液中所有离子的浓度由大到小的顺序为:________________________ 。点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4−)+c(C2O42−)=________ mol/L。
(1)常温下0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+) B.
 C.c(H+)·c(OH-)
C.c(H+)·c(OH-) (2)取10mL的乙溶液,加入等体积的水,CH3COOH的电离平衡
 的比值将
的比值将(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗NaOH溶液体积的大小关系为V(甲)
(4)已知25℃时,下列酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=4.7×10-11 | 3.0×10-8 |
下列四种离子结合H+能力最强的是
A.HCO
 B.CO
B.CO C.ClO- D.CH3COO-
C.ClO- D.CH3COO-写出下列反应的离子方程式:HClO+Na2CO3(少量):
Ⅱ.室温下,0.1 mol·L-l的KOH溶液滴10.00mL 0.10 mol·L-l H2C2O4 (二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:

(5)点③所示溶液中所有离子的浓度由大到小的顺序为:
您最近一年使用:0次



