金属钛素有“太空金属”、“海洋金属”、“未来金属”等美誉,我国有丰富的钛矿资源。一种以钛铁矿 ,含
,含 ,等杂质)为主要原料制备钛白粉
,等杂质)为主要原料制备钛白粉 的工艺流程如下图所示。
的工艺流程如下图所示。
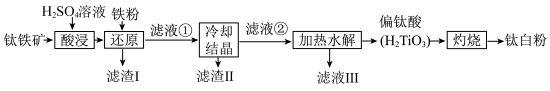
已知:① 不溶于水和稀酸;
不溶于水和稀酸;
②“酸浸”后钛元素主要以 形式存在;
形式存在;
③ 在
在 时生成沉淀,
时生成沉淀, 时沉淀完全。
时沉淀完全。
回答下列问题:
(1)提高“酸浸”浸出率的方法有___________ 。
(2)写出“酸浸”操作 发生反应的化学方程式
发生反应的化学方程式___________ 。
(3)滤渣Ⅰ的主要成分为___________ (填写化学式)。
(4)该流程中常加入铁粉来还原体系中的 。某课题研究小组为探究最佳反应条件,在保持相同的反应时间的条件下获得如下探究结果。图A为保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随pH的变化图,图B为保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随温度的变化图)
。某课题研究小组为探究最佳反应条件,在保持相同的反应时间的条件下获得如下探究结果。图A为保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随pH的变化图,图B为保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随温度的变化图)

①分析图A中M点以后体系中Fe(Ⅲ)含量随pH增大而增大的原因___________ 。
②图B所示还原体系中Fe(Ⅲ)的最佳反应温度是___________ ℃。
(5)经处理后,流程中可循环利用有___________ (填写化学式)。
(6)一种电解法制钛的工艺如下图所示,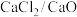 共熔体为介质,在阴极被还原的钙进一步还原
共熔体为介质,在阴极被还原的钙进一步还原 得到钛,在阴极制取钛的相关反应方程式为
得到钛,在阴极制取钛的相关反应方程式为___________ 。

 ,含
,含 ,等杂质)为主要原料制备钛白粉
,等杂质)为主要原料制备钛白粉 的工艺流程如下图所示。
的工艺流程如下图所示。
已知:①
 不溶于水和稀酸;
不溶于水和稀酸;②“酸浸”后钛元素主要以
 形式存在;
形式存在;③
 在
在 时生成沉淀,
时生成沉淀, 时沉淀完全。
时沉淀完全。回答下列问题:
(1)提高“酸浸”浸出率的方法有
(2)写出“酸浸”操作
 发生反应的化学方程式
发生反应的化学方程式(3)滤渣Ⅰ的主要成分为
(4)该流程中常加入铁粉来还原体系中的
 。某课题研究小组为探究最佳反应条件,在保持相同的反应时间的条件下获得如下探究结果。图A为保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随pH的变化图,图B为保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随温度的变化图)
。某课题研究小组为探究最佳反应条件,在保持相同的反应时间的条件下获得如下探究结果。图A为保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随pH的变化图,图B为保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随温度的变化图)
①分析图A中M点以后体系中Fe(Ⅲ)含量随pH增大而增大的原因
②图B所示还原体系中Fe(Ⅲ)的最佳反应温度是
(5)经处理后,流程中可循环利用有
(6)一种电解法制钛的工艺如下图所示,
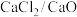 共熔体为介质,在阴极被还原的钙进一步还原
共熔体为介质,在阴极被还原的钙进一步还原 得到钛,在阴极制取钛的相关反应方程式为
得到钛,在阴极制取钛的相关反应方程式为
更新时间:2023-12-02 11:49:28
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】高纯二氧化硅可用来制造光纤。某蛇纹石的成分见下表:
通过下图流程可由蛇纹石制备较纯净的二氧化硅。
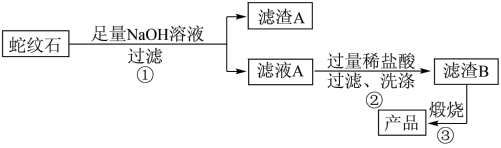
(1)蛇纹石中涉及的可溶性金属氧化物有_______ (写化学式)。
(2)步骤①中涉及SiO2反应的离子方程式为_______ 。
(3)滤渣 的成分有
的成分有_______ (填化学式)。
(4)步骤②中洗涤沉淀的方法是_______
(5)步骤③反应的化学方程式为____ ;实验室进行步骤③需要用到的主要仪器有____ 、泥三角、酒精灯和____
| 组分 | SiO2 | MgO | Na2O | K2O | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.8 |

(1)蛇纹石中涉及的可溶性金属氧化物有
(2)步骤①中涉及SiO2反应的离子方程式为
(3)滤渣
 的成分有
的成分有(4)步骤②中洗涤沉淀的方法是
(5)步骤③反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】一种利用钛铁矿(主要成分为FeTiO3,还含有少量Fe2O3)联合生产铁红和钛白粉的工艺流程如图所示,回答下列问题:
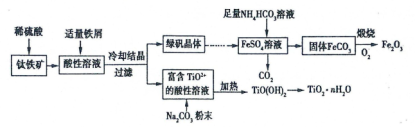
(1)为加快钛铁矿在稀硫酸中的溶解,可采取的措施有______ 任写两种)。
(2)FeSO4溶液与 NH4HCO3溶液反应的离子方程式是________ 。
(3)TiO2+水解为TiO(OH)2沉淀的离子方程式为__________ ,需要加入Na2CO3粉末的目的是__________________________________________ 。
(4)常温下,在生成的FeCO3达到沉淀溶解平衡的溶液中,测得溶液中c(CO32-) = 3.0×10-6 mol/L,需要控制溶液pH____________ 时,才能使所得的FeCO3中不含Fe(OH)2。(已知:Ksp[FeCO3] = 3.0×10-11,Ksp[Fe(OH)2] = 1.0×10-16)

(1)为加快钛铁矿在稀硫酸中的溶解,可采取的措施有
(2)FeSO4溶液与 NH4HCO3溶液反应的离子方程式是
(3)TiO2+水解为TiO(OH)2沉淀的离子方程式为
(4)常温下,在生成的FeCO3达到沉淀溶解平衡的溶液中,测得溶液中c(CO32-) = 3.0×10-6 mol/L,需要控制溶液pH
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。请根据信息回答下列问题:
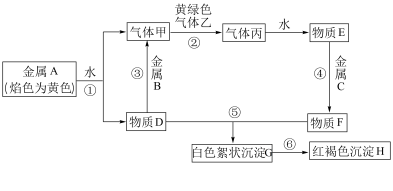
已知:铝和氢氧化钠溶液反应生成气体。
(1)用湿润的淀粉碘化钾试纸检验气体乙的原理:___________ (用离子方程式表示)。
(2)写出金属C和水蒸气在高温条件下反应的化学方程式___________ 。
(3)写出反应⑥的化学方程式___________ 。
(4)金属A的某种含氧化物可用作供氧剂,写出其与 反应的化学方程式并用双线桥标出电子转移的方向和数目
反应的化学方程式并用双线桥标出电子转移的方向和数目___________ 。
(5)向 某浓度的D溶液中缓慢通入一定量的
某浓度的D溶液中缓慢通入一定量的 ,充分反应后,得到
,充分反应后,得到 和
和 的混合溶液丁。向上述所得溶液中,逐滴滴加
的混合溶液丁。向上述所得溶液中,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
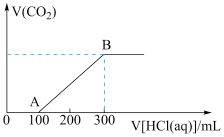
生成混合溶液丁对应的离子方程式为___________ ,B点溶液中溶质的物质的量浓度(体积变化忽略不计)___________ 。

已知:铝和氢氧化钠溶液反应生成气体。
(1)用湿润的淀粉碘化钾试纸检验气体乙的原理:
(2)写出金属C和水蒸气在高温条件下反应的化学方程式
(3)写出反应⑥的化学方程式
(4)金属A的某种含氧化物可用作供氧剂,写出其与
 反应的化学方程式并用双线桥标出电子转移的方向和数目
反应的化学方程式并用双线桥标出电子转移的方向和数目(5)向
 某浓度的D溶液中缓慢通入一定量的
某浓度的D溶液中缓慢通入一定量的 ,充分反应后,得到
,充分反应后,得到 和
和 的混合溶液丁。向上述所得溶液中,逐滴滴加
的混合溶液丁。向上述所得溶液中,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
生成混合溶液丁对应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某金属A及其化合物之间有如下的转化关系:

(1)写出A、B的化学式:A_______ ,B_________ 。
(2)写出B→D的化学方程式_______________________________ 。
(3)写出B→C的离子方程式________________________________ 。
(4)写出E→C的化学方程式________________________________ 。

(1)写出A、B的化学式:A
(2)写出B→D的化学方程式
(3)写出B→C的离子方程式
(4)写出E→C的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】部分物质间的转化关系如下图所示(部分物质已省略。已知A→B是实验室制取黄绿色气体的主要方法之一,H的焰色呈黄色,请完成下列填空。
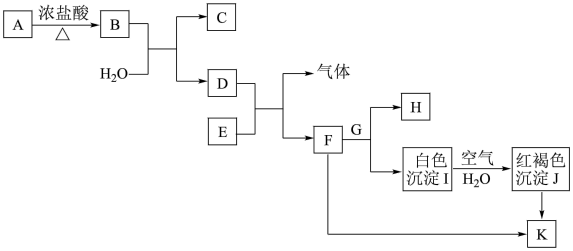
(1)检验F溶液中阳离子的试剂是_______ 。若Cu2+中含有F中阳离子的杂质,应加入_______ (填化学式)除杂。
(2)Ⅰ转化为J的化学方程式为_______ 。
(3)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
(4)当前,新冠病毒变异毒株奥密克戎来势汹汹,化学消毒剂在疫情防控中起着重要作用。
①目前,很多自来水厂用黄绿色气体来杀菌、消毒。A→B的离子反应方程式为_______ 。
②C可以杀菌、消毒,但不稳定,难以保存,原因是_______ (用化学方程式表示)。
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,写出相关离子方程式_______ 。
④ClO2为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(NaClO2)固体与B反应可得到ClO2和NaCl,该反应中,氧化剂与还原剂的物质的量之比为_______ 。

(1)检验F溶液中阳离子的试剂是
(2)Ⅰ转化为J的化学方程式为
(3)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
| A.胶体L具有丁达尔效应 | B.胶体L的分散质粒子直径为 |
| C.胶体L是均一的分散系 | D.胶体L比K的饱和溶液颜色深 |
①目前,很多自来水厂用黄绿色气体来杀菌、消毒。A→B的离子反应方程式为
②C可以杀菌、消毒,但不稳定,难以保存,原因是
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,写出相关离子方程式
④ClO2为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(NaClO2)固体与B反应可得到ClO2和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙、H为还原性气体,丁为一种常见的挥发性酸,G为红褐色沉淀,I的颜色呈浅绿色。
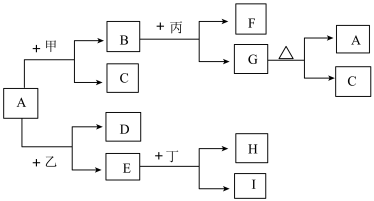
(1)若F是由Na+和SO42-组成的溶液,则甲的化学式是_________ ,若D是能使澄清石灰水变浑浊的气体,则乙的化学式为_________ ;
(2)丁的化学成分可能是_____________ 。
(3)若在I溶液中加入氢氧化钠溶液,可以观察到的现象是_____________ ,对应的化学方程式依次是________________ ;_________________ 。
(4)写出E和C反应的方程式并用单线桥法标明电子的转移方向和数目:_________________ 。
(5)若A中混有杂质Al2O3,除去杂质的方法是先加入过量的__________ ,再_________ 进行分离(填实验操作)

(1)若F是由Na+和SO42-组成的溶液,则甲的化学式是
(2)丁的化学成分可能是
| A.浓硫酸 | B.稀硝酸 | C.盐酸 | D.浓硝酸 |
(3)若在I溶液中加入氢氧化钠溶液,可以观察到的现象是
(4)写出E和C反应的方程式并用单线桥法标明电子的转移方向和数目:
(5)若A中混有杂质Al2O3,除去杂质的方法是先加入过量的
您最近一年使用:0次
【推荐1】环氧乙烷(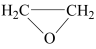 ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
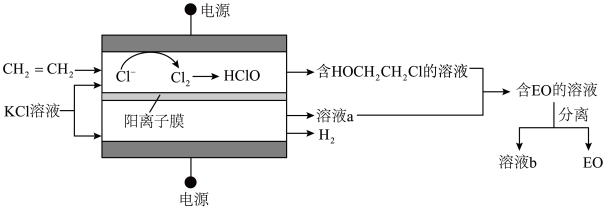
(1)①阳极室产生C12后发生的反应有:C12+H2O HCl+HClO、
HCl+HClO、___________ 。
②溶液a的溶质为___________ 。
③制备过程的总反应方程式为___________ 。
(2)一定条件下,反应物按一定流速通过该装置。电解效率 的定义:
的定义: ×100%
×100%
① (EO)=100%,则溶液b的溶质为
(EO)=100%,则溶液b的溶质为___________ 。
②当乙烯完全消耗时,测得 (EO)≈70%,推测
(EO)≈70%,推测 (EO)≈70%的原因可能为:
(EO)≈70%的原因可能为:
I.阳极有H2O放电
II.阳极室流出液中含有C12和HClO
……
i.检验电解产物,推测I不成立。需要检验的物质是___________ 。
ii.实验证实推测Ⅱ成立,所用试剂是___________ 。
可选试剂:AgNO3溶液、KI溶液、淀粉溶液、品红溶液
 ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
(1)①阳极室产生C12后发生的反应有:C12+H2O
 HCl+HClO、
HCl+HClO、②溶液a的溶质为
③制备过程的总反应方程式为
(2)一定条件下,反应物按一定流速通过该装置。电解效率
 的定义:
的定义: ×100%
×100%①
 (EO)=100%,则溶液b的溶质为
(EO)=100%,则溶液b的溶质为②当乙烯完全消耗时,测得
 (EO)≈70%,推测
(EO)≈70%,推测 (EO)≈70%的原因可能为:
(EO)≈70%的原因可能为:I.阳极有H2O放电
II.阳极室流出液中含有C12和HClO
……
i.检验电解产物,推测I不成立。需要检验的物质是
ii.实验证实推测Ⅱ成立,所用试剂是
可选试剂:AgNO3溶液、KI溶液、淀粉溶液、品红溶液
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】二氧化碳、甲烷等是主要的温室气体。研发二氧化碳和甲烷的利用技术对治理生态环境具有重要意义。
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH1=a kJ•mol-1
CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=b kJ•mol-1
2CO(g)+O2(g)=2CO2(g) ΔH3=c kJ•mol-1
则催化重整反应CO2(g)+CH4(g) 2CO(g)+2H2(g)的ΔH4=
2CO(g)+2H2(g)的ΔH4=_______ 。
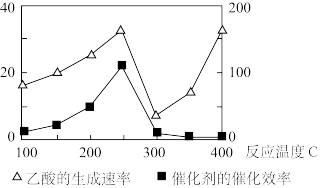
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,还可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因可能是_______ 。
(3)催化重整反应 CO2(g)+CH4(g) 2CO(g)+2H2(g)中,测得CH4的平衡转化率与温度及压强的关系如图所示:
2CO(g)+2H2(g)中,测得CH4的平衡转化率与温度及压强的关系如图所示:
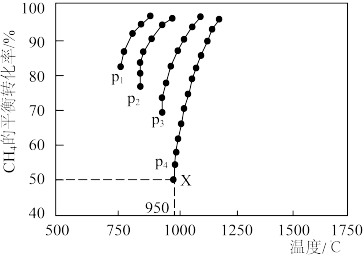
①由图可知,p1、p2、p3、p4由大到小的顺序为_______ 。
②在压强为p4、投料比n(CH4)/n(CO2)为1、950℃的条件下,X点平衡常数Kp=_______
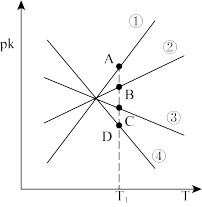
(4)若反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.17kJ•mol-1的正、逆反应速率分别可表示为v正=k正c(CO2)•c(H2)、v逆=k逆c(CO)•c(H2O),则如图所示①②③④四条斜线中,能表示pk正随T变化关系的是斜线
CO(g)+H2O(g) ΔH2=+41.17kJ•mol-1的正、逆反应速率分别可表示为v正=k正c(CO2)•c(H2)、v逆=k逆c(CO)•c(H2O),则如图所示①②③④四条斜线中,能表示pk正随T变化关系的是斜线_______ ,能表示pk逆随T变化关系的是斜线_______ (pk=-lgk)。
(5)一种CO2电还原装置如图所示:
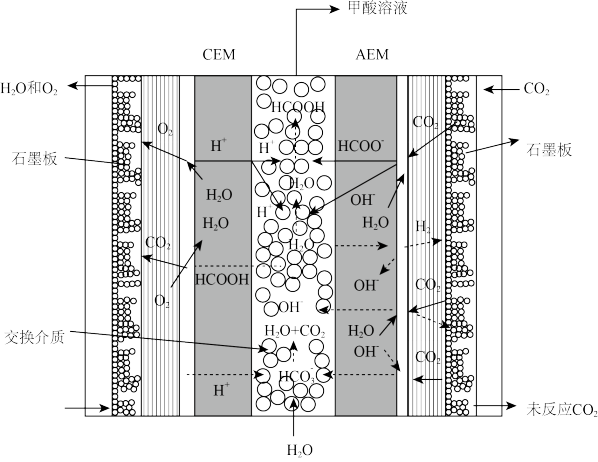
写出阴极的电极反应方程式:_______ 。
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH1=a kJ•mol-1
CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=b kJ•mol-1
2CO(g)+O2(g)=2CO2(g) ΔH3=c kJ•mol-1
则催化重整反应CO2(g)+CH4(g)
 2CO(g)+2H2(g)的ΔH4=
2CO(g)+2H2(g)的ΔH4=(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,还可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因可能是

(3)催化重整反应 CO2(g)+CH4(g)
 2CO(g)+2H2(g)中,测得CH4的平衡转化率与温度及压强的关系如图所示:
2CO(g)+2H2(g)中,测得CH4的平衡转化率与温度及压强的关系如图所示:
①由图可知,p1、p2、p3、p4由大到小的顺序为
②在压强为p4、投料比n(CH4)/n(CO2)为1、950℃的条件下,X点平衡常数Kp=
(4)若反应CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41.17kJ•mol-1的正、逆反应速率分别可表示为v正=k正c(CO2)•c(H2)、v逆=k逆c(CO)•c(H2O),则如图所示①②③④四条斜线中,能表示pk正随T变化关系的是斜线
CO(g)+H2O(g) ΔH2=+41.17kJ•mol-1的正、逆反应速率分别可表示为v正=k正c(CO2)•c(H2)、v逆=k逆c(CO)•c(H2O),则如图所示①②③④四条斜线中,能表示pk正随T变化关系的是斜线
(5)一种CO2电还原装置如图所示:

写出阴极的电极反应方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
(1)已知:①2Cu(s)+ O2(g)=Cu2O(s);△H=﹣169kJ•mol﹣1
O2(g)=Cu2O(s);△H=﹣169kJ•mol﹣1
②C(s)+ O2(g)=CO(g);△H=﹣110.5kJ•mol﹣1
O2(g)=CO(g);△H=﹣110.5kJ•mol﹣1
③Cu(s)+ O2(g)=CuO(s);△H=﹣157kJ•mol﹣1
O2(g)=CuO(s);△H=﹣157kJ•mol﹣1
则方法a发生的热化学方程式是:_____ 。
(2)方法c采用离子交换膜控制电解液中OH﹣的浓度而制备纳米Cu2O,装置如图所示:
该离子交换膜为_____ 离子交换膜(填“阴”或“阳”),该电池的阳极反应式为_____ ,钛极附近的pH值_____ (填“增大”“减小”或“不变”)。
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为_____ 。
(4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验:
2H2O(g) 2H2(g)+O2(g)△H>0.水蒸气的浓度随时间t变化如下表所示:
2H2(g)+O2(g)△H>0.水蒸气的浓度随时间t变化如下表所示:
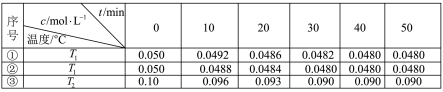
①对比实验的温度:T2_____ T1(填“>”“<”或“=”),能否通过对比实验①③到达平衡所需时间长短判断:_____ (填“能”或“否”)。
②实验①前20min的平均反应速率 v(O2)=_____
③催化剂的催化效率:实验①_____ 实验②(填“>”或“<”)。

| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O |
| 方法c | 电解法,反应为2Cu+H2O Cu2O+H2↑ Cu2O+H2↑ |
| 方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)已知:①2Cu(s)+
 O2(g)=Cu2O(s);△H=﹣169kJ•mol﹣1
O2(g)=Cu2O(s);△H=﹣169kJ•mol﹣1②C(s)+
 O2(g)=CO(g);△H=﹣110.5kJ•mol﹣1
O2(g)=CO(g);△H=﹣110.5kJ•mol﹣1③Cu(s)+
 O2(g)=CuO(s);△H=﹣157kJ•mol﹣1
O2(g)=CuO(s);△H=﹣157kJ•mol﹣1则方法a发生的热化学方程式是:
(2)方法c采用离子交换膜控制电解液中OH﹣的浓度而制备纳米Cu2O,装置如图所示:
该离子交换膜为
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为
(4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验:
2H2O(g)
 2H2(g)+O2(g)△H>0.水蒸气的浓度随时间t变化如下表所示:
2H2(g)+O2(g)△H>0.水蒸气的浓度随时间t变化如下表所示:
①对比实验的温度:T2
②实验①前20min的平均反应速率 v(O2)=
③催化剂的催化效率:实验①

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】青蒿挥发油是青蒿的活性成分(几乎不溶于水,可溶于乙醚,熔点156-157℃,对热不稳定,乙醚的沸点34.6℃),有抗菌、解热、止咳等作用。实验室从青蒿中提取青蒿挥发油的流程如图所示。

索氏提取装置如图所示,实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与青蒿小段接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对青蒿小段的连续萃取。回答下列问题:
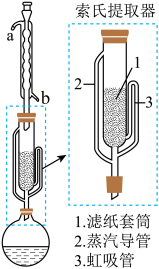
(1)实验时需将青蒿剪成1-2cm小段,放入滤纸套筒1中,剪成小段的目的是___ ,圆底烧瓶中加入乙醚为溶剂时,应不超过烧瓶容积的___ 。
(2)索氏提取器中滤纸套筒的高度(x)、套管内青蒿小段的高度(y)及虹吸管的高度(z)由大到小的顺序是___ (用x、y、z回答),与常规的萃取相比,采用索氏提取器的优点是___ 。
(3)提取时球形冷凝管中冷水应从__ (填“a”或“b”)管导入,提取液需经___ (“常压”或“减压”)蒸馏法除去大部分溶剂,下列仪器在该蒸馏中需要用到的有___ (填字母标号)。
A.直形冷凝管B.球形冷凝管C.锥形瓶D.烧杯E.温度计

索氏提取装置如图所示,实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与青蒿小段接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对青蒿小段的连续萃取。回答下列问题:

(1)实验时需将青蒿剪成1-2cm小段,放入滤纸套筒1中,剪成小段的目的是
(2)索氏提取器中滤纸套筒的高度(x)、套管内青蒿小段的高度(y)及虹吸管的高度(z)由大到小的顺序是
(3)提取时球形冷凝管中冷水应从
A.直形冷凝管B.球形冷凝管C.锥形瓶D.烧杯E.温度计
您最近一年使用:0次
【推荐2】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO)制备草酸镍晶体(NiC2O4·2H2O)的流程如下:
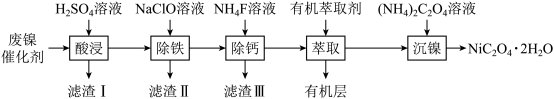
(1)NiC2O4·2H2O中C的化合价是___ 。既能加快“酸浸”反应速率又能提高“酸浸”原料利用率的操作措施为___ 。
(2)“滤渣Ⅰ”的主要成分是___ 。
(3)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是___ 。
(4)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
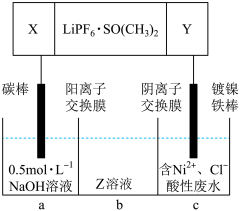
①电极X的反应材料是___ (填化学式);中间隔室b可以得到的主要物质Z是___ (填化学式)。
②电解总反应的离子方程式为___ 。
已知F=96500C/mol,若电池工作tmin,维持电流强度为I A,理论回收Ni___ g(写出计算表达式即可)。

(1)NiC2O4·2H2O中C的化合价是
(2)“滤渣Ⅰ”的主要成分是
(3)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是
(4)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。

①电极X的反应材料是
②电解总反应的离子方程式为
已知F=96500C/mol,若电池工作tmin,维持电流强度为I A,理论回收Ni
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某合金废料主要含铁、铜、铝,为从合金废料中得到Fe2O3、Al2O3和金属Cu等产品,某化学兴趣小组按如图所示工艺流程进行实验(杂质不与稀硫酸反应)。(提示:Al3++4OH-=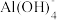 )
)

请回答下列问题:
(1)固体A主要含有的物质是___________ 。
(2)B到C发生反应的离子方程式为_______ ,溶液C中的阳离子主要有__________ 。
(3)若D为NaOH,则溶液E中铝元素的存在形式是___________ (填化学式)。
(4)灼烧沉淀F时所用主要仪器之一是___________(填字母)。
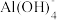 )
)
请回答下列问题:
(1)固体A主要含有的物质是
(2)B到C发生反应的离子方程式为
(3)若D为NaOH,则溶液E中铝元素的存在形式是
(4)灼烧沉淀F时所用主要仪器之一是___________(填字母)。
| A.蒸发皿 | B.烧杯 | C.坩埚 | D.试管 |
您最近一年使用:0次



