回收再利用金属冶炼厂的酸性废水(主要含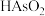 、
、 、
、 、
、 、
、 ),制备亚砷酸铜
),制备亚砷酸铜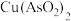 的流程如下。
的流程如下。
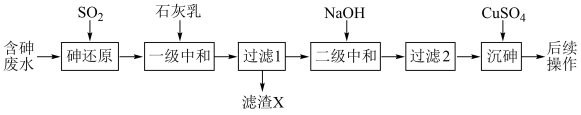
(1)基态砷原子的电子排布式为_______ 。
(2)砷的还原。常温下,五价砷溶液中各种微粒的物质的量分数随pH的变化曲线如图所示。向酸性废水中通入 ,能把五价砷转化为三价砷。
,能把五价砷转化为三价砷。
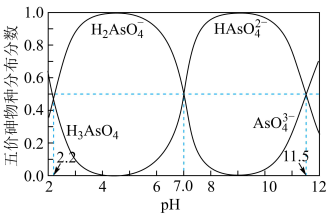
① 的二级电离平衡常数
的二级电离平衡常数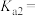
_______ 。
②pH为1时“还原”的主要反应的离子方程式为_______ 。
(3)中和除杂。当溶液中离子浓度小于 ,可认为已经完全除去。
,可认为已经完全除去。
已知: 在
在 时开始转化为
时开始转化为 ,
,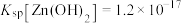 ,
, ,
, 。
。
①一级中和控制pH为2左右,滤渣X的主要成分有_______ 。
②二级中和沉淀重金属离子应控制pH范围为_______ 。
(4)应用碘量法可测定亚砷酸铜中的铜含量。称取2.000g试样溶于稀 搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成
搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成 溶液,取
溶液,取 所配溶液于碘量瓶中加入过量的碘化钾溶液,用
所配溶液于碘量瓶中加入过量的碘化钾溶液,用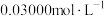
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。
①计算样品中铜元素的质量分数_______ 。(写出计算过程)
②已知纯亚砷酸铜中铜元素的质量分数为23.02%,实际测得样品中铜元素的质量分数有偏差(操作步骤均正确)的原因为_______ 。(已知: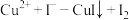 ;
;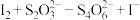 ,未配平)
,未配平)
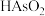 、
、 、
、 、
、 、
、 ),制备亚砷酸铜
),制备亚砷酸铜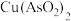 的流程如下。
的流程如下。
(1)基态砷原子的电子排布式为
(2)砷的还原。常温下,五价砷溶液中各种微粒的物质的量分数随pH的变化曲线如图所示。向酸性废水中通入
 ,能把五价砷转化为三价砷。
,能把五价砷转化为三价砷。
①
 的二级电离平衡常数
的二级电离平衡常数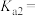
②pH为1时“还原”的主要反应的离子方程式为
(3)中和除杂。当溶液中离子浓度小于
 ,可认为已经完全除去。
,可认为已经完全除去。已知:
 在
在 时开始转化为
时开始转化为 ,
,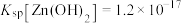 ,
, ,
, 。
。①一级中和控制pH为2左右,滤渣X的主要成分有
②二级中和沉淀重金属离子应控制pH范围为
(4)应用碘量法可测定亚砷酸铜中的铜含量。称取2.000g试样溶于稀
 搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成
搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成 溶液,取
溶液,取 所配溶液于碘量瓶中加入过量的碘化钾溶液,用
所配溶液于碘量瓶中加入过量的碘化钾溶液,用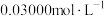
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。①计算样品中铜元素的质量分数
②已知纯亚砷酸铜中铜元素的质量分数为23.02%,实际测得样品中铜元素的质量分数有偏差(操作步骤均正确)的原因为
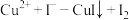 ;
;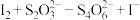 ,未配平)
,未配平)
更新时间:2023-12-07 21:11:32
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
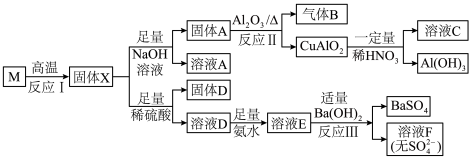
【推荐1】固态化合物M的组成为CuSi2O5,以M为原料实现如下转化:
(1)①固体D的成分为_______ ,溶液E中含氮微粒有_______ 。
②写出反应Ⅱ的化学反应方程式_______ 。
③溶液F加热可得纳米 ,过程中pH会明显下降,原因是
,过程中pH会明显下降,原因是_______ 。
(2)下列说法正确的是_______。
(3)已知 能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验_______ 。
(1)①固体D的成分为
②写出反应Ⅱ的化学反应方程式
③溶液F加热可得纳米
 ,过程中pH会明显下降,原因是
,过程中pH会明显下降,原因是(2)下列说法正确的是_______。
| A.反应Ⅰ不能在陶瓷坩埚中进行 |
| B.固体X可溶于浓氨水 |
| C.溶液A经净化处理后可用于工业粘合剂 |
D.反应Ⅲ中发生的离子反应有: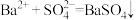 |
(3)已知
 能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
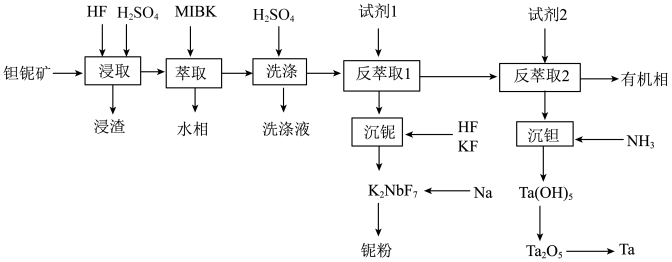
【推荐2】钽(Ta)和铌(Nb)的性质相似,因此常常共生于自然界的矿物中。一种以钽铌伴生矿(主要成分为SiO2、MnO2、Nb2O5、Ta2O5和少量的TiO2、FeO、CaO、MgO)为原料制取钽和铌的流程如下:
已知:①MIBK为甲基异丁基酮;
②KspCaF2=2.510-11,KspMgF2=6.410-9
(1)“浸取”时通常在_____材料的反应器中进行(填标号)。
(2)浸渣的主要成分是_____ ,Ta2O5与氢氟酸反应的离子方程式为_____ 。
(3)“浸取”时,HF的浓度对铌、钽的浸出率的影响如下图所示,则HF的最佳浓度为_____ 。
①流程中钠热还原法制备铌粉的化学方程式为_____ 。
②传统的熔盐电解法采用的电解质体系通常为K2NbF7-NaCl,电解总化学反应方程式为_____ 。
已知:①MIBK为甲基异丁基酮;
②KspCaF2=2.510-11,KspMgF2=6.410-9
(1)“浸取”时通常在_____材料的反应器中进行(填标号)。
| A.陶瓷 | B.玻璃 | C.铅 | D.塑料 |
(2)浸渣的主要成分是
(3)“浸取”时,HF的浓度对铌、钽的浸出率的影响如下图所示,则HF的最佳浓度为

①流程中钠热还原法制备铌粉的化学方程式为
②传统的熔盐电解法采用的电解质体系通常为K2NbF7-NaCl,电解总化学反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】亚硝酰氯( NOCl)是重要的有机合成试剂,可由NO与Cl2在常温下合成。某学习小组在实验室利用如图装置制备亚硝酰氯。

已知:①亚硝酰氯易水解,能与O2反应;
②沸点:NOCl为-5.5℃,Cl2为-34℃,NO为-152℃;
③常温下,2NO + Cl2 =2NOCl2 2NO2 + Cl2 =2NO2Cl。
请回答下列问题:
(1)NOCl中N元素的化合价为_______ ;NOCl水解生成两种酸,其化学方程式为_______ 。
(2)实验所需的NO在A装置中制得,反应的离子方程式为_______ 。
(3)装置B中所盛试剂为_______ 其作用是_______ 。
(4)实验开始时,先关闭K3,打开K2、K4,从a处通一段时间氩气,其目的是_______ 。 然后在a处接废气处理装置,关闭K1、K4,打开K3,再打开分液漏斗的活塞,滴加酸性FeSO4溶液,当观察到D中_______ 时, 关闭K2,打开K1、K4 ,通干燥纯净的Cl2。
(5)为收集产物和分离未反应的两种原料, E、F装置采用不同温度的低温浴槽,其中装置E的温度T区间应控制在_______ ,装置F 的U形管中收集到的是_______ 。

已知:①亚硝酰氯易水解,能与O2反应;
②沸点:NOCl为-5.5℃,Cl2为-34℃,NO为-152℃;
③常温下,2NO + Cl2 =2NOCl2 2NO2 + Cl2 =2NO2Cl。
请回答下列问题:
(1)NOCl中N元素的化合价为
(2)实验所需的NO在A装置中制得,反应的离子方程式为
(3)装置B中所盛试剂为
(4)实验开始时,先关闭K3,打开K2、K4,从a处通一段时间氩气,其目的是
(5)为收集产物和分离未反应的两种原料, E、F装置采用不同温度的低温浴槽,其中装置E的温度T区间应控制在
您最近一年使用:0次
【推荐1】草酸钴(CoOC2O3)用途广泛,一种利用水钴矿[主要成分为Co2O3,还含少量Fe2O3、Al2O3、MgO、MnO、CaO等]制取CoC2O4·2H2O的工艺流程如下:
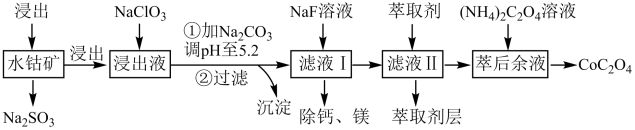
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)浸出过程中加入Na2SO3的作用是将__________ 还原(填离子符号),该步反应的离子方程式为_________ 。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+ ,氯元素被还原为最低价。该反应的离子方程式为_______________ 。
(3)加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是(用离子方程式表示,写出其中一个即可)_____________ 。
(4)萃取剂对金属离子的萃取率与pH的关系如右图所示。使用萃取剂适宜的pH=________(填序号)左右。

(5)滤液I“除钙,镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液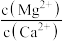 =
=_____ 。

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的作用是将
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+ ,氯元素被还原为最低价。该反应的离子方程式为
(3)加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是(用离子方程式表示,写出其中一个即可)
(4)萃取剂对金属离子的萃取率与pH的关系如右图所示。使用萃取剂适宜的pH=________(填序号)左右。

| A.2.0 | B.3.0 | C.4.0 |
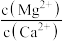 =
=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】食醋(主要成分 )、纯碱(
)、纯碱( )和小苏打(
)和小苏打( )均为家庭厨房中常用的物质。已知:
)均为家庭厨房中常用的物质。已知:
回答下列问题:
(1)25℃时, 溶液的
溶液的 ,则溶液中由水电离出的
,则溶液中由水电离出的
_________  。
。
(2)常温下,将20mL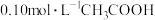 溶液和20mL
溶液和20mL 溶液分别与20mL
溶液分别与20mL 溶液混合(假设混合后溶液体积为两溶液体积之和)。
溶液混合(假设混合后溶液体积为两溶液体积之和)。
①反应开始时,反应速率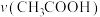
_________  (填“>”、“<”或“=”,下同)。
(填“>”、“<”或“=”,下同)。
②充分反应后,两溶液中
_________ 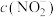 。
。
(3)25℃时,向 溶液中加入一定量的
溶液中加入一定量的 ,所得混合液的
,所得混合液的 ,则混合液中
,则混合液中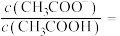
_________ 。
(4)常温下,下列方法可使 的电离程度增大的是
的电离程度增大的是_________ (填字母)。
a.加入少量稀盐酸 b.加热溶液 c.加水稀释 d.加入少量冰醋酸
(5)生活中可用醋酸除水垢,但工业锅炉的水垢中常含有硫酸钙,需先用 溶液处理,最后再用
溶液处理,最后再用 溶液除去。已知:25℃时,
溶液除去。已知:25℃时, 、
、 ,结合化学平衡原理解释加入
,结合化学平衡原理解释加入 溶液的原因
溶液的原因_________ 。
 )、纯碱(
)、纯碱( )和小苏打(
)和小苏打( )均为家庭厨房中常用的物质。已知:
)均为家庭厨房中常用的物质。已知:| 弱酸 |  |  |  |
| 电离常数 |  |   |  |
回答下列问题:
(1)25℃时,
 溶液的
溶液的 ,则溶液中由水电离出的
,则溶液中由水电离出的
 。
。(2)常温下,将20mL
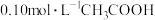 溶液和20mL
溶液和20mL 溶液分别与20mL
溶液分别与20mL 溶液混合(假设混合后溶液体积为两溶液体积之和)。
溶液混合(假设混合后溶液体积为两溶液体积之和)。①反应开始时,反应速率
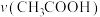
 (填“>”、“<”或“=”,下同)。
(填“>”、“<”或“=”,下同)。②充分反应后,两溶液中

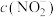 。
。(3)25℃时,向
 溶液中加入一定量的
溶液中加入一定量的 ,所得混合液的
,所得混合液的 ,则混合液中
,则混合液中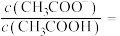
(4)常温下,下列方法可使
 的电离程度增大的是
的电离程度增大的是a.加入少量稀盐酸 b.加热溶液 c.加水稀释 d.加入少量冰醋酸
(5)生活中可用醋酸除水垢,但工业锅炉的水垢中常含有硫酸钙,需先用
 溶液处理,最后再用
溶液处理,最后再用 溶液除去。已知:25℃时,
溶液除去。已知:25℃时, 、
、 ,结合化学平衡原理解释加入
,结合化学平衡原理解释加入 溶液的原因
溶液的原因
您最近一年使用:0次
【推荐3】二氧化铈(CeO2)是一种重要的稀土化合物。以氟碳铈矿( 主要含CeCO3F)为原料制备CeO2的一种工艺流程如下:

已知:i.Ce4+能与F-结合成[ CeFx](4-x)+,也能与 结合成[CeSO4]2+;
结合成[CeSO4]2+;
ⅱ.在硫酸体系中Ce4+能被萃取剂[(HA)2 ]萃取,而Ce3+不能。
ⅲ.常温下,Ce2(CO3)3饱和溶液浓度为1.0×10-6mol/L。请回答下列问题:
(1)铈的原子序数是58,它在元素周期表的位置是_________________________ 。
(2)“氧化焙烧”过程中可以加快反应速率和提高原料利用率的方法是____________________ 、_________________ (写出2种即可)。
(3)“氧化焙烧”产物CeO2与稀H2SO4 反应的离子方程式为________________ 。浸出的过程中常加入适量的Na2SO4浓溶液,其作用是_____________________________ 。
(4)“萃取”时存在反应:Ce4++n(HA)2 Ce(H2n-4A2n)+4H+。萃取后水层中还存在的含铈元素的微粒主要是
Ce(H2n-4A2n)+4H+。萃取后水层中还存在的含铈元素的微粒主要是__________ ,经处理后可循环使用。
(5)“反萃取”中加H2O2的主要反应离子方程式为_______________________ 。在“反萃取”后所得水层中加入1.0mol/L的NH4HCO3溶液,产生Ce2(CO3)3沉淀,当Ce3+沉淀完全时[c(Ce3+)=1×10-5mol/L],溶液中c( )约为
)约为______________ 。
(6)CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生着CeO2 CeO2(1-x)+xO2 ↑(0≤x≤0.25)的循环。请写出CeO2消除CO尾气的化学方程式
CeO2(1-x)+xO2 ↑(0≤x≤0.25)的循环。请写出CeO2消除CO尾气的化学方程式_____________________________ 。

已知:i.Ce4+能与F-结合成[ CeFx](4-x)+,也能与
 结合成[CeSO4]2+;
结合成[CeSO4]2+;ⅱ.在硫酸体系中Ce4+能被萃取剂[(HA)2 ]萃取,而Ce3+不能。
ⅲ.常温下,Ce2(CO3)3饱和溶液浓度为1.0×10-6mol/L。请回答下列问题:
(1)铈的原子序数是58,它在元素周期表的位置是
(2)“氧化焙烧”过程中可以加快反应速率和提高原料利用率的方法是
(3)“氧化焙烧”产物CeO2与稀H2SO4 反应的离子方程式为
(4)“萃取”时存在反应:Ce4++n(HA)2
 Ce(H2n-4A2n)+4H+。萃取后水层中还存在的含铈元素的微粒主要是
Ce(H2n-4A2n)+4H+。萃取后水层中还存在的含铈元素的微粒主要是(5)“反萃取”中加H2O2的主要反应离子方程式为
 )约为
)约为(6)CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生着CeO2
 CeO2(1-x)+xO2 ↑(0≤x≤0.25)的循环。请写出CeO2消除CO尾气的化学方程式
CeO2(1-x)+xO2 ↑(0≤x≤0.25)的循环。请写出CeO2消除CO尾气的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知X、Y、Z、W、Q、R、E七种元素中,原子序数X<Y<Z<W<Q<R<E,其结构或性质信息如下表。
请根据信息回答有关问题:
(1)元素X的原子核外共有_______ 种不同运动状态的电子,有_______ 种不同能级的电子。
(2)Q的基态原子电子排布式为_______ ,R的元素符号为_______ ,E元素基态原子的价电子排布式为_______ 。
(3)含有元素W的盐的焰色试验为_______ 色,许多金属元素形成的盐都可以发生焰色试验,其原因是_______ 。
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数 |
| Y | 元素原子最外层电子排布式为nsnnpn+1 |
| Z | 单质在常温、常压下是气体,原子的M层上有1个未成对的p电子 |
| W | 元素的正一价离子的电子层结构与氩相同 |
| Q | 元素的核电荷数为Y和Z之和 |
| R | 元素的正三价离子的3d能级为半充满 |
| E | 元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
(1)元素X的原子核外共有
(2)Q的基态原子电子排布式为
(3)含有元素W的盐的焰色试验为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】Cu4O(PO4)2是锂-磷酸氧铜电池正极的活性物质,它可通过下列反应制备:2Na3PO4+CuSO4+2NH3·H2O= Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu的电子排布式:_____ 。
(2)PO43-的空间构型是______ 。
(3)P、S、N元素第一电离能由大到小顺序为_____ 。
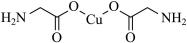
(4)氨基乙酸铜分子结构如下图,其中碳原子的杂化方式为____ ,基态碳原子核外电子有__ 种运动状态。
(5)晶胞原子坐标参数,表示晶胞内部各原子的相对位置,图1为铜与氧形成的某化合物晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0),则D原子的坐标参数为
,0),则D原子的坐标参数为______ 。
(6)图2为铜晶体中铜原子的堆积图,则晶体铜原子的堆积方式为_____ 。

(1)写出基态Cu的电子排布式:
(2)PO43-的空间构型是
(3)P、S、N元素第一电离能由大到小顺序为
(4)氨基乙酸铜分子结构如下图,其中碳原子的杂化方式为

(5)晶胞原子坐标参数,表示晶胞内部各原子的相对位置,图1为铜与氧形成的某化合物晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0),则D原子的坐标参数为
,0),则D原子的坐标参数为(6)图2为铜晶体中铜原子的堆积图,则晶体铜原子的堆积方式为

您最近一年使用:0次
【推荐3】亚铁氰化钾(K4[Fe(CN)6])是重要的化工原料和食品添加剂,又称黄血盐。黄血盐溶液与稀硫酸加热时发生反应:K4[Fe(CN)6+6H2SO4+6H2O 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑。回答下列问题:
2K2SO4+FeSO4+3(NH4)2SO4+6CO↑。回答下列问题:
(1)写出基态Fe2+的核外电子排布式______ 。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有______ 和______ 。:1mol K4[Fe(CN)6]中含有σ键的数目为_____ NA。
(3)(NH4)2SO4中N原子的杂化方式为______ ;N和O相比,第一电离能更大的是______ ,电负性更大的是______ 。
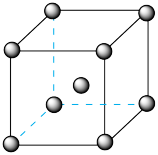
(4)铁、钾、钠均采用体心立方堆积,结构如图。晶胞中金属原子的配位数为______ ,钠、钾相比,熔点更高的是______ ,原因是______ 。已知铁的原子半径为r cm,阿伏加 德罗常数为NA,铁的相对原子质量为a,则铁的密度为______ g·cm-3。
 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑。回答下列问题:
2K2SO4+FeSO4+3(NH4)2SO4+6CO↑。回答下列问题:(1)写出基态Fe2+的核外电子排布式
(2)K4[Fe(CN)6]中的作用力除共价键外,还有
(3)(NH4)2SO4中N原子的杂化方式为
(4)铁、钾、钠均采用体心立方堆积,结构如图。晶胞中金属原子的配位数为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】三硫代碳酸钠(Na2CS3)在农业上用作杀菌剂和杀线虫剂,在工业上用于处理废水中的重金属离子。某化学兴趣小组对Na2CS3进行了某些性质实验和定量测定。
实验一:探究Na2CS3的性质
(1)取少量Na2CS3样品于试管中,加水溶解,滴加酸性KMnO4溶液,溶液紫色褪去。
①使用的酸性KMnO4溶液,可以选用____ 酸化(选填字母)。
A.硫酸 B.硝酸 C.盐酸
②已知该反应的氧化产物是 ,该反应的氧化剂与还原剂的物质的量之比为
,该反应的氧化剂与还原剂的物质的量之比为____ 。
实验二:测定Na2CS3溶液的浓度
按如图所示装置进行实验:将50.0mLNa2CS3
溶液置于三颈烧瓶中,打开仪器d的活塞,滴入足量2.0mol·L−1的稀硫酸,关闭活塞。

已知: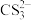 +2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
+2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
(2)仪器d的名称是_______ 。
(3)B中发生反应的化学方程式为_______ 。
(4)反应开始时需要先通入一段时间N2,目的是排除装置中的空气,防止A中生成的H2S被氧化。反应结束后,打开活塞K,再缓慢通入一段时间热N2(高于60℃),其目的是_______ 。
(5)为了计算该Na2CS3溶液的浓度,可测定B中生成沉淀的质量。对B中混合物进行过滤、洗涤、干燥、称重。若B中生成沉淀的质量为7.2g,则该Na2CS3溶液的物质的量浓度是_______ mol/L。
(6)也可以通过测定C中溶液质量的增加值来计算Na2CS3溶液的浓度,装置e中的试剂为_______ ;若缺少装置f,计算值会_____ (填“无影响”“偏高”或“偏低”)。
实验一:探究Na2CS3的性质
(1)取少量Na2CS3样品于试管中,加水溶解,滴加酸性KMnO4溶液,溶液紫色褪去。
①使用的酸性KMnO4溶液,可以选用
A.硫酸 B.硝酸 C.盐酸
②已知该反应的氧化产物是
 ,该反应的氧化剂与还原剂的物质的量之比为
,该反应的氧化剂与还原剂的物质的量之比为实验二:测定Na2CS3溶液的浓度
按如图所示装置进行实验:将50.0mLNa2CS3
溶液置于三颈烧瓶中,打开仪器d的活塞,滴入足量2.0mol·L−1的稀硫酸,关闭活塞。

已知:
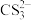 +2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
+2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)(2)仪器d的名称是
(3)B中发生反应的化学方程式为
(4)反应开始时需要先通入一段时间N2,目的是排除装置中的空气,防止A中生成的H2S被氧化。反应结束后,打开活塞K,再缓慢通入一段时间热N2(高于60℃),其目的是
(5)为了计算该Na2CS3溶液的浓度,可测定B中生成沉淀的质量。对B中混合物进行过滤、洗涤、干燥、称重。若B中生成沉淀的质量为7.2g,则该Na2CS3溶液的物质的量浓度是
(6)也可以通过测定C中溶液质量的增加值来计算Na2CS3溶液的浓度,装置e中的试剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】纳米TiO2在化纤、橡胶、化妆品等领域有着极其广泛的应用。
Ⅰ.制备:制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2。
(1)TiCI4水解生成TiO2·xH2O的化学方程式为___________ 。
Ⅱ.测定纯度:用氧化还原滴定法测定TiO2的质量分数:称量2.0 gTiO2样品溶解并还原为Ti3+,配制成100ml待测溶液。从中取出25ml待测溶液,再以KSCN溶液作指示剂,用0.2000 mol·L-1NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
(2)配制含Ti3+溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、胶头滴管、量筒外,还需要的仪器名称___________ 。
(3)滴定Ti3+时发生反应的离子方程式为___________ 。
(4)达到滴定终点时的现象是___________ 。
(5)某学生根据3次实验分别记录有关数据如下表:
计算TiO2样品的质量分数是___________ 。
(6)若在配制标准溶液过程中,下列操作使TiO2质量分数测定结果偏高的是___________。
Ⅰ.制备:制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2。
(1)TiCI4水解生成TiO2·xH2O的化学方程式为
Ⅱ.测定纯度:用氧化还原滴定法测定TiO2的质量分数:称量2.0 gTiO2样品溶解并还原为Ti3+,配制成100ml待测溶液。从中取出25ml待测溶液,再以KSCN溶液作指示剂,用0.2000 mol·L-1NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
(2)配制含Ti3+溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、胶头滴管、量筒外,还需要的仪器名称
(3)滴定Ti3+时发生反应的离子方程式为
(4)达到滴定终点时的现象是
(5)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测溶液的体积/mL | 0.2000 mol·L-1NH4Fe(SO4)2标准溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 29.80 | 29.80 |
| 第二次 | 25.00 | 1.50 | 29.30 | 27.80 |
| 第三次 | 25.00 | 2.00 | 32.20 | 30.20 |
(6)若在配制标准溶液过程中,下列操作使TiO2质量分数测定结果偏高的是___________。
| A.滴至终点,俯视读数 |
| B.待测液移入锥形瓶后,加入10 mL蒸馏水 |
| C.盛装标准液滴定管尖嘴有气泡时便开始滴定,滴定后无气泡 |
| D.盛装标准液滴定管用蒸馏水润洗后,未用标准液润洗 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】钴被誉为战略物资,有出色的性能和广泛的应用。一种利用水钴矿(主要成分为Co2O3,含少量Fe2O3、MnO等)制取钴产品的工艺流程如下:

已知:①浸出液含有的金属阳离子主要有Fe2+、Co2+、Mn2+等
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
回答下列问题:
(1)写出浸出过程中Co2O3发生反应的离子方程式为______ 。
(2)“加Na2CO3调pH至3.7”,过滤所得到的沉淀成分为____ 。
(3)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的主要目的是__ ;萃取剂使用的最佳pH范围是____ (填代号)。
A 1.0~1.5 B 2.0~2.5 C 3.0~3.5 D 4.0~5.0

(4)向“萃取后余液”中加入沉钴剂生成CoCO3,同时产生一种使澄清石灰水变浑浊的气体,其相应的离子方程式为_______ 。
(5)在空气中焙烧CoCO3生成相应的金属氧化物和CO2,测得充分煅烧后固体质量为4.82g,CO2的体积为1.344 L(标准状况),则金属氧化物的化学式为_________ 。

已知:①浸出液含有的金属阳离子主要有Fe2+、Co2+、Mn2+等
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式为
(2)“加Na2CO3调pH至3.7”,过滤所得到的沉淀成分为
(3)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的主要目的是
A 1.0~1.5 B 2.0~2.5 C 3.0~3.5 D 4.0~5.0

(4)向“萃取后余液”中加入沉钴剂生成CoCO3,同时产生一种使澄清石灰水变浑浊的气体,其相应的离子方程式为
(5)在空气中焙烧CoCO3生成相应的金属氧化物和CO2,测得充分煅烧后固体质量为4.82g,CO2的体积为1.344 L(标准状况),则金属氧化物的化学式为
您最近一年使用:0次



