某温度下,向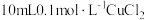 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
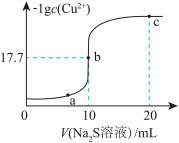
溶液,滴加过程中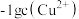 与
与 溶液体积的关系如图所示。下列有关说法正确的是
溶液体积的关系如图所示。下列有关说法正确的是
已知: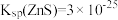 (溶液混合后体积的变化忽略不计)
(溶液混合后体积的变化忽略不计)
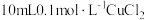 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中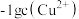 与
与 溶液体积的关系如图所示。下列有关说法正确的是
溶液体积的关系如图所示。下列有关说法正确的是已知:
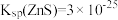 (溶液混合后体积的变化忽略不计)
(溶液混合后体积的变化忽略不计)
A. 溶液中: 溶液中: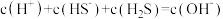 |
| B.a、b、c三点对应的溶液中,水的电离程度最大的为b点 |
C.向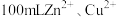 物质的量浓度均为 物质的量浓度均为 的混合溶液中逐滴加入 的混合溶液中逐滴加入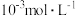 的 的 溶液, 溶液, 先沉淀 先沉淀 |
D.c点溶液中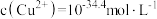 |
更新时间:2023-12-05 15:19:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,下列有关电解质溶液的说法正确的是
A.由水电离出的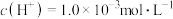 ,则该溶液可能是稀盐酸 ,则该溶液可能是稀盐酸 |
B.将 的 的 溶液稀释10倍,则溶液中 溶液稀释10倍,则溶液中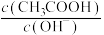 减小 减小 |
C.向稀硫酸中加入氨水至中性,则溶液中 |
D.浓度为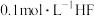 溶液不断加水稀释, 溶液不断加水稀释, 始终增大 始终增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,用0.100mol/L的NaOH溶液滴定20.00ml、0.100mol/L的HNO2溶液,lg 与所加NaOH溶液体积的关系如图所示,下列说法错误的是
与所加NaOH溶液体积的关系如图所示,下列说法错误的是

 与所加NaOH溶液体积的关系如图所示,下列说法错误的是
与所加NaOH溶液体积的关系如图所示,下列说法错误的是
| A.25℃时,用0.100mol/L的HNO2溶液的pH值为2.75 |
| B.B点对应的溶液中,2c(H+)+c(HNO2)=c(NO2-)+2c(OH-) |
| C.C点对应溶液的PH=7,加入NaOH溶液的体积为20.00ml |
| D.滴定过程中从A到D点溶液中水的电离程度先增大后减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列溶液中有关物质的量浓度关系正确的是
| A.Na2S 溶液中 c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| B.Na2CO3溶液中:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| C.室温下,pH=1的CH3COOH溶液和pH=13的NaOH溶液等体积混合,溶液中离子浓度的大小顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.0.1mol•L-1的NaHC2O4溶液的pH=4,则c(HC2O4-)>c(H+)>c(H2C2O4)>c(C2O42-) |
您最近一年使用:0次
【推荐1】某工厂以菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料生产硫酸锰晶体的工艺流程如下图所示:

常温下几种金属氢氧化物沉淀时的pH:
下列说法错误的是

常温下几种金属氢氧化物沉淀时的pH:
 |  |  | |
| 开始沉淀时的pH | 7.2 | 2.7 | 4.7 |
| 完全沉淀时的pH | 10.0 | 3.7 | 6.7 |
A.试剂a只能是 溶液 溶液 |
B.调pH时,为不引入新的杂质,试剂b可以选择 |
C.pH调整的范围为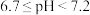 |
| D.过滤所得的晶体最后用乙醇洗涤 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,Ksp(CaSO4)= 9×10-4,常温下CaSO4在水中的沉淀溶解平衡曲线如图所示。下列判断中正确的是
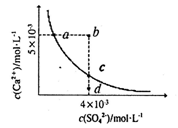

| A.a点对应的溶液中c(H+)·c(OH-) 的数值为1×10-14 |
| B.a 点对应的Ksp不等于c点对应的Ksp |
| C.b 点将有沉淀生成,平衡后溶液中c(SO42-)= 3×10-3mol/L,而向d 点溶液中加入适量的CaSO4固体可以变到c 点 |
| D.CaSO4的饱和溶液中c(SO42-) > c(Ca2+) >c(H+) >c(OH-) |
您最近一年使用:0次
【推荐3】T℃时,三种盐的沉淀溶解平衡曲线如图所示,已知 pM 为阳离子浓度的负对数,pR 为阴离子浓度的负对数,下列说法正确的是


A.Y 点:c(Ca2+)>c(SO ),Z点:c(CO ),Z点:c(CO )>c(Mn2+) )>c(Mn2+) |
| B.溶度积:Ksp(MnCO3)>Ksp(CaCO3)>Ksp(CaSO4) |
| C.X点对应的CaCO3溶液为不饱和溶液,可以继续溶解CaCO3 |
D.T℃时,CaSO4(s)+CO (aq) (aq) CaCO3(s)+SO CaCO3(s)+SO (aq)的平衡常数 K 的数量级为 103 (aq)的平衡常数 K 的数量级为 103 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】旧铅蓄电池会导致铅污染,RSR求工艺回收铅的流程如图所示。

已知:a.铅膏的主要成分是 和
和 ,
, 是强酸;
是强酸;
b.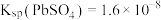 ,
,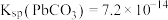 。
。
下列有关说法正确的是

已知:a.铅膏的主要成分是
 和
和 ,
, 是强酸;
是强酸;b.
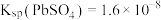 ,
,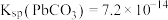 。
。下列有关说法正确的是
A.副产品M主要成分为硫酸铵,其水溶液中离子浓度最大的为 |
B.反应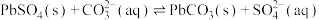 的 的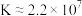 |
C.气体N为 ,步骤④的反应原理是利用强酸制取弱酸 ,步骤④的反应原理是利用强酸制取弱酸 |
| D.步骤⑤中Pb在阳极析出 |
您最近一年使用:0次
【推荐2】已知: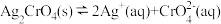
 ,T℃时,向Na2CrO4溶液中不断加入AgNO3固体,得到曲线如下图所示。下列说法正确的是
,T℃时,向Na2CrO4溶液中不断加入AgNO3固体,得到曲线如下图所示。下列说法正确的是

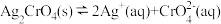
 ,T℃时,向Na2CrO4溶液中不断加入AgNO3固体,得到曲线如下图所示。下列说法正确的是
,T℃时,向Na2CrO4溶液中不断加入AgNO3固体,得到曲线如下图所示。下列说法正确的是
| A.降低a点悬浊液的温度,则a点可沿虚线移动到b点 |
| B.向a点的悬浊液加入少量硝酸银固体,则a点可沿虚线移动到c点 |
C.d点溶液中离子浓度大小顺序为:c( )>c(Na+)>c(Ag+)>c( )>c(Na+)>c(Ag+)>c( ) ) |
D.在d点的悬浊液中,c( )=1×10-9 mol/L )=1×10-9 mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】牙形石(一种微型古生物遗体)主要成分为Ca3(PO4)2,存在于灰岩(主要成分为CaCO3)中。可以通过合适的酸除去灰岩以显示出牙形石的形态,进而分析当时的地层环境。根据以下信息,分析错误 的是
已知:(1)Ksp[Ca3(PO4)2]=2.07×10-33
(2)钙的磷酸盐中只有磷酸二氢钙可溶于水,其余难溶于水
(3)酸的电离平衡常数
已知:(1)Ksp[Ca3(PO4)2]=2.07×10-33
(2)钙的磷酸盐中只有磷酸二氢钙可溶于水,其余难溶于水
(3)酸的电离平衡常数
| 弱酸 | H3PO4 | CH3COOH | H2CO3 |
| 电离平衡常数(25℃) | Ka1=6.9×10-3 Ka2=6.2×10-8 Ka3=4.8×10-13 | Ka=1.8×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 |
A.当加入过量的盐酸时与牙形石反应为:Ca3(PO4)2+4H+=2H2PO +3Ca2+ +3Ca2+ |
| B.过量的醋酸可以溶解灰岩:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
C.过量醋酸与牙形石反应:Ca3(PO4)2+4CH3COOH=3Ca2++4CH3COO-+2H2PO |
| D.醋酸可用于除去灰岩显示出牙形石 |
您最近一年使用:0次



