在某一恒温体积可变的密闭容器中发生反应: △H<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
△H<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
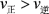
 △H<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
△H<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是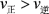
| A.t2时刻改变的条件是向密闭容器中加Z |
B.0~t2时, |
C.I、II两过程达到平衡时,X的体积分数 |
D.I、II两过程达到平衡时,平衡常数 |
更新时间:2023-11-13 15:16:51
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法中正确的是
| A.电解精炼铜时,将粗铜与电源的负极相连 |
| B.当反应物的总能量高于生成物的总能量时,该反应为吸热反应 |
C.FeCl3(aq)+3KSCN(aq) 3KCl(aq)+Fe(SCN)3(aq)体系中加入KCl固体,平衡向逆反应方向移动 3KCl(aq)+Fe(SCN)3(aq)体系中加入KCl固体,平衡向逆反应方向移动 |
| D.1807年,化学家戴维电解熔融氯化钾得到钾,直到现在,工业上依然用电解法制备金属钠、镁、铝等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知NO2与N2O4可相互转化:2NO2(g) N2O4(g)
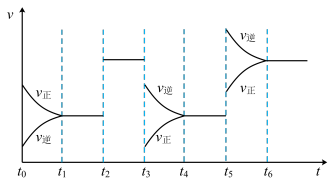
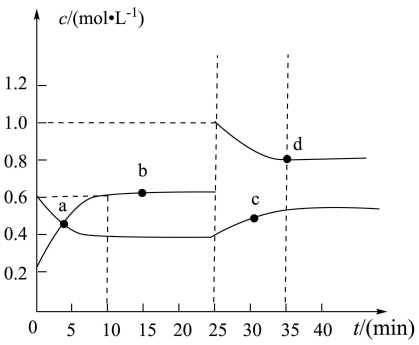
N2O4(g)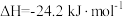 ,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析合理的是
,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析合理的是
 N2O4(g)
N2O4(g)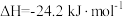 ,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析合理的是
,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析合理的是
| A.25min时,正反应速率减小 |
| B.反应进行到10min时,体系吸收的热量为9.68kJ |
C.a、b、c、d四点中 正与 正与 逆均相等 逆均相等 |
D.10min时, 的生成速率为 的生成速率为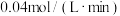 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】选择不同的反应探究化学反应速率的影响因素,所用试剂不合理 的是
a.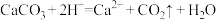 (观察气泡产生的快慢)
(观察气泡产生的快慢)
b.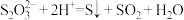 (观察浑浊产生的快慢)
(观察浑浊产生的快慢)
a.
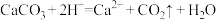 (观察气泡产生的快慢)
(观察气泡产生的快慢)b.
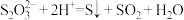 (观察浑浊产生的快慢)
(观察浑浊产生的快慢)| 反应 | 影响因素 | 所用试剂 | |
| A | a | 接触面积 | 块状CaCO3、0.5 mol/L HCl 粉末状CaCO3、0.5 mol/L HCl |
| B | a | H+浓度 | 块状CaCO3、0.5 mol/L HCl 块状CaCO3、3.0 mol/LHCl |
| C | b | H+浓度 | 0.1 mol/L Na2S2O3、稀H2SO4 0.1mol/L Na2S2O3、浓H2SO4 |
| D | b | 温度 | 0.1 mol/L Na2S2O3、0.1 Na2S2O3 H2SO4、冷水 0.1 mol/L Na2S2O3、0.1 Na2S2O3 H2SO4、热水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】如图所示向A中充入1 mol X 、1 mol Y,向B中充入2 mol X、2 mol Y,起始时,
V(A) = V(B) = a L。在相同温度和有催化剂存在下,两容器中各自发生下述反应:X(g)+Y(g) 2Z(g)+W(g) ΔH<0。达到平衡时,V(A) = 1.1a L。(连通管中气体体积不计)下列说法正确的是( )
2Z(g)+W(g) ΔH<0。达到平衡时,V(A) = 1.1a L。(连通管中气体体积不计)下列说法正确的是( )
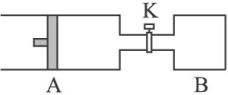
V(A) = V(B) = a L。在相同温度和有催化剂存在下,两容器中各自发生下述反应:X(g)+Y(g)
 2Z(g)+W(g) ΔH<0。达到平衡时,V(A) = 1.1a L。(连通管中气体体积不计)下列说法正确的是( )
2Z(g)+W(g) ΔH<0。达到平衡时,V(A) = 1.1a L。(连通管中气体体积不计)下列说法正确的是( )
| A.n(Z)B = 2n(Z)A |
| B.A容器中X的转化率为20% |
| C.若向A和B中均再加入1molX和1molY,X的体积分数均增大 |
| D.打开K保持温度不变,又达到平衡时,A的体积为3.3a L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得达到平衡时的有关数据如下[已知X(g)+3Y(g) 2Z(g) ΔH=−Q kJ·mol−1]:
2Z(g) ΔH=−Q kJ·mol−1]:
下列说法正确的是
 2Z(g) ΔH=−Q kJ·mol−1]:
2Z(g) ΔH=−Q kJ·mol−1]:| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1 mol X、3 mol Y | 2 mol Z | 4 mol Z |
| Z的浓度(mol·L−1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A.2c1>c3 | B.a+b=Q | C.2p2<p3 | D.α1+α3>1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知反应CO(g)+2H2(g) CH3OH(g) ΔH=Q kJ·mol-1,在三个不同容积的容器中分别充入1 mol CO与2 mol H2,恒温恒容,测得平衡时CO的转化率如表。下列说法正确的是( )
CH3OH(g) ΔH=Q kJ·mol-1,在三个不同容积的容器中分别充入1 mol CO与2 mol H2,恒温恒容,测得平衡时CO的转化率如表。下列说法正确的是( )
 CH3OH(g) ΔH=Q kJ·mol-1,在三个不同容积的容器中分别充入1 mol CO与2 mol H2,恒温恒容,测得平衡时CO的转化率如表。下列说法正确的是( )
CH3OH(g) ΔH=Q kJ·mol-1,在三个不同容积的容器中分别充入1 mol CO与2 mol H2,恒温恒容,测得平衡时CO的转化率如表。下列说法正确的是( )| 温度(℃) | 容器体积 | CO转化率 | 平衡压强(p) | |
| ① | 200 | V1 | 50% | p1 |
| ② | 200 | V2 | 70% | p2 |
| ③ | 350 | V3 | 50% | p3 |
| A.反应速率:③>①>② |
| B.平衡时体系压强:p1∶p2=5∶4 |
| C.若容器体积V1>V3,则Q<0 |
| D.若从实验②中的容器,抽走0.15 mol CO和0.30 mol H2,则CO转化率>70% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】哈伯法合成氨的反应原理为 ,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
 ,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是A.该反应在低温下能自发进行,则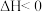 |
B.选用高效催化剂,可降低该反应的 |
C.其它条件不变,增大起始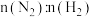 的比值,可提高N2的平衡转化率 的比值,可提高N2的平衡转化率 |
| D.提高体系的压强可增大反应的化学平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 稀溶液中存在如下平衡:
稀溶液中存在如下平衡:
Ⅰ.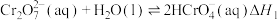
Ⅱ.
关于该溶液的说法不正确 的是(温度变化忽略不计)
 稀溶液中存在如下平衡:
稀溶液中存在如下平衡:Ⅰ.
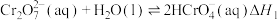
Ⅱ.

关于该溶液的说法
| A.加水稀释,溶液中离子总数增加 |
B.加入少量浓 溶液,Ⅰ和Ⅱ均向正反应方向移动 溶液,Ⅰ和Ⅱ均向正反应方向移动 |
C.加入少量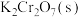 ,溶液颜色不再变化时, ,溶液颜色不再变化时,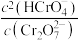 比原溶液中的小 比原溶液中的小 |
D.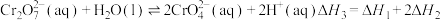 |
您最近一年使用:0次
【推荐3】温度为T1时,在容积为10 L的恒容密闭容器充入一定量的M (g)和N (g),发生反应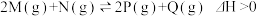 。反应过程中的部分数据如表所示,下列说法正确的是
。反应过程中的部分数据如表所示,下列说法正确的是
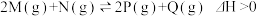 。反应过程中的部分数据如表所示,下列说法正确的是
。反应过程中的部分数据如表所示,下列说法正确的是| t/min | 0 | 5 | 10 |
| n(M)/ mol | 6.0 | 2.0 | |
| n(N)/ mol | 3.0 | 1.0 |
| A.T2时该反应的化学平衡常数为0.64,则T1>T2 |
| B.0-5 min内,用M表示的平均反应速率为0.4 mol∙L-1∙min-1 |
| C.该反应在第8 min时v逆>v正 |
| D.当M、N的转化率之比保持不变时,可判断该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
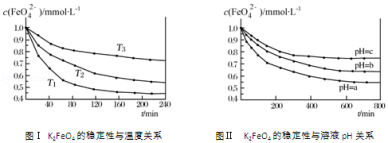
【推荐1】K2FeO4在水中不稳定,发生反应:4FeO42-+10H2O 4Fe(OH)3(胶体)+8OH-+3O2,其稳定性与温度(T)和溶液pH的关系分别如图所示。下列说法不正确的是
4Fe(OH)3(胶体)+8OH-+3O2,其稳定性与温度(T)和溶液pH的关系分别如图所示。下列说法不正确的是
 4Fe(OH)3(胶体)+8OH-+3O2,其稳定性与温度(T)和溶液pH的关系分别如图所示。下列说法不正确的是
4Fe(OH)3(胶体)+8OH-+3O2,其稳定性与温度(T)和溶液pH的关系分别如图所示。下列说法不正确的是
| A.由图Ⅰ可知K2FeO4的稳定性随温度的升高而减弱 |
| B.由图Ⅱ可知图中a>c |
| C.由图Ⅰ可知温度:T1>T2>T3 |
| D.由图Ⅰ可知上述反应△H>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的浓度、反应速率分别随时间的变化如图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的浓度、反应速率分别随时间的变化如图所示:
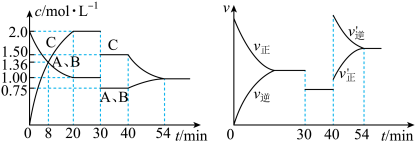
下列说法中不正确的是
 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的浓度、反应速率分别随时间的变化如图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的浓度、反应速率分别随时间的变化如图所示:
下列说法中不正确的是
| A.30~40 min 内该反应使用了催化剂 |
| B.化学方程式中的x=1,正反应为放热反应 |
| C.30 min时减小压强,40 min时升高温度 |
| D.8 min前A的平均反应速率为0.08 mol·L-1·min-1 |
您最近一年使用:0次