BTCu是荧光增强型Cu2+荧光分子探针,可对环境和生物体内的微量Cu2+进行有效检测。BTCu识别Cu2+机理如下图:

回答下列问题:
(1)基态Cu原子的价电子排布式为___________ 。
(2)BTCu中所含第二周期元素的第一电离能由小到大的顺序为___________ (用元素符号表示)。
(3)探针BTCu与Cu2+的识别过程既有氧化脱氢反应,也有配合形式的参与。1molBTCu-Cu+中,Cu+形成的配位键有___________ mol,B原子的杂化轨道类型是___________ 。
(4)某晶体的晶胞结构如下图所示。已知:a=b=0.524 nm,c-1.032 nm,晶胞棱边夹角均为90°,NA为阿伏加德罗常数的值。(1nm=1×10-7cm)

①距离Fe最近且等距的S有___________ 个。
②该晶体的化学式是___________ 。
③该晶体的密度是___________ g/cm3 (列出计算式)。

回答下列问题:
(1)基态Cu原子的价电子排布式为
(2)BTCu中所含第二周期元素的第一电离能由小到大的顺序为
(3)探针BTCu与Cu2+的识别过程既有氧化脱氢反应,也有配合形式的参与。1molBTCu-Cu+中,Cu+形成的配位键有
(4)某晶体的晶胞结构如下图所示。已知:a=b=0.524 nm,c-1.032 nm,晶胞棱边夹角均为90°,NA为阿伏加德罗常数的值。(1nm=1×10-7cm)

①距离Fe最近且等距的S有
②该晶体的化学式是
③该晶体的密度是
更新时间:2024-01-03 16:29:24
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]________ 。
(2)根据元素周期律,元素的电负性Ga________ (填“大于”或“小于”,下同)As,第一电离能B________ Ga;BF3和NH3的分子能够通过配位键相结合的原因是_______________________ 。
(3)杀虫剂Na3AsO4中阴离子的空间构型为________ ,As原子采取________ 杂化。
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体,从F-和Cl-结构的不同分析其原因是_____________ 。
(5)原子晶体GaAs的晶胞参数a=x pm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为________ ;A原子距离B原子所在六面体的侧面的最短距离为________ (用x表示)pm;该晶体的密度为________ g·cm-3(阿伏伽德罗常数的值用NA表示)
 。
。
(1)基态Ga原子的核外电子排布式为[Ar]
(2)根据元素周期律,元素的电负性Ga
(3)杀虫剂Na3AsO4中阴离子的空间构型为
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体,从F-和Cl-结构的不同分析其原因是
(5)原子晶体GaAs的晶胞参数a=x pm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
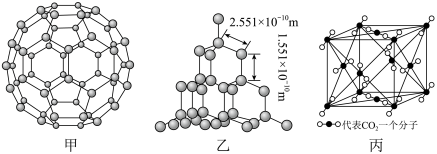
【推荐2】下面是C60、金刚石和二氧化碳的分子模型。
请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:_________________
(2)从晶体类型来看,C60属于_________ 晶体。
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目是__________________________ ;晶体硅中硅原子与共价键的个数比为____________
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有________ 个二氧化碳分子,二氧化碳分子中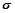 键与
键与 键的个数比为
键的个数比为________________ 。
(5)有机化合物中碳原子的成键方式有多种,这也是有机化合物种类繁多的原因之一。丙烷分子中2号碳原子的杂化方式是_______ ,丙烯分子中2号碳原子的杂化方式是_______ ,丙烯分子中最多有______ 个原子共平面。

请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:
(2)从晶体类型来看,C60属于
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目是
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有
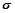 键与
键与 键的个数比为
键的个数比为(5)有机化合物中碳原子的成键方式有多种,这也是有机化合物种类繁多的原因之一。丙烷分子中2号碳原子的杂化方式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】氧化钪( )在合金、电光源、催化剂和陶瓷等领域有广泛应用,以钪锰矿石(含
)在合金、电光源、催化剂和陶瓷等领域有广泛应用,以钪锰矿石(含 、
、 、
、 、
、 、CaO、FeO)为原料制备氧化钪的一种工艺流程如图所示。
、CaO、FeO)为原料制备氧化钪的一种工艺流程如图所示。
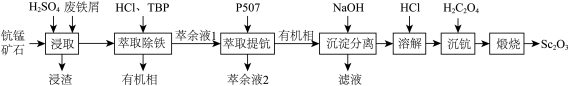
已知:①TBP和P507均为有机萃取剂:②常温下,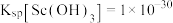 ;③草酸可与多种金属离子形成可溶性络合物。回答下列问题:
;③草酸可与多种金属离子形成可溶性络合物。回答下列问题:
(1)钪锰矿石中含铁元素,则基态Fe的价电子排布式为___________ 。
(2)“浸取”时铁屑被 氧化为
氧化为 ,该反应的离子方程是
,该反应的离子方程是___________ 。
(3)常温下,“沉淀分离”时加入NaOH溶液调节pH至6,滤液中 的浓度为
的浓度为___________ 。
(4)已知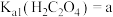 ,
,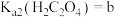 ,
,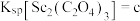 。“沉钪”时,发生反应
。“沉钪”时,发生反应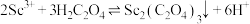 ,此反应的平衡常数K=
,此反应的平衡常数K=___________ (用含a、b、c的代数式表示)。反应过程中,草酸用量过多时,钪的沉淀率下降,原因可能是___________ 。
(5)草酸钪晶体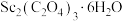 :在空气中加热,
:在空气中加热, 随温度的变化情况如图所示。250℃时,晶体的主要成分是
随温度的变化情况如图所示。250℃时,晶体的主要成分是___________ (填化学式)。550~850℃发生反应的化学方程式为___________ 。

 )在合金、电光源、催化剂和陶瓷等领域有广泛应用,以钪锰矿石(含
)在合金、电光源、催化剂和陶瓷等领域有广泛应用,以钪锰矿石(含 、
、 、
、 、
、 、CaO、FeO)为原料制备氧化钪的一种工艺流程如图所示。
、CaO、FeO)为原料制备氧化钪的一种工艺流程如图所示。
已知:①TBP和P507均为有机萃取剂:②常温下,
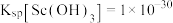 ;③草酸可与多种金属离子形成可溶性络合物。回答下列问题:
;③草酸可与多种金属离子形成可溶性络合物。回答下列问题:(1)钪锰矿石中含铁元素,则基态Fe的价电子排布式为
(2)“浸取”时铁屑被
 氧化为
氧化为 ,该反应的离子方程是
,该反应的离子方程是(3)常温下,“沉淀分离”时加入NaOH溶液调节pH至6,滤液中
 的浓度为
的浓度为(4)已知
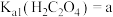 ,
,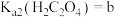 ,
,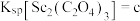 。“沉钪”时,发生反应
。“沉钪”时,发生反应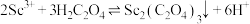 ,此反应的平衡常数K=
,此反应的平衡常数K=(5)草酸钪晶体
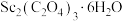 :在空气中加热,
:在空气中加热, 随温度的变化情况如图所示。250℃时,晶体的主要成分是
随温度的变化情况如图所示。250℃时,晶体的主要成分是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】新型铜锌锡疏化合物( )薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:
)薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:
(1) 的价电子排布式为
的价电子排布式为_______ , 位于元素周期表的
位于元素周期表的_______ 区。
(2)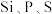 第一电离能由大到小的顺序是
第一电离能由大到小的顺序是_______ 。
(3) 和
和 键角较小的是
键角较小的是_______ ,原因是_______ 。
(4)向 溶液中滴加氨水至过量,最终得到蓝色溶液,溶液中
溶液中滴加氨水至过量,最终得到蓝色溶液,溶液中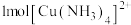 含有
含有_______ 个σ键。再向溶液中如入乙醇,得到深蓝色晶体,该晶体中不存在_______ (填标号)。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
(5)具有6个配体的 的配合物
的配合物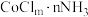 ,若
,若 此配合物与足量的
此配合物与足量的 溶液反应只生成
溶液反应只生成 沉淀,该配合物的化学式为
沉淀,该配合物的化学式为_______ (需区分内界和外界)
(6)氨缩脲( )分子中σ键与π键的数目之比为
)分子中σ键与π键的数目之比为_______ 。氨缩脲与胆矾溶液反应得到如图所示的紫色物质,1mol紫色物质中含配位键的数目为_______ 。

 )薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:
)薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:(1)
 的价电子排布式为
的价电子排布式为 位于元素周期表的
位于元素周期表的(2)
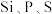 第一电离能由大到小的顺序是
第一电离能由大到小的顺序是(3)
 和
和 键角较小的是
键角较小的是(4)向
 溶液中滴加氨水至过量,最终得到蓝色溶液,溶液中
溶液中滴加氨水至过量,最终得到蓝色溶液,溶液中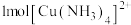 含有
含有A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
(5)具有6个配体的
 的配合物
的配合物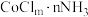 ,若
,若 此配合物与足量的
此配合物与足量的 溶液反应只生成
溶液反应只生成 沉淀,该配合物的化学式为
沉淀,该配合物的化学式为(6)氨缩脲(
 )分子中σ键与π键的数目之比为
)分子中σ键与π键的数目之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(1)31Ga基态原子的核外电子排布式是___________ 。C、N、O三种元素第一电离能从大到小的顺序是____________ 。写出一种与 OH- 互为等电子体的分子为_________________ (填化学式)。
(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是_________ ;N2H4分子中氮原子轨道的杂化类型是_______ 。
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在__________ (填标号)
a. 离子键 b. 共价键 c. 配位键 d. 范德华力
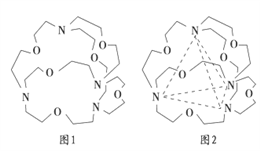
③图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是________ (填标号)。
a. CF4 b. NH4+ c.CH4 d. H2O
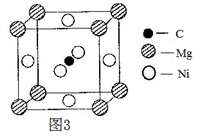
(3)最近发现,只含C、Mg和Ni三种元素的某种晶体具有超导性。该晶体的一个晶胞如图3所示,则该晶体的化学式为___________ 。
(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在
a. 离子键 b. 共价键 c. 配位键 d. 范德华力
③图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是
a. CF4 b. NH4+ c.CH4 d. H2O

(3)最近发现,只含C、Mg和Ni三种元素的某种晶体具有超导性。该晶体的一个晶胞如图3所示,则该晶体的化学式为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某班同学用如下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)基态Fe原子的价层电子排布式为___________ ;铁元素在元素周期表中的位置是___________ ,属于___________ 区。
(2)甲组同学探究 与I-的反应。取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L
与I-的反应。取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L  溶液混合。分别取2mL此溶液于4支试管中进行如下实验:
溶液混合。分别取2mL此溶液于4支试管中进行如下实验:
①第一支试管中加入3滴硝酸酸化的 溶液,生成黄色沉淀;
溶液,生成黄色沉淀;
②第二支试管中加入1mL 充分振荡、静置,
充分振荡、静置, 层呈紫色;
层呈紫色;
③第三支试管中加入3滴某黄色溶液,生成蓝色沉淀;
④第四支试管中加入3滴KSCN溶液,溶液变红。
实验③加入的试剂为___________ (填化学式);实验___________ (填序号)的现象可以证明该氧化还原反应为可逆反应。
(3)乙组同学设计如下实验探究亚铁盐的性质。
①实验I中由白色沉淀生成红褐色沉淀的化学方程式为___________ 。
②对实验Ⅱ所得白色沉淀展开研究:
ⅰ.取Ⅱ中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;
ⅱ.向ⅰ所得溶液中滴入KSCN试剂,溶液几乎不变红;
ⅲ.向ⅱ溶液中再滴入少量氯水,溶液立即变为红色。
根据以上现象,实验中生成的白色沉淀的化学式为___________ 。溶液立即变为红色对应的离子方程式为___________ 。
(4)丙组同学向乙组同学得到的红色溶液中滴入EDTA试剂,溶液红色立即褪去。通过查阅资料,发现可能是EDTA的配合能力比 更强,加入EDTA后,EDTA与三价铁形成了更稳定的配合物,红色消失。该配合物阴离子的结构如图所示,图中M代表
更强,加入EDTA后,EDTA与三价铁形成了更稳定的配合物,红色消失。该配合物阴离子的结构如图所示,图中M代表 。配合物中C、N、O元素的第一电离能由大到小的顺序为
。配合物中C、N、O元素的第一电离能由大到小的顺序为___________ , 的配位数为
的配位数为___________ 。

 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)基态Fe原子的价层电子排布式为
(2)甲组同学探究
 与I-的反应。取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L
与I-的反应。取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L  溶液混合。分别取2mL此溶液于4支试管中进行如下实验:
溶液混合。分别取2mL此溶液于4支试管中进行如下实验:①第一支试管中加入3滴硝酸酸化的
 溶液,生成黄色沉淀;
溶液,生成黄色沉淀;②第二支试管中加入1mL
 充分振荡、静置,
充分振荡、静置, 层呈紫色;
层呈紫色;③第三支试管中加入3滴某黄色溶液,生成蓝色沉淀;
④第四支试管中加入3滴KSCN溶液,溶液变红。
实验③加入的试剂为
(3)乙组同学设计如下实验探究亚铁盐的性质。
| 实验方案 | 现象 | 查阅资料 | |
| Ⅰ | 1.0 mL 0.1 mol/L 溶液中滴加1.0 mL 0.5 mol/L NaOH溶液 溶液中滴加1.0 mL 0.5 mol/L NaOH溶液 | 生成白色沉淀,后沉淀基本变为红褐色 | 在溶液中不存在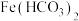 |
| Ⅱ | 1.0 mL 0.1 mol/L  溶液中滴加1.0 mL 0.5 mol/L 溶液中滴加1.0 mL 0.5 mol/L  溶液 溶液 | 生成白色沉淀,后沉淀颜色几乎不变 |
②对实验Ⅱ所得白色沉淀展开研究:
ⅰ.取Ⅱ中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;
ⅱ.向ⅰ所得溶液中滴入KSCN试剂,溶液几乎不变红;
ⅲ.向ⅱ溶液中再滴入少量氯水,溶液立即变为红色。
根据以上现象,实验中生成的白色沉淀的化学式为
(4)丙组同学向乙组同学得到的红色溶液中滴入EDTA试剂,溶液红色立即褪去。通过查阅资料,发现可能是EDTA的配合能力比
 更强,加入EDTA后,EDTA与三价铁形成了更稳定的配合物,红色消失。该配合物阴离子的结构如图所示,图中M代表
更强,加入EDTA后,EDTA与三价铁形成了更稳定的配合物,红色消失。该配合物阴离子的结构如图所示,图中M代表 。配合物中C、N、O元素的第一电离能由大到小的顺序为
。配合物中C、N、O元素的第一电离能由大到小的顺序为 的配位数为
的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】本题包括A、B两小题,请选定其中一题,并在相应的答题区域内作答。若多做,则按A题评分。
A.《物质结构与性质》非血红素铁是食物中的铁存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物。
(1)Fe2+基态核外电子排布式为______________ 。
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为________ (填化学式)。
(3)蛋白质分子中氨基氮原子的轨道杂化类型是___ ;1mol 乙酸分子中含有σ的键的数目为_____ 。
(4)把氯气通入黄血盐(K4[Fe(CN)6])溶液中,得到赤血盐(K3[Fe(CN)6]),写 出该变化的化学方程式_______________________ 。
(5)FeO晶胞结构如图所示,FeO晶体中Fe2+配位数为____ 。

A.《物质结构与性质》非血红素铁是食物中的铁存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物。
(1)Fe2+基态核外电子排布式为
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为
(3)蛋白质分子中氨基氮原子的轨道杂化类型是
(4)把氯气通入黄血盐(K4[Fe(CN)6])溶液中,得到赤血盐(K3[Fe(CN)6]),写 出该变化的化学方程式
(5)FeO晶胞结构如图所示,FeO晶体中Fe2+配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】继去年12月西安交大研发了新型石墨烯量子点白光发光材料,并成功应用到白光WLED器件中,2019年8月,中国科学院福建物质结构研究所合成了首例缺陷诱导的晶态无机硼酸盐单一组分白光材料Ba2[Sn(OH)6][B(OH)4]2,并获得了该化合物的LED器件。
(1)石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。

①在石墨烯晶体中,每个C原子连接__ 个六元环,每个六元环占有___ 个C原子。
②图乙中1号C与相邻C形成的键角__ (填“>”、“<”或“=”)图甲中1号C与相邻C形成的键角,理由是__ 。
(2)已知氮化硼与砷化镓属于同种晶体类型。砷化镓以第三代半导体著称,熔点为1230℃,具有空间网状结构,两种晶体熔点较高的是__ (填化学式),其理由是__ 。
(3)8-羟基喹啉铝是OLED中的重要发光材料及电子传输材料,其微观结构如图所示,8-羟基喹啉铝中存在的化学键为___ 。
A.离子键 B.极性键 C.非极性键 D.配位键 E.π键 F.金属键

(4)已知BaF2晶体是面心立方结构,晶胞结构如图所示。晶胞中代表F原子的是__ (填“黑”或“白”)球。已知BaF2晶胞参数为apm,设阿伏加 德罗常数的值为NA,则BaF2的密度是__ g•cm-3(列出计算表达式)。

(1)石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。

①在石墨烯晶体中,每个C原子连接
②图乙中1号C与相邻C形成的键角
(2)已知氮化硼与砷化镓属于同种晶体类型。砷化镓以第三代半导体著称,熔点为1230℃,具有空间网状结构,两种晶体熔点较高的是
(3)8-羟基喹啉铝是OLED中的重要发光材料及电子传输材料,其微观结构如图所示,8-羟基喹啉铝中存在的化学键为
A.离子键 B.极性键 C.非极性键 D.配位键 E.π键 F.金属键

(4)已知BaF2晶体是面心立方结构,晶胞结构如图所示。晶胞中代表F原子的是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铜的化合物具有广泛的用途。
(1)Cu2+基态核外电子排布式为__________________ 。
(2)往硫酸铜溶液中加入过量氨水,溶液最终变成深蓝色,继续加入乙醇,可析出[Cu(NH3)4]SO4·H2O,N、O、S原子的第一电离能由大到小的顺序为__________________ ,与SO42-互为等电子体的分子的化学式为__ ,每个乙醇分子中sp3杂化的原子个数为_________________ 。
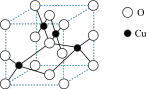
(3)铜的一种氧化物晶体结构如图所示,其中O原子的配位数为_________________ 。
(4) Cu2O的熔点比Cu2S高的原因是__________________ 。
(1)Cu2+基态核外电子排布式为
(2)往硫酸铜溶液中加入过量氨水,溶液最终变成深蓝色,继续加入乙醇,可析出[Cu(NH3)4]SO4·H2O,N、O、S原子的第一电离能由大到小的顺序为
(3)铜的一种氧化物晶体结构如图所示,其中O原子的配位数为

(4) Cu2O的熔点比Cu2S高的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】镧系为元素周期表中第ⅢB族、原子序数为57至71的元素。
(1)镝(Dy)的基态原子电子排布式为[Xe]4f106s2,画出镝(Dy)原子外围电子排布图:_____ 。
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+的电子排布式为_______________ 。
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是_______ (填元素名称)。
几种镧系元素的电离能(单位:kJ·mol-1)
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为_______________ (用元素符号表示)。
②元素Al也有类似成键情况,气态氯化铝分子表示为(AlCl3)2,分子中Al 原子杂化方式为________ ,分子中所含化学键类型有______________ (填字母)。
a.离子键 b.极性键 C.非极性键 d.配位键
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点,则PrO2(二氧化镨)的晶胞中有______ 个氧原子;已知晶胞参数为a pm,密度为ρg·cm-3,NA=________ (用含a、ρ的代数式表示)。
(1)镝(Dy)的基态原子电子排布式为[Xe]4f106s2,画出镝(Dy)原子外围电子排布图:
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+的电子排布式为
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是
几种镧系元素的电离能(单位:kJ·mol-1)
| 元素 | I1 | I2 | I3 | I4 |
| Yb(镱) | 604 | 1217 | 4494 | 5014 |
| Lu(镥) | 532 | 1390 | 4111 | 4987 |
| La(镧) | 538 | 1067 | 1850 | 5419 |
| Ce(铈) | 527 | 1047 | 1949 | 3547 |
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为
②元素Al也有类似成键情况,气态氯化铝分子表示为(AlCl3)2,分子中Al 原子杂化方式为
a.离子键 b.极性键 C.非极性键 d.配位键
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点,则PrO2(二氧化镨)的晶胞中有
您最近一年使用:0次
【推荐2】2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
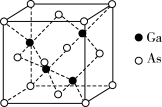
(1)基态Ga原子价电子排布式__________________ ,核外电子占据最高能级的电子云形状为_________ ;基态As原子最高能层上有_______ 个电子。
(2)镓失去电子的逐级电离能(单位:kJ•mol−1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为____ 和+3,砷的第一电离能比镓_____ (填“大”或“小”)。
(3)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为__________ 。
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中Ga原子的杂化方式为______ ,AsH3分子的空间构型为____________ 。
(5)相同压强下,AsH3的沸点______ NH3(填“大于”或“小于”),原因为__________________
(6)GaAs为原子晶体,其晶胞结构如图所示,Ga与As以___________ (填“共价键”或“离子键”)键合。设阿伏加 德罗常数的值为NA,该晶胞边长为a pm,则GaAs晶体的密度为_____ g•cm−3(列出计算式即可)。

(1)基态Ga原子价电子排布式
(2)镓失去电子的逐级电离能(单位:kJ•mol−1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为
(3)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中Ga原子的杂化方式为
(5)相同压强下,AsH3的沸点
(6)GaAs为原子晶体,其晶胞结构如图所示,Ga与As以
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】卤族元素的单质和化合物很多,利用所学物质结构与性质的知识去认识和理解它们。
(1)溴的核外电子排布式为__ 。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在。使氢氟酸分子缔合作用力是___ 。
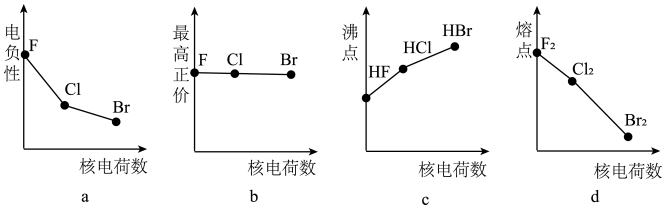
(3)下列曲线表示卤族元素某种性质随核电荷数递增的变化趋势,正确的是___ 。
(4)已知高碘酸有两种形式,化学式分别为H5IO6(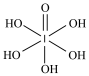 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6___ HIO4(填“>”、“<”或“=”)。IO 的VSEPR模型为
的VSEPR模型为__ 。
(5)铜与氯形成化合物的晶胞如附图所示(黑点代表铜粒子)。
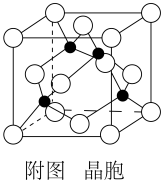
①该晶体的化学式为__ 。
②一定条件下,Cu2O比CuO更稳定的原因是__ 。
③已知该晶体的密度为ρg·cm-3,阿伏加 德罗常数为NA,则该晶体的边长为__ pm。(用含ρ、NA的式子表示)
(1)溴的核外电子排布式为
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在。使氢氟酸分子缔合作用力是
(3)下列曲线表示卤族元素某种性质随核电荷数递增的变化趋势,正确的是

(4)已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6 的VSEPR模型为
的VSEPR模型为(5)铜与氯形成化合物的晶胞如附图所示(黑点代表铜粒子)。

①该晶体的化学式为
②一定条件下,Cu2O比CuO更稳定的原因是
③已知该晶体的密度为ρg·cm-3,阿伏加 德罗常数为NA,则该晶体的边长为
您最近一年使用:0次



