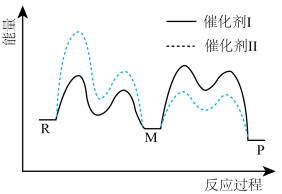
催化剂I和II均能催化反应 。反应历程(下图)中,M为中间产物。其它条件相同时,下列说法正确的是
。反应历程(下图)中,M为中间产物。其它条件相同时,下列说法正确的是
 。反应历程(下图)中,M为中间产物。其它条件相同时,下列说法正确的是
。反应历程(下图)中,M为中间产物。其它条件相同时,下列说法正确的是
| A.使用催化剂I和II,催化历程相同 |
| B.反应达平衡时,升高温度,P的浓度增大 |
| C.使用催化剂II时,反应体系更快达到平衡 |
| D.使用催化剂I时,反应过程中M所能达到的最高浓度更大 |
更新时间:2024-01-11 14:05:12
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】工业上常利用CO2和NH3合成尿素[CO(NH2)2],该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是
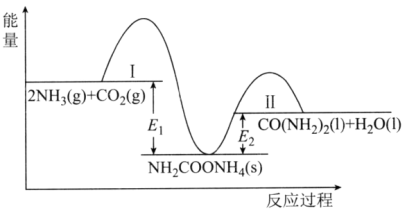

| A.NH2COONH4为合成尿素反应的中间产物 |
| B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能 |
| C.逆反应过程Ⅱ快于过程Ⅰ |
D.2NH3(g)+CO2(g) CO(NH2)2(1)+H2O(1)的焓变△H=El-E2 CO(NH2)2(1)+H2O(1)的焓变△H=El-E2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】一定条件下,石墨转化为金刚石要吸收能量。在该条件下,下列结论正确的是
| A.金刚石比石墨稳定 |
| B.等质量的金刚石和石墨完全燃烧释放的热量相同 |
| C.1mol C(金刚石)比1mol C(石墨)的总键能大 |
| D.1mol C(金刚石)比1mol C(石墨)的总能量高 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】两个均充有H2S的刚性密闭容器,起始压强均为pkPa,以温度、Al2O3催化剂为条件变量,进行实验:2H2S(g) 2H2(g)+S2(g),反应相同时间,结果如图所示。下列说法错误的是
2H2(g)+S2(g),反应相同时间,结果如图所示。下列说法错误的是

 2H2(g)+S2(g),反应相同时间,结果如图所示。下列说法错误的是
2H2(g)+S2(g),反应相同时间,结果如图所示。下列说法错误的是
| A.温度升高,H2S分解的正,逆反应速率均增大 |
B.900℃,ts后达平衡,H2的平均生成速率为 pkPa∙s−1 pkPa∙s−1 |
| C.Al2O3催化剂使得正反应的活化能小于逆反应的活化能 |
| D.1100℃,曲线II、III重合,说明Al2O3催化剂失去活性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为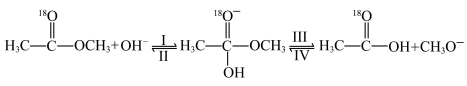 能量变化如图所示。已知
能量变化如图所示。已知 为快速平衡,下列说法错误的是
为快速平衡,下列说法错误的是

 能量变化如图所示。已知
能量变化如图所示。已知 为快速平衡,下列说法错误的是
为快速平衡,下列说法错误的是
| A.反应I为加成反应,且是反应的决速步骤 |
B.反应结束后,溶液中存在 |
| C.反应结束后,溶液中存在CH318OH |
D. 和 和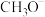 的总能量与 的总能量与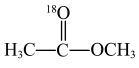 和 和 的总能量之差等于图示总反应的焓变 的总能量之差等于图示总反应的焓变 |
您最近一年使用:0次
【推荐1】我国科研人员利用单原子铜修饰的氮化碳,可实现更有效、更有选择性地将CO2通过光催化还原为燃料(如图)的目的。下列说法错误的是
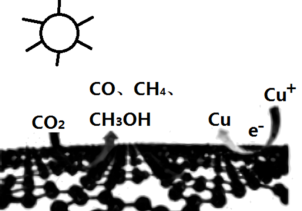

| A.光合过程中光能转化为化学能 | B.氮化碳的化学式为C3N4 |
| C.光合过程中铜不参与反应 | D.1molCO2转化为1molCH4转移8mol电子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】三元WO3/C3N4/Ni(OH)x光催化剂产氢机理如图。下列说法不正确的是
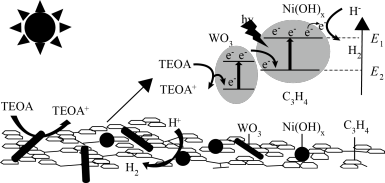

| A.TEOA→TEOA+为还原反应 | B.Ni(OH)x降低了H+→H2的活化能 |
| C.能量转化形式为太阳能→化学能 | D.WO3参与了制氢反应过程 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列实验装置能达到实验目的的是( )
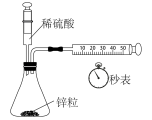 | 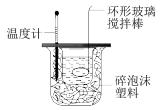 | 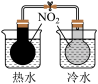 | 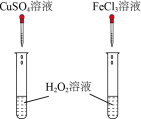 |
| A.测定一定时间内生成 H2的反应速率 | B.可以进行中和热的测定实验 | C.比较温度对化学反应速率的影响 | D.比较Cu2+、Fe3+对 H2O2分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl- [CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如图:以下结论和解释正确的是
[CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如图:以下结论和解释正确的是

 [CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如图:以下结论和解释正确的是
[CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如图:以下结论和解释正确的是
| A.由实验①可推知正反应的ΔH<0 |
| B.实验②中c(H2O)增大平衡逆向移动 |
| C.由实验③可知配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
| D.原蓝色溶液中加入少量NaCl固体,实验现象与实验③相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl-⇌[CoCl4]2-+6H2OΔH,用该溶液做实验,溶液的颜色变化如图:

以下结论和解释错误的是

以下结论和解释错误的是
| A.由实验①可推知ΔH>0 |
| B.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中σ键数之比为9∶2 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
您最近一年使用:0次

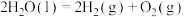
 相关的说法,正确的是
相关的说法,正确的是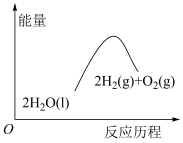

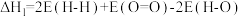 (E表示键能)
(E表示键能) 的燃烧热
的燃烧热




 CH3COOOH+H2O,下列有关说法正确的是
CH3COOOH+H2O,下列有关说法正确的是

