二甲醚(DME)作为一种新兴的基本有机化工原料,在制药、燃料、农药等化学工业中有许多用途,还是未来制取低碳烯烃的主要原料之一、回答下列问题。
(1)已知: 的燃烧热
的燃烧热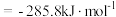 ,CO(g)的燃烧热
,CO(g)的燃烧热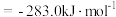 ,二甲醚
,二甲醚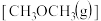 的燃烧热
的燃烧热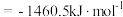 ,H2O(g)=H2O(l) △H=-44.0kJmol-1。则
,H2O(g)=H2O(l) △H=-44.0kJmol-1。则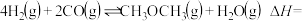
___________  。
。
(2)恒温恒容条件下,能说明 达到平衡的标志是___________(填序号)。
达到平衡的标志是___________(填序号)。
(3)在T℃时,向容积为1L的恒容容器中充入物质的量之和为3mol的 和CO且
和CO且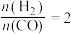 ,发生反应
,发生反应 ,达到平衡时
,达到平衡时 的体积分数对应图甲中a点。
的体积分数对应图甲中a点。
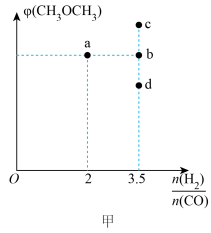
当起始 =3.5时,反应达到平衡状态后,CH3OCH3的体积分数可能对应图甲中的
=3.5时,反应达到平衡状态后,CH3OCH3的体积分数可能对应图甲中的___________ (填“b”“c”或“d”)点。
(4)某温度下,将2.0molCO(g)和4.0molH2(g)充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图乙所示,关于温度和压强的关系判断正确的是___________(填序号)。

(5)在恒温恒压(p)条件下,密闭容器中充入2.0molCO(g)和4.0molH2(g)发生应4H2(g)+2CO(g)⇌CH3OCH3(g)+H2O(g),平衡时H2的转化率为50%。达到平衡时,p(H2)=_________ ;平衡常数Kp=_________ (以分压表示,分压=总压×物质的量分数)。
(1)已知:
 的燃烧热
的燃烧热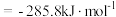 ,CO(g)的燃烧热
,CO(g)的燃烧热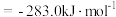 ,二甲醚
,二甲醚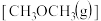 的燃烧热
的燃烧热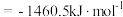 ,H2O(g)=H2O(l) △H=-44.0kJmol-1。则
,H2O(g)=H2O(l) △H=-44.0kJmol-1。则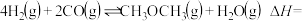
 。
。(2)恒温恒容条件下,能说明
 达到平衡的标志是___________(填序号)。
达到平衡的标志是___________(填序号)。| A.H2、CO、CH3OCH3、H2O的反应速率之比为4:2:1:1 |
| B.H2、CO、CH3OCH3、H2O的物质的量之比为4:2:1:1 |
| C.混合气体的平均摩尔质量保持不变 |
| D.容器中气体的密度保持不变 |
(3)在T℃时,向容积为1L的恒容容器中充入物质的量之和为3mol的
 和CO且
和CO且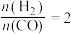 ,发生反应
,发生反应 ,达到平衡时
,达到平衡时 的体积分数对应图甲中a点。
的体积分数对应图甲中a点。
当起始
 =3.5时,反应达到平衡状态后,CH3OCH3的体积分数可能对应图甲中的
=3.5时,反应达到平衡状态后,CH3OCH3的体积分数可能对应图甲中的(4)某温度下,将2.0molCO(g)和4.0molH2(g)充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图乙所示,关于温度和压强的关系判断正确的是___________(填序号)。

A.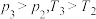 | B.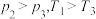 |
C.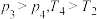 | D. |
(5)在恒温恒压(p)条件下,密闭容器中充入2.0molCO(g)和4.0molH2(g)发生应4H2(g)+2CO(g)⇌CH3OCH3(g)+H2O(g),平衡时H2的转化率为50%。达到平衡时,p(H2)=
更新时间:2024-01-10 15:20:36
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】Ⅰ.据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+205.9 kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9 kJ·mol-1 ①
CO(g)+H2O(g) CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 ②
二氧化碳重整:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③
则反应①自发进行的条件是______________ ,ΔH3=______________ kJ·mol-1。
Ⅱ.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g) 2NH3(g)。
2NH3(g)。
(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1 mol、0.3 mol时,平衡后混合物中氨的体积分数(φ)如下图所示。
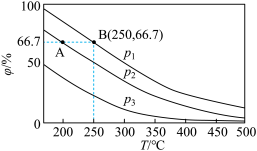
①其中,p1、p2和p3由大到小的顺序是______________________________ ,其原因是__________________________________________________________________ 。
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)________ vB(N2)(填“>”“<”或“=”)。
③若在250 ℃、p1为105 Pa条件下,反应达到平衡时容器的体积为1 L,则该条件下B点N2的分压p(N2)为_____________________ Pa (分压=总压×物质的量分数,保留一位小数)。
Ⅲ.以连二硫酸根(S2O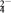 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:

(3)①阴极区的电极反应式为_________________________________ 。
②NO吸收转化后的主要产物为NH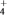 ,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为________ mL。
Ⅳ、常温下,将a mol·L-1的醋酸与b mol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=___________ (用含a和b的代数式表示)。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+205.9 kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9 kJ·mol-1 ①CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 ②二氧化碳重整:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③则反应①自发进行的条件是
Ⅱ.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)
 2NH3(g)。
2NH3(g)。(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1 mol、0.3 mol时,平衡后混合物中氨的体积分数(φ)如下图所示。

①其中,p1、p2和p3由大到小的顺序是
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)
③若在250 ℃、p1为105 Pa条件下,反应达到平衡时容器的体积为1 L,则该条件下B点N2的分压p(N2)为
Ⅲ.以连二硫酸根(S2O
 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
(3)①阴极区的电极反应式为
②NO吸收转化后的主要产物为NH
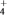 ,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为Ⅳ、常温下,将a mol·L-1的醋酸与b mol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】含氯化合物的反应在化学工业中具有重要的地位。回答下列问题:
(1)工业上,常用 检验输送氯气的管道是否泄漏。
检验输送氯气的管道是否泄漏。
已知: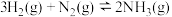
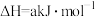
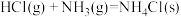
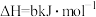


反应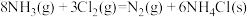 的
的
_______  。
。
(2)氯乙烷是重要的含氯化合物,常用于医药、农药的制造。可用乙烯和氯化氢反应制备氯乙烷,反应方程式为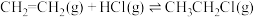 。在1L恒温恒容密闭容器中充入2.5
。在1L恒温恒容密闭容器中充入2.5
 和1.5
和1.5
 ,在催化剂作用下发生反应,测得
,在催化剂作用下发生反应,测得 及
及 的物质的量随时间变化如图1所示:
的物质的量随时间变化如图1所示:

①12.5s时反应恰好达到平衡,则0~12.5s内, 的平均反应速率为
的平均反应速率为_______  。
。
②第一次平衡时, 的平衡转化率为
的平衡转化率为_______ 。
③在第20s时,仅改变了某一个条件,则改变的条件是_______ ;第25s后,反应重新达到平衡,则该反应的平衡常数
_______ (保留两位有效数字)。
④在1L的恒温恒容密闭容器中发生上述反应,下列能说明反应已经达到平衡的是_______ (填标号)。
A.容器内气体的总压强不变
B.容器内碳元素的质量分数不变
C.单位时间内,断裂1
 键的同时,有1
键的同时,有1
 键形成
键形成
D.容器内气体的密度不变
(3)工业上常用氯苯(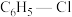 )和硫化氢(
)和硫化氢( )反应来制备一种用途广泛的有机合成中间体苯硫酚(
)反应来制备一种用途广泛的有机合成中间体苯硫酚( ),但会有副产物苯(
),但会有副产物苯( )生成,发生的反应如下:
)生成,发生的反应如下:
I.
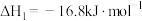 ;
;
II.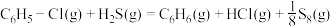
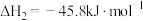 。
。
现将一定量的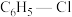 和
和 置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20min,测定生成物的浓度,得到图2和图3(R为
置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20min,测定生成物的浓度,得到图2和图3(R为 与
与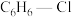 的起始物质的量之比)。
的起始物质的量之比)。

结合图2和图3,该模拟工业生产制备 的适宜条件为
的适宜条件为_______ 。
(1)工业上,常用
 检验输送氯气的管道是否泄漏。
检验输送氯气的管道是否泄漏。已知:
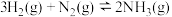
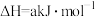
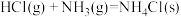
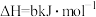


反应
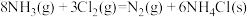 的
的
 。
。(2)氯乙烷是重要的含氯化合物,常用于医药、农药的制造。可用乙烯和氯化氢反应制备氯乙烷,反应方程式为
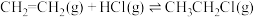 。在1L恒温恒容密闭容器中充入2.5
。在1L恒温恒容密闭容器中充入2.5
 和1.5
和1.5
 ,在催化剂作用下发生反应,测得
,在催化剂作用下发生反应,测得 及
及 的物质的量随时间变化如图1所示:
的物质的量随时间变化如图1所示:
①12.5s时反应恰好达到平衡,则0~12.5s内,
 的平均反应速率为
的平均反应速率为 。
。②第一次平衡时,
 的平衡转化率为
的平衡转化率为③在第20s时,仅改变了某一个条件,则改变的条件是

④在1L的恒温恒容密闭容器中发生上述反应,下列能说明反应已经达到平衡的是
A.容器内气体的总压强不变
B.容器内碳元素的质量分数不变
C.单位时间内,断裂1

 键的同时,有1
键的同时,有1
 键形成
键形成D.容器内气体的密度不变
(3)工业上常用氯苯(
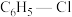 )和硫化氢(
)和硫化氢( )反应来制备一种用途广泛的有机合成中间体苯硫酚(
)反应来制备一种用途广泛的有机合成中间体苯硫酚( ),但会有副产物苯(
),但会有副产物苯( )生成,发生的反应如下:
)生成,发生的反应如下:I.

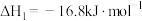 ;
;II.
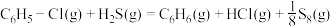
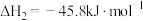 。
。现将一定量的
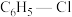 和
和 置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20min,测定生成物的浓度,得到图2和图3(R为
置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20min,测定生成物的浓度,得到图2和图3(R为 与
与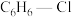 的起始物质的量之比)。
的起始物质的量之比)。
结合图2和图3,该模拟工业生产制备
 的适宜条件为
的适宜条件为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】【卷号】1931756177006592
【题号】1933708114804736
【推荐3】
汽车尾气中的氮氧化物气体是导致雾霾的要原因之一。请回答下列有关尾气治理的问题:
(1)用化学方程式解释汽车尾气中含有NO的原因_______________________________ 。
(2)汽车排气管内安装的催化转化器,可使汽车尾气中的主要污染物NO、CO转化为无毒的大气循环物质。
已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ•mol-1
2C(s)+O2(g)=2CO(g) △H= -221.0kJ•mol-1
C(s)+O2(g)=CO2(g) △H= -393.5 kJ•mol-1
则分析反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的△H=___________ kJ•mol-1。
(3)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中,在不同条件下反应过程中部分物质的浓度变化状况如图1所示。

①计算反应在第9-12 min时的平衡常数K=____________ 。
②第12 min时改变的反应条件可能是_____________ (任写一条)。
(4)某研究机构在实验室以Ag-ZSM-5为催化剂。测得单位时间内NO转化为N2的转化率随温度变化情况如图2所示。
①若不使用CO,发现当温度超过775 K时,NO的分解率降低,其可能的原因是________________ 。
②在n(NO)/n(CO) =1的条件下,为更好地除去NO,应控制的最佳温度应在____ K左右。
(5)氮氧化物进入水体可转化为NO3-,电化学降解法可用于治理水中NO3-的污染,原理如右图所示。则电源正极为______ (选填“A”或“B”),阴极电极反应式为__________________ 。

【题号】1933708114804736
【推荐3】
汽车尾气中的氮氧化物气体是导致雾霾的要原因之一。请回答下列有关尾气治理的问题:
(1)用化学方程式解释汽车尾气中含有NO的原因
(2)汽车排气管内安装的催化转化器,可使汽车尾气中的主要污染物NO、CO转化为无毒的大气循环物质。
已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ•mol-1
2C(s)+O2(g)=2CO(g) △H= -221.0kJ•mol-1
C(s)+O2(g)=CO2(g) △H= -393.5 kJ•mol-1
则分析反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的△H=
(3)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中,在不同条件下反应过程中部分物质的浓度变化状况如图1所示。

①计算反应在第9-12 min时的平衡常数K=
②第12 min时改变的反应条件可能是
(4)某研究机构在实验室以Ag-ZSM-5为催化剂。测得单位时间内NO转化为N2的转化率随温度变化情况如图2所示。
①若不使用CO,发现当温度超过775 K时,NO的分解率降低,其可能的原因是
②在n(NO)/n(CO) =1的条件下,为更好地除去NO,应控制的最佳温度应在
(5)氮氧化物进入水体可转化为NO3-,电化学降解法可用于治理水中NO3-的污染,原理如右图所示。则电源正极为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮的氧化物的催化还原是环保研究热点。
(1)常在催化条件下用 还原
还原 来消除氮氧化物的污染。已知:a、b都大于0。
来消除氮氧化物的污染。已知:a、b都大于0。
①
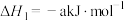
②



___________  (用含a、b的代数式表示)
(用含a、b的代数式表示)
(2)铜还原NO生成 可将NO转化为无污染物质:
可将NO转化为无污染物质:
 。向恒容密闭容器中充入NO和足量Cu,发生上述反应。
。向恒容密闭容器中充入NO和足量Cu,发生上述反应。
①达到平衡后,升高温度,NO的正反应速率___________ (填“大于”“小于”或“等于”)NO的逆反应速率。
②达到平衡后,增大Cu的质量,平衡___________ (填“向左”“向右”或“不”)移动。
(3)CO还原NO的反应为
 。向体积均为
。向体积均为 的甲、乙两个恒容密闭容器中分别充入
的甲、乙两个恒容密闭容器中分别充入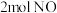 和
和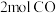 ,分别在绝热、恒温条件下发生上述反应。两反应体系中的压强随时间的变化曲线如图所示。
,分别在绝热、恒温条件下发生上述反应。两反应体系中的压强随时间的变化曲线如图所示。

①
___________ 0(填“>”“<”或“=”)。乙容器在___________ (填“绝热”或“恒温”)条件下进行。
②CO的转化率:a___________ b(填“>”“<”或“=”),判断依据是___________ 。
③a点
___________ 。b点平衡常数K___________ a点浓度商Q(填“>”“<”或“=”)。
(1)常在催化条件下用
 还原
还原 来消除氮氧化物的污染。已知:a、b都大于0。
来消除氮氧化物的污染。已知:a、b都大于0。①

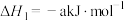
②




 (用含a、b的代数式表示)
(用含a、b的代数式表示)(2)铜还原NO生成
 可将NO转化为无污染物质:
可将NO转化为无污染物质:
 。向恒容密闭容器中充入NO和足量Cu,发生上述反应。
。向恒容密闭容器中充入NO和足量Cu,发生上述反应。①达到平衡后,升高温度,NO的正反应速率
②达到平衡后,增大Cu的质量,平衡
(3)CO还原NO的反应为

 。向体积均为
。向体积均为 的甲、乙两个恒容密闭容器中分别充入
的甲、乙两个恒容密闭容器中分别充入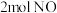 和
和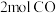 ,分别在绝热、恒温条件下发生上述反应。两反应体系中的压强随时间的变化曲线如图所示。
,分别在绝热、恒温条件下发生上述反应。两反应体系中的压强随时间的变化曲线如图所示。
①

②CO的转化率:a
③a点

您最近一年使用:0次
【推荐2】I.2022年3月30日,我国在酒泉卫星发射中心用长征十一号运载火箭,成功将天平二号A、B、C卫星发射升空。卫星,火箭的第一、二级发动机中,所用的燃料为偏二甲肼和四氧化二氮,偏二甲肼可用肼来制备。用肼 作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①
②
(1)写出气态肼和 反应的热化学方程式:
反应的热化学方程式:_____ 。
(2)已知 和
和 反应生成
反应生成 吸收
吸收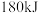 能量,反应过程中能量变化如下图所示。
能量,反应过程中能量变化如下图所示。
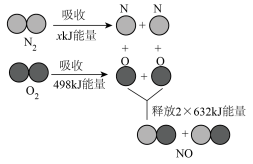
根据图示回答下列问题:断裂 吸收的能量x值为
吸收的能量x值为_____ 。
Ⅱ. (红棕色)和
(红棕色)和 (无色)之间发生反应:
(无色)之间发生反应: 。将一定量
。将一定量 气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
(3)下列可以说明该反应达到平衡的是_____。
(4)在温度为T的条件下,向该恒容密闭容器中充入 随时间的变化曲线如图所示。
随时间的变化曲线如图所示。

①在图中画出 时间段内,
时间段内,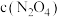 随时间的变化曲线
随时间的变化曲线_____ 。
②1~4四个点中, 的点有
的点有_____ 。
③反应进行到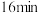 时,
时, 的转化率是
的转化率是_____ 。
④下列措施能使该反应速率加快的是_____ 。
A.增大 的浓度 B.增大容器体积 C.加入合适的催化剂 D.恒容条件下充入
的浓度 B.增大容器体积 C.加入合适的催化剂 D.恒容条件下充入
 作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:①

②

(1)写出气态肼和
 反应的热化学方程式:
反应的热化学方程式:(2)已知
 和
和 反应生成
反应生成 吸收
吸收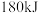 能量,反应过程中能量变化如下图所示。
能量,反应过程中能量变化如下图所示。
根据图示回答下列问题:断裂
 吸收的能量x值为
吸收的能量x值为Ⅱ.
 (红棕色)和
(红棕色)和 (无色)之间发生反应:
(无色)之间发生反应: 。将一定量
。将一定量 气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
气体充入体积为2L的恒容密闭容器中,控制反应温度为T。(3)下列可以说明该反应达到平衡的是_____。
A.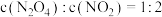 | B. |
| C.容器内气体的颜色不再变化 | D.混合气体的压强不再变化 |
 随时间的变化曲线如图所示。
随时间的变化曲线如图所示。
①在图中画出
 时间段内,
时间段内,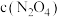 随时间的变化曲线
随时间的变化曲线②1~4四个点中,
 的点有
的点有③反应进行到
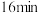 时,
时, 的转化率是
的转化率是④下列措施能使该反应速率加快的是
A.增大
 的浓度 B.增大容器体积 C.加入合适的催化剂 D.恒容条件下充入
的浓度 B.增大容器体积 C.加入合适的催化剂 D.恒容条件下充入
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氯乙烯是合成聚氯乙烯的单体,工业上常用乙烯氧氯化法制取,其主要反应为 。
。
(1)每生成1 g氯乙烯,放出_______ J的热量。
(2)工业上要提高氯乙烯的平衡产率,可采取的措施有_______(填标号)。
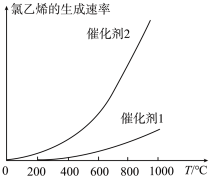
(3)催化剂的选择是合成氯乙烯的核心技术之一,使用催化剂1(反应的活化能为Ea1)或催化剂2(反应的活化能为Ea2)合成时,氯乙烯的生成速率与温度的关系如图。Ea1_______ (填“>”、“=”或“<”,下同)Ea2;当反应方程式相同时,使用催化剂1(反应的焓变为 或催化剂2(反应的焓变为
或催化剂2(反应的焓变为 )时,
)时,
_______  ;
;
(4)保持体系压强始终为0. 1 MPa,起始时充入4 mol C2H4、2 mol Cl2和1 mol O2,反应达到平衡后,5种组分的物质的量分数随温度T的变化如图所示。

①图中表示C2H4、H2O变化的曲线分别是_______ 、_______ 。(填标号)
②图中P点对应温度下,乙烯的转化率为_______ ,此时反应平衡常数Kp=_______  。
。
 。
。(1)每生成1 g氯乙烯,放出
(2)工业上要提高氯乙烯的平衡产率,可采取的措施有_______(填标号)。
| A.升高温度 | B.增大压强 |
| C.不断分离出水蒸气 | D.加入合适的催化剂 |
 或催化剂2(反应的焓变为
或催化剂2(反应的焓变为 )时,
)时,
 ;
;
(4)保持体系压强始终为0. 1 MPa,起始时充入4 mol C2H4、2 mol Cl2和1 mol O2,反应达到平衡后,5种组分的物质的量分数随温度T的变化如图所示。

①图中表示C2H4、H2O变化的曲线分别是
②图中P点对应温度下,乙烯的转化率为
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】海洋资源的利用具有广阔前景。
(1)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是___________ (填序号)
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式___________ 。
③用CCl4提取碘时除了用CCl4还可以选用的试剂是___________ (填字母序号)
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:___________ 。
(2)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH=K2CO3+3H2O,则该燃料电池的负极的电极反应为___________ 。
(3)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a、b、c、d括号内数据表示坐标。
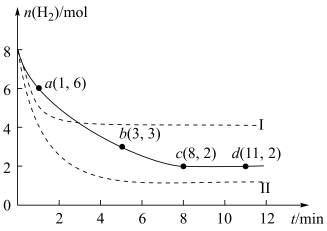
①a点正反应速率___________ (填“大于”“等于”或“小于”)a点逆反应速率。
②平衡时CO2的物质的量浓度是___________ mol/L。
③能够说明该反应达到化学平衡状态的标志是___________ (双选)。
A.单位时间内消耗1 mol CO2,同时生成3 mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
(1)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③用CCl4提取碘时除了用CCl4还可以选用的试剂是
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:
(2)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH=K2CO3+3H2O,则该燃料电池的负极的电极反应为
(3)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a、b、c、d括号内数据表示坐标。

①a点正反应速率
②平衡时CO2的物质的量浓度是
③能够说明该反应达到化学平衡状态的标志是
A.单位时间内消耗1 mol CO2,同时生成3 mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】请根据下列各题要求填空。
(1)已知CO(g)和CH3OH(l)的燃烧热△H分别为-283.0 kJ/mol和-726.5 kJ/mol。请写出甲醇不完全烧生成一氧化碳和液态水的热化学方程式:_______ 。
(2)用离子方程式表示泡沫灭火器灭火原理:_______ 。
(3)物质的量浓度相同的NaOH溶液、NH4Cl溶液等体积混合后,所得溶液中离子浓度由大到小的顺序是_______ 。
(4)一定温度、体积的密闭容器中,可逆反应A(s)+3B(g) 2C(g)达到平衡时,下列说法能判断该反应达到平衡的有
2C(g)达到平衡时,下列说法能判断该反应达到平衡的有_______ 。
①C的生成速率和C的分解速率相等
②单位时间内生成a mol A,同时生成3a mol B
③混合气体的密度不再变化
④A、B、C物质的量之比为1:3:2
⑤混合气体的总压强不再变化
⑥混合气体的平均相对分子质量不变
⑦容器中C的体积分数不变
(5)室温下,用0.100 mol/L盐酸溶液滴定20.00 mL0.100 mol/L的氨水溶液,滴定曲线如图所示。 点所示的溶液中c(Cl-)
点所示的溶液中c(Cl-) _______  (填“>”“<”或“
(填“>”“<”或“ ”)。
”)。

(1)已知CO(g)和CH3OH(l)的燃烧热△H分别为-283.0 kJ/mol和-726.5 kJ/mol。请写出甲醇不完全烧生成一氧化碳和液态水的热化学方程式:
(2)用离子方程式表示泡沫灭火器灭火原理:
(3)物质的量浓度相同的NaOH溶液、NH4Cl溶液等体积混合后,所得溶液中离子浓度由大到小的顺序是
(4)一定温度、体积的密闭容器中,可逆反应A(s)+3B(g)
 2C(g)达到平衡时,下列说法能判断该反应达到平衡的有
2C(g)达到平衡时,下列说法能判断该反应达到平衡的有①C的生成速率和C的分解速率相等
②单位时间内生成a mol A,同时生成3a mol B
③混合气体的密度不再变化
④A、B、C物质的量之比为1:3:2
⑤混合气体的总压强不再变化
⑥混合气体的平均相对分子质量不变
⑦容器中C的体积分数不变
(5)室温下,用0.100 mol/L盐酸溶液滴定20.00 mL0.100 mol/L的氨水溶液,滴定曲线如图所示。
 点所示的溶液中c(Cl-)
点所示的溶液中c(Cl-)  (填“>”“<”或“
(填“>”“<”或“ ”)。
”)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】工业上通过丁烷裂解可以获得乙烯和丙烯等化工原料:
①C4H10(丁烷,g) CH4(g)+C3H6(丙烯,g);
CH4(g)+C3H6(丙烯,g);
②C4H10(丁烷,g) C2H6(g)+C2H4(g)。
C2H6(g)+C2H4(g)。
(1)丙烯和乙烯均能与Br2发生加反应,标准状况下,33.6L由丙烯和乙烯组成的混合气体与足量的溴水反应,最多消耗
(2)向一体积为2L的恒容密团容器中充入2 mol丁烷,在一定温度和催化剂作用下发生上述2个反应,测得丁烷、丙烯的物质的量与时间关系如图所示。

①下列情况表明上述反应达到平衡状态的是
A.混合气体密度不随时间变化 B.混合气体平均摩尔质量不随时间变化
C.混合气体总压强不随时间变化 D.混合气体中碳原子总数不随时间变化
E.体系中各物质的浓度相等
②0 -4 min内,乙烷的平均反应速率为
③在该条件下,丁烷的平衡转化率为
④平衡体系中,n(乙烯):n(丙烯)=
您最近一年使用:0次
【推荐1】工业生产硫酸中,SO2的催化氧化是关键步骤,排放处理未达标的尾气会产生严重的空气污染。回答下列问题:
(1)SO2是形成酸雨的污染物之一,酸雨的pH范围是___________ 。
(2)已知:①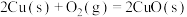
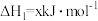
②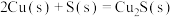
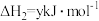
③
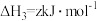
写出Cu2S和O2反应生成 和SO2的热化学方程式
和SO2的热化学方程式___________ 。
(3)硫酸工业中涉及反应: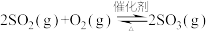
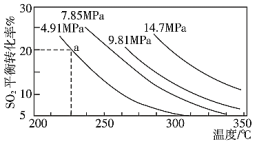
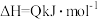 。一定条件下,在恒压密闭容器中,通入2 molSO2和1 mol O2发生上述反应,
。一定条件下,在恒压密闭容器中,通入2 molSO2和1 mol O2发生上述反应, 的平衡转化率和压强、温度的关系如图所示。a点时该反应的压强平衡常数Kp=
的平衡转化率和压强、温度的关系如图所示。a点时该反应的压强平衡常数Kp=___________ (保留三位有效数字,已知:分压=气体总压强×该气体的物质的量分数,用各气体物质的分压替代浓度计算的平衡常数叫压强平衡常数)。恒压条件下,关于该反应的下列说法中正确的是___________ 。
A.Q大于0
B.相同时间内生成0.2 mol SO2,同时消耗0.1 mol O2,反应达到平衡
C.相同温度下压强越大,SO2的转化率就越大,该反应的平衡常数就越大
D.反应达到平衡后,保持温度不变,再充入2 mol SO2和1 mol O2,SO2的平衡转化率不变
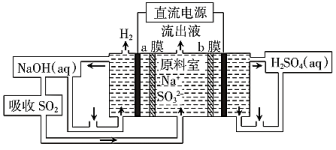
(4)用如图装置回收SO2,可制得硫酸,电极均为惰性电极,a、b膜分别为阳离子、阴离子交换膜,写出阴极的电极反应式___________ 。当阴极收集到标准状况下的H2 44.8 L时,理论上在阳极能得到___________ gH2SO4。
(1)SO2是形成酸雨的污染物之一,酸雨的pH范围是
(2)已知:①
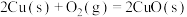
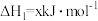
②
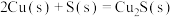
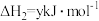
③

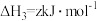
写出Cu2S和O2反应生成
 和SO2的热化学方程式
和SO2的热化学方程式(3)硫酸工业中涉及反应:
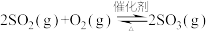
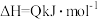 。一定条件下,在恒压密闭容器中,通入2 molSO2和1 mol O2发生上述反应,
。一定条件下,在恒压密闭容器中,通入2 molSO2和1 mol O2发生上述反应, 的平衡转化率和压强、温度的关系如图所示。a点时该反应的压强平衡常数Kp=
的平衡转化率和压强、温度的关系如图所示。a点时该反应的压强平衡常数Kp=
A.Q大于0
B.相同时间内生成0.2 mol SO2,同时消耗0.1 mol O2,反应达到平衡
C.相同温度下压强越大,SO2的转化率就越大,该反应的平衡常数就越大
D.反应达到平衡后,保持温度不变,再充入2 mol SO2和1 mol O2,SO2的平衡转化率不变
(4)用如图装置回收SO2,可制得硫酸,电极均为惰性电极,a、b膜分别为阳离子、阴离子交换膜,写出阴极的电极反应式

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】党的二十大报告中强调“实现碳达峰碳中和是一场广泛而深刻的经济社会系统性变革”。
 的转化和利用是实现碳中和的有效途径。回答下列问题:
的转化和利用是实现碳中和的有效途径。回答下列问题:
Ⅰ.利用 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
①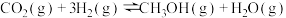
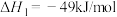
②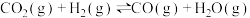
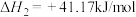
③

(1)反应③中活化能
__________ (填“>”或“<”)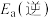 。
。
(2)在催化剂作用下,按 的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时
的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示: 。
。
①从图中曲线的变化趋势分析a点之后温度升高,甲醇选择性降低的原因__________ ,在实际工业生产中压强不能过高也不能过低的原因是____________ 。
② 时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则
时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则 的分压=
的分压=__________ MPa,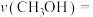
__________ MPa/min,反应②的
__________ ( 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
Ⅱ.近年来,有研究人员用 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示:
的回收利用,其工作原理如图所示: ,则该电极反应式为
,则该电极反应式为____________________ 。

 的转化和利用是实现碳中和的有效途径。回答下列问题:
的转化和利用是实现碳中和的有效途径。回答下列问题:Ⅰ.利用
 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:①
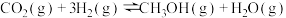
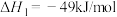
②
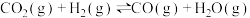
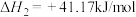
③


(1)反应③中活化能

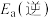 。
。(2)在催化剂作用下,按
 的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时
的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示:
 。
。①从图中曲线的变化趋势分析a点之后温度升高,甲醇选择性降低的原因
②
 时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则
时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则 的分压=
的分压=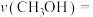

 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。Ⅱ.近年来,有研究人员用
 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示:
的回收利用,其工作原理如图所示: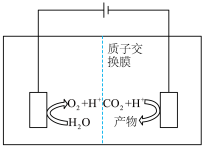
 ,则该电极反应式为
,则该电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】本题有三种新技术处理空气污染物,请回答相关问题。
I.NH3选择性催化还原NO(NH3—SCR)技术在燃煤电厂烟气脱硝过程中有着重要的应用。该方法主要反应的热化学方程式为4NH3(g)+4NO(g)+O2(g)⇌4N2(g)+6H2O(g) ∆H0
已知:2H2(g)+O2(g)⇌2H2O(g) ∆H1=-484kJ·mol-1
(1)计算4NH3(g)+4NO(g)+O2(g)⇌4N2(g)+6H2O(g) ∆H=___________ kJ·mol-1。
(2)利用NH3-SCR技术催化还原氮氧化物,反应原理如图甲所示:

当NO2、NO与足量氨气在一定条件下发生反应,且参与反应的NO2和NO的物质的量之比为1:2。若有2molNO2参与反应,则整个过程中转移的电子数目为___________
II.CO可作为工业合成甲醇的直接碳源,利用CO和H2反应合成甲醇的原理为CO(g)+2H2(g)⇌CH3OH(g)。在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图乙所示。

(3)其他条件相同时,B点和C点反应速率的大小关系为B___________ C(填“>”“<"或“=”),判断的依据是___________ 。
(4)在B点时,CO的转化率为___________ 。
(5)计算300°C,P2kPa时的平衡常数Kp=___________ 。(用含P2的式子表示。以分压表示,分压=总压×体积分数)。
III.氮的氧化物脱除可以利用电化学原理处理,利用如图装置可同时吸收SO2和NO。已知:H2S2O4是一种弱酸。

(6)阴极的电极反应式为________ 。若没有能量损失,相同条件下,SO2和NO的体积比为_______ 时,两种气体都能被完全处理。
I.NH3选择性催化还原NO(NH3—SCR)技术在燃煤电厂烟气脱硝过程中有着重要的应用。该方法主要反应的热化学方程式为4NH3(g)+4NO(g)+O2(g)⇌4N2(g)+6H2O(g) ∆H0
已知:2H2(g)+O2(g)⇌2H2O(g) ∆H1=-484kJ·mol-1
N2(g)+3H2(g)⇌2NH3(g) ∆H2=-92.4kJ·mol-1
N2(g)+O2(g)⇌2NO(g) ∆H3=+180.5kJ·mol-1
(1)计算4NH3(g)+4NO(g)+O2(g)⇌4N2(g)+6H2O(g) ∆H=
(2)利用NH3-SCR技术催化还原氮氧化物,反应原理如图甲所示:

当NO2、NO与足量氨气在一定条件下发生反应,且参与反应的NO2和NO的物质的量之比为1:2。若有2molNO2参与反应,则整个过程中转移的电子数目为
II.CO可作为工业合成甲醇的直接碳源,利用CO和H2反应合成甲醇的原理为CO(g)+2H2(g)⇌CH3OH(g)。在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图乙所示。

(3)其他条件相同时,B点和C点反应速率的大小关系为B
(4)在B点时,CO的转化率为
(5)计算300°C,P2kPa时的平衡常数Kp=
III.氮的氧化物脱除可以利用电化学原理处理,利用如图装置可同时吸收SO2和NO。已知:H2S2O4是一种弱酸。

(6)阴极的电极反应式为
您最近一年使用:0次



