工业上生产CO的反应原理为
 。一定条件下,将足量焦炭和一定量
。一定条件下,将足量焦炭和一定量 放入体积为2L的恒容密闭容器中发生反应,
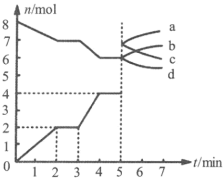
放入体积为2L的恒容密闭容器中发生反应, 和CO的物质的量n随时间t的变化关系如图。下列说法正确的是
和CO的物质的量n随时间t的变化关系如图。下列说法正确的是

 。一定条件下,将足量焦炭和一定量
。一定条件下,将足量焦炭和一定量 放入体积为2L的恒容密闭容器中发生反应,
放入体积为2L的恒容密闭容器中发生反应, 和CO的物质的量n随时间t的变化关系如图。下列说法正确的是
和CO的物质的量n随时间t的变化关系如图。下列说法正确的是
A.0~2min,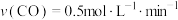 ;2~3min, ;2~3min, |
B.当容器内的气体密度( )不变时,反应一定达到平衡状态,且 )不变时,反应一定达到平衡状态,且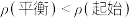 |
C.3min时温度由 升高到 升高到 ,则 ,则 ,平衡常数 ,平衡常数 |
D.5min时再充入一定量的CO,a、d曲线分别表示 、 、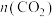 的变化 的变化 |
23-24高三上·辽宁锦州·期末 查看更多[3]
山东省青岛第五十八中学2023-2024学年高二下学期期初考试化学试卷 (已下线)题型12 化学平衡图表分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)辽宁省锦州市2023-2024学年高三上学期1月期末化学试题
更新时间:2024-01-13 11:44:18
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
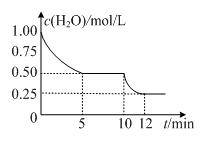
【推荐1】在2L密闭容器中进行反应C(s)+H2O(g) CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
 CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
| A.5min时该反应的K值一定小于12 min时的K值 |
| B.0~5min内,v (H2)=0.05mol/(L•min) |
| C.10 min时,改变的外界条件可能是减小压强 |
| D.该反应混合气体的平均相对分子质量:5min时小于12 min 时的 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】T℃,将2 mol X和1 mol Y充入体积为1L的密闭容器中,已知:2X(s)+Y(g)  2Z(g) △H=-M kJ·mol-1。10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法正确的是
2Z(g) △H=-M kJ·mol-1。10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法正确的是
 2Z(g) △H=-M kJ·mol-1。10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法正确的是
2Z(g) △H=-M kJ·mol-1。10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法正确的是| A.在第10 min时,Z的反应速率为0.02 mol·L-1·min-l |
B.在0~10 min内,Y的反应速率为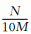 mol·L-1·min-l mol·L-1·min-l |
| C.增加X的物质的量可以加快反应速率 |
| D.反应达平衡后,保持T℃,通入稀有气体增加压强,则化学反应速率变快 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某烟气中含N2、O2、SO2等气体,以FeSO4催化氧化处理其中的SO2,部分流程如图1所示。实验开始时需向“脱硫”装置中加入一定量的FeSO4溶液,并加入适量铁粉。保持其他条件相同,吸收液的起始温度对脱硫率和吸收液pH的影响如图2所示: 2H2SO4。反应过程中Fe2+作催化剂,发生I和II两个反应,其中反应I为4Fe2++O2+4H+=4Fe3++2H2O
2H2SO4。反应过程中Fe2+作催化剂,发生I和II两个反应,其中反应I为4Fe2++O2+4H+=4Fe3++2H2O
ii.当溶液的pH约为5.4时,有利于SO2的脱除。
下列说法不正确 的是

 2H2SO4。反应过程中Fe2+作催化剂,发生I和II两个反应,其中反应I为4Fe2++O2+4H+=4Fe3++2H2O
2H2SO4。反应过程中Fe2+作催化剂,发生I和II两个反应,其中反应I为4Fe2++O2+4H+=4Fe3++2H2Oii.当溶液的pH约为5.4时,有利于SO2的脱除。
下列说法
| A.为提高SO2的脱除率,烟气通入的速率不宜过快 |
B.反应II为SO2+2Fe3++2H2O=2Fe2++4H++ |
| C.温度大于60℃时脱硫率下降,原因是H2SO4受热分解为SO2 |
| D.“脱硫”后溶液pH约为5.5,原因是加入的Fe将H2SO4转化为FeSO4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 在电子、光学和催化剂领域有广泛应用,设计通过
在电子、光学和催化剂领域有广泛应用,设计通过 制备
制备 和
和 制备
制备 的反应原理分别如下:I.
的反应原理分别如下:I.

Ⅱ.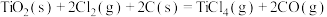
 。
。
下列说法错误的是
 在电子、光学和催化剂领域有广泛应用,设计通过
在电子、光学和催化剂领域有广泛应用,设计通过 制备
制备 和
和 制备
制备 的反应原理分别如下:I.
的反应原理分别如下:I.

Ⅱ.
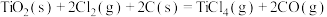
 。
。下列说法错误的是
| A.反应I能自发进行主要是焓减驱动 |
| B.反应I的体系中加入碳粉,可改变反应进行的方向 |
| C.反应Ⅱ正反应的活化能比逆反应的活化能大 |
D.减小压强和降低温度,会降低反应Ⅱ的速率,但可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】一种绿色甲醇的生产方法是:通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制取甲醇。
主反应:
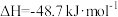
副反应:
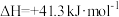
将 和
和 按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知:
按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知: 的产率=
的产率=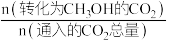 。下列说法错误的是
。下列说法错误的是
主反应:

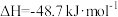
副反应:

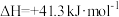
将
 和
和 按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知:
按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知: 的产率=
的产率=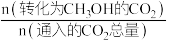 。下列说法错误的是
。下列说法错误的是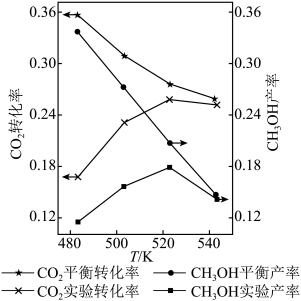
| A.由图可知,催化剂活性最好的温度大约在523K |
| B.483K升温到523K,主反应的反应速率受温度影响更大 |
C.温度由523K升到543K, 的实验产率快速降低的主要原因可能是:温度升高,催化剂的活性降低,导致主反应速率迅速减小 的实验产率快速降低的主要原因可能是:温度升高,催化剂的活性降低,导致主反应速率迅速减小 |
D.为了提高 的平衡转化率和 的平衡转化率和 的平衡产率,可以选择低温、低压条件 的平衡产率,可以选择低温、低压条件 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】在2L密闭容器中进行反应C(s)+H2O(g) CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是

 CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
| A.5min时该反应的K值一定小于12 min时的K值 |
| B.0~5min内,v (H2)=0.05mol/(L•min) |
| C.10 min时,改变的外界条件可能是减小压强 |
| D.该反应混合气体的平均相对分子质量:5min时小于12 min 时的 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】 制
制 的平衡体系中存在如下反应:
的平衡体系中存在如下反应:
反应Ⅰ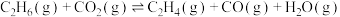

反应Ⅱ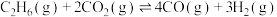

将2 mol 和3 mol
和3 mol  投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性(
投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性( 条件下)与温度、压强的关系如图所示。已知:乙烯的选择性
条件下)与温度、压强的关系如图所示。已知:乙烯的选择性 。下列说法错误的是
。下列说法错误的是
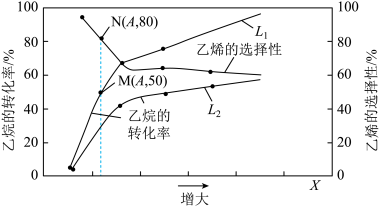
 制
制 的平衡体系中存在如下反应:
的平衡体系中存在如下反应:反应Ⅰ
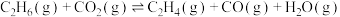

反应Ⅱ
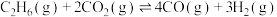

将2 mol
 和3 mol
和3 mol  投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性(
投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性( 条件下)与温度、压强的关系如图所示。已知:乙烯的选择性
条件下)与温度、压强的关系如图所示。已知:乙烯的选择性 。下列说法错误的是
。下列说法错误的是
| A.X代表温度,L代表压强 |
B.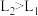 |
C.N点时, 转化成的CO的物质的量为0.4 mol 转化成的CO的物质的量为0.4 mol |
| D.M点时,反应Ⅰ的平衡常数为0.5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0~t1阶段c(B)未画出]。图乙为t2时刻后改变条件平衡体系中化学反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件并且改变的条件均不同。已知,t3~t4阶段为使用催化剂。下列说法正确的是


| A.t5~t6阶段可能是减小压强 |
| B.t4~t5阶段改变的条件为降低反应温度 |
| C.B的起始物质的量为0.02mol |
| D.若t1=15s,生成物C在t0~t1时间段的化学反应速率为0.004mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】随着聚酯工业的快速发展, 的需求量和HCl的产出量也随之迅速增长。Deacon发明了直接氧化HCl制备
的需求量和HCl的产出量也随之迅速增长。Deacon发明了直接氧化HCl制备 的反应:
的反应: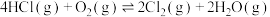 。如图为某刚性容器中,进料浓度比
。如图为某刚性容器中,进料浓度比
 分别等于1∶1、4∶1、7∶1时,HCl的平衡转化率随温度变化的关系。下列关于该反应的说法正确的是
分别等于1∶1、4∶1、7∶1时,HCl的平衡转化率随温度变化的关系。下列关于该反应的说法正确的是

 的需求量和HCl的产出量也随之迅速增长。Deacon发明了直接氧化HCl制备
的需求量和HCl的产出量也随之迅速增长。Deacon发明了直接氧化HCl制备 的反应:
的反应: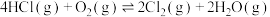 。如图为某刚性容器中,进料浓度比
。如图为某刚性容器中,进料浓度比
 分别等于1∶1、4∶1、7∶1时,HCl的平衡转化率随温度变化的关系。下列关于该反应的说法正确的是
分别等于1∶1、4∶1、7∶1时,HCl的平衡转化率随温度变化的关系。下列关于该反应的说法正确的是
A.相同条件下,升高温度可以提高 的产率 的产率 |
B.曲线Ⅰ表示进料浓度比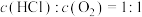 |
C.进料浓度比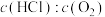 越大,平衡常数K越小 越大,平衡常数K越小 |
| D.该反应在低温条件下更易自发进行 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将一定量的氨基甲酸铵置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
下列有关叙述正确的是
 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
| A.在低温下该反应能自发进行 |
| B.15℃时,该反应的化学平衡常数约为2.0 |
| C.当混合气体平均相对分子质量不变时,该反应达到化学反应限度 |
| D.恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变 |
您最近一年使用:0次

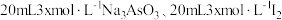 和
和 溶液混合,发生反应:
溶液混合,发生反应: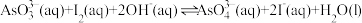 。溶液中
。溶液中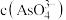 与反应时间
与反应时间 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是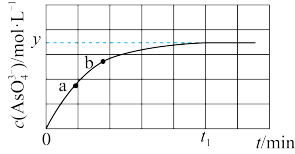
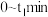 用
用 表示的平均反应速率为
表示的平均反应速率为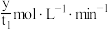
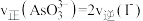 时,反应达到平衡状态
时,反应达到平衡状态 ,则该反应的平衡常数
,则该反应的平衡常数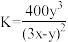
 能与
能与 按
按 结合形成多种粒子,六步反应的平衡常数依次用
结合形成多种粒子,六步反应的平衡常数依次用 表示。25℃时,各粒子的物质的量分数
表示。25℃时,各粒子的物质的量分数 与
与 的关系如图所示。下列叙述正确的是(
的关系如图所示。下列叙述正确的是(
 依次增大
依次增大
 的
的



