污染的大气使臭氧层中 催化分解的反应机理与总反应可表示为:
催化分解的反应机理与总反应可表示为:
第一步: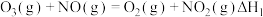
第二步: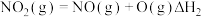
第三步: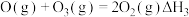
总反应: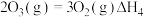
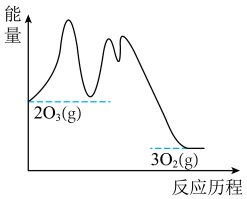
其能量与反应历程的关系如图所示。下列叙述正确的是
 催化分解的反应机理与总反应可表示为:
催化分解的反应机理与总反应可表示为:第一步:
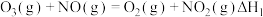
第二步:
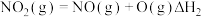
第三步:
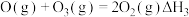
总反应:
其能量与反应历程的关系如图所示。下列叙述正确的是

A. 是该反应的催化剂 是该反应的催化剂 | B.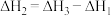 |
C.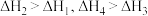 | D.决定总反应速率的是第二步 |
更新时间:2024-03-09 20:45:41
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列变化中只存在放热过程的是( )
| A.氯化钠晶体熔化 | B.氢氧化钠晶体溶于水 |
| C.液氮的气化 | D.水蒸气的液化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关热化学方程式的叙述,正确的是( )
| A.反应物的总能量低于生成物的总能量时,该反应必须加热才能发生 |
| B.由N2O4(g)⇌2NO2(g) ΔH=+56.9kJ·mol-1,可知将1molN2O4(g)置于密闭容器中充分反应后吸收的热量为56.9kJ |
| C.由:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,可知含1molHCN的稀溶液与含1molNaOH的稀溶液混合,放出热量为57.3kJ |
| D.已知101kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1,则1mol碳完全燃烧放出的热量大于110.5kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】证据推理与模型认知是化学学科的核心素养之一、下列事实与相应定律或原理相符的是
| A.向漂白液中加入少量稀硫酸能增强漂白液的漂白效果——元素周期律 |
| B.常温常压下,1体积乙醇完全燃烧消耗3体积O2——阿伏加德罗定律 |
| C.通过测量C、CO的燃烧热来间接计算2C(s)+O2(g)=2CO(g)的反应热——盖斯定律 |
| D.体积可变密闭容器中加入等体积的H2和I2(g),加压体系颜色加深——勒夏特列原理 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列图示与对应的叙述相符合的是
A. 表示对某化学平衡体系改变温度后反应速率随时间的变化 表示对某化学平衡体系改变温度后反应速率随时间的变化 |
B. 表示反应物断键吸收的总能量大于生成物成键放出的总能量 表示反应物断键吸收的总能量大于生成物成键放出的总能量 |
C.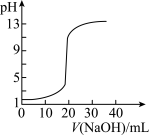 表示0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化 表示0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化 |
D. 表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况 表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知强酸与强碱的稀溶液发生中和反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,向0.1 L 0.2 mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀盐酸,恰好完全反应。则其焓变ΔH1、ΔH2、ΔH3的关系是
| A.ΔH1>ΔH2>ΔH3 | B.ΔH1>ΔH3>ΔH2 | C.ΔH1=ΔH3>ΔH2 | D.ΔH1<ΔH3<ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ·mol-1。分别向1 L0.5mol·L-1的NaOH的溶液中加入①醋酸;②稀硫酸;③稀盐酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是 ( )
| A.△H1>△H2>△H3 | B.△H1<△H2<△H3 |
| C.△H1>△H2=△H3 | D.△H1=△H2<△H3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 蒸干并灼烧AlCl3溶液 | 得到白色固体 | 获得Al2O3固体 |
| B | 分别将1 mL pH=3的HA和HB溶液加水稀释至100mL,测溶液pH | pH(HA)>pH(HB) | 酸性:HA<HB |
| C | 向某溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 溶液中存在Fe2+ |
| D | 向A、B两支试管中各加入2 mL10%的H2O2溶液,向B试管中加入2滴1mol/LFeCl3溶液 | B试管中产生气泡速率快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】化学反应速率与生产、生活密切相关。以下措施能减慢化学反应速率的是
| A.用煤粉代替煤块燃烧 |
| B.食物存放在冰箱里 |
C. 分解制 分解制 时加入少量 时加入少量 |
D.用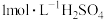 代替 代替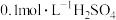 与锌粒反应制 与锌粒反应制 |
您最近一年使用:0次


 从催化剂表面脱离的过程
从催化剂表面脱离的过程 为吸热反应
为吸热反应 ∆H,该反应分两步进行:
∆H,该反应分两步进行: ∆H1=+akJ∙mol-1
∆H1=+akJ∙mol-1 ∆H2=-bkJ∙mol-1
∆H2=-bkJ∙mol-1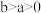 ,下列说法正确的是
,下列说法正确的是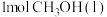 时,放出的热量小于bkJ
时,放出的热量小于bkJ 和足量
和足量 完全反应生成
完全反应生成 和
和 时吸收的能量是
时吸收的能量是
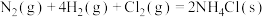

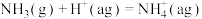

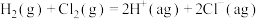
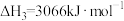



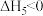
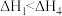
 ,
,

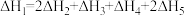
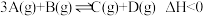 ,下列说法正确的是
,下列说法正确的是

