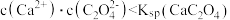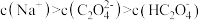电位滴定是利用溶液电位突变指示终点的滴定法。常温下,用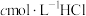 标准溶液测定VmL某生活用品中
标准溶液测定VmL某生活用品中 的含量(假设其他物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位E与V(HCl)的关系如图所示。已知:两个滴定终点时消耗盐酸的体积差可计算出
的含量(假设其他物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位E与V(HCl)的关系如图所示。已知:两个滴定终点时消耗盐酸的体积差可计算出 的量。下列说法正确的是
的量。下列说法正确的是
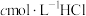 标准溶液测定VmL某生活用品中
标准溶液测定VmL某生活用品中 的含量(假设其他物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位E与V(HCl)的关系如图所示。已知:两个滴定终点时消耗盐酸的体积差可计算出
的含量(假设其他物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位E与V(HCl)的关系如图所示。已知:两个滴定终点时消耗盐酸的体积差可计算出 的量。下列说法正确的是
的量。下列说法正确的是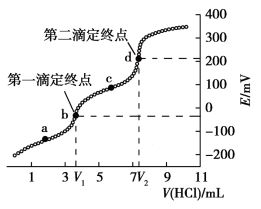
| A.水的电离程度:a>b>d>c |
B.a至c点对应溶液中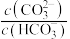 逐渐增大 逐渐增大 |
C.VmL生活用品中含有 的质量为 的质量为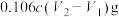 |
D.b点溶液中,离子浓度排序: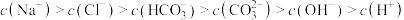 |
2024·辽宁·一模 查看更多[2]
更新时间:2024-03-27 22:04:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,向1 L浓度为0.4 mol·L-1的乙醇酸[CH2(OH)COOH]溶液中加入8 g NaOH固体得到X溶液,将X溶液平均分成两等份,一份通入HCl气体,得到溶液Y,另一份加入NaOH固体得到溶液Z,溶液Y、Z的pH随所加物质的物质的量的变化情况如图所示(体积变化忽略不计)。下列说法正确的是


| A.c点对应曲线代表的是加入NaOH的曲线 |
| B.溶液中水的电离程度:c>b |
| C.a点:c[CH2(OH)COO-]>c(Na+)>c(H+)>c(OH-) |
D.稀释Y溶液后,溶液中 变大 变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】用NaOH标准溶液滴定未知浓度的盐酸(盐酸放置于锥形瓶),若测定结果偏低,原因可能是
| A.锥形瓶洗净后残留少量蒸馏水 |
| B.滴定前滴定管内有气泡,滴定后气泡消失 |
| C.滴定过程中锥形瓶中溶液变色后立即停止滴定 |
| D.标准液读数时,滴定前俯视,滴定后仰视 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下,通过下列实验探究 溶液的性质。
溶液的性质。
下列说法正确的是
 溶液的性质。
溶液的性质。| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测得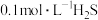 溶液的pH为4 溶液的pH为4 |
| 2 | 向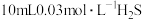 溶液中加入 溶液中加入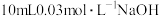 溶液,再滴加酚酞溶液,溶液颜色变红 溶液,再滴加酚酞溶液,溶液颜色变红 |
| 3 | 向2中所得溶液中继续加入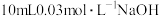 溶液,溶液红色加深 溶液,溶液红色加深 |
| 4 | 向3中所得溶液中继续加入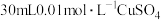 溶液,出现黑色沉淀 溶液,出现黑色沉淀 |
A.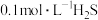 溶液中存在 溶液中存在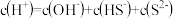 |
B.实验2所得溶液中存在 |
C.实验3所得溶液中存在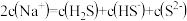 |
D.若忽略溶液混合时的体积变化,依据实验4的现象,可得出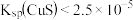 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将一定浓度的盐酸和氨水混合后,离子浓度之间的关系不可能出现的是
| A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) | B.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.c(NH4+)>c(Cl-)>c(OH-)>c(H+) | D.c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温常压下,将amolCO2气体通入1Lbmol•L-1的NaOH溶液中,下列对所得溶液的描述不正确的是


| A.当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图变化关系 |
B.当a=b时,所得溶液中存在:c(OH-)+c( )=c(H+)+c(H2CO3) )=c(H+)+c(H2CO3) |
C.当2a=b时,所得溶液中存在:c(Na+)>c( )>c(OH-)>c( )>c(OH-)>c( )>(H+) )>(H+) |
D.当 < < <1时,所得溶液中一定存在:c(Na+)=c( <1时,所得溶液中一定存在:c(Na+)=c( )+c( )+c( )+c(H2CO3) )+c(H2CO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
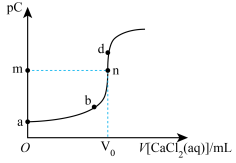
【推荐1】常温下,向20 mL 0.1 mol·L-1 Na2CO3溶液中滴加0.1 mol·L-1 CaCl2溶液,CO 浓度与CaCl2溶液体积的关系如图所示。已知:pC= −lg c(CO
浓度与CaCl2溶液体积的关系如图所示。已知:pC= −lg c(CO ),Ksp(CdCO3)=1.0×10-12,Ksp(CaCO3)=3.6×10-9。下列说法正确的是
),Ksp(CdCO3)=1.0×10-12,Ksp(CaCO3)=3.6×10-9。下列说法正确的是
 浓度与CaCl2溶液体积的关系如图所示。已知:pC= −lg c(CO
浓度与CaCl2溶液体积的关系如图所示。已知:pC= −lg c(CO ),Ksp(CdCO3)=1.0×10-12,Ksp(CaCO3)=3.6×10-9。下列说法正确的是
),Ksp(CdCO3)=1.0×10-12,Ksp(CaCO3)=3.6×10-9。下列说法正确的是
A.a点溶液:c(OH−) < 2c(HCO )+2c(H2CO3) )+2c(H2CO3) |
| B.图像中V0=20,m=5 |
| C.水的电离程度:a<b<n |
| D.若用CdCl2溶液替代CaCl2溶液,则n点向b点方向迁移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,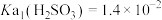 ,
, ,通过下列实验探究
,通过下列实验探究 、
、 溶液的性质。
溶液的性质。
实验1:用pH试纸测量0.1
 溶液的pH,测得pH约为5。
溶液的pH,测得pH约为5。
实验2:向0.1
 溶液中通入少量
溶液中通入少量 ,测得溶液pH约为8。
,测得溶液pH约为8。
实验3:向 溶液中滴几滴酚酞,加水稀释,溶液红色变浅。
溶液中滴几滴酚酞,加水稀释,溶液红色变浅。
实验4:向 溶液中滴加少量
溶液中滴加少量 溶液,产生白色沉淀。
溶液,产生白色沉淀。
下列所得结论正确的是
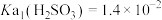 ,
, ,通过下列实验探究
,通过下列实验探究 、
、 溶液的性质。
溶液的性质。实验1:用pH试纸测量0.1

 溶液的pH,测得pH约为5。
溶液的pH,测得pH约为5。实验2:向0.1

 溶液中通入少量
溶液中通入少量 ,测得溶液pH约为8。
,测得溶液pH约为8。实验3:向
 溶液中滴几滴酚酞,加水稀释,溶液红色变浅。
溶液中滴几滴酚酞,加水稀释,溶液红色变浅。实验4:向
 溶液中滴加少量
溶液中滴加少量 溶液,产生白色沉淀。
溶液,产生白色沉淀。下列所得结论正确的是
A.实验1可知0.1  溶液中存在: 溶液中存在: |
B.实验2得到的溶液中存在: |
C.实验3中随着水不断加入,溶液中 的值逐渐变小 的值逐渐变小 |
D.实验4中发生反应的离子方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
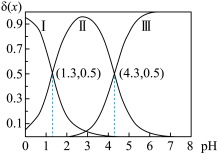
【推荐1】草酸 是二元弱酸。向
是二元弱酸。向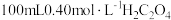 溶液中加入
溶液中加入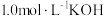 溶液调节
溶液调节 ,加水控制溶液体积为
,加水控制溶液体积为 。测得溶液中微粒的
。测得溶液中微粒的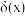 随
随 变化如图所示,其中
变化如图所示,其中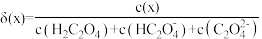 ,x代表微粒
,x代表微粒 或
或 。常温时,下列叙述正确的是
。常温时,下列叙述正确的是
 是二元弱酸。向
是二元弱酸。向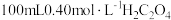 溶液中加入
溶液中加入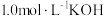 溶液调节
溶液调节 ,加水控制溶液体积为
,加水控制溶液体积为 。测得溶液中微粒的
。测得溶液中微粒的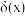 随
随 变化如图所示,其中
变化如图所示,其中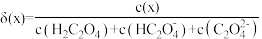 ,x代表微粒
,x代表微粒 或
或 。常温时,下列叙述正确的是
。常温时,下列叙述正确的是
A.曲线Ⅱ是 的变化曲线 的变化曲线 |
B.曲线I随 增大, 增大, 的电离程度减小 的电离程度减小 |
C.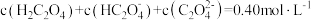 |
D. 时, 时,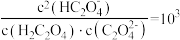 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关化学实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向两个装满水的大小相等的表面皿中,分别加入绿豆小金属钠和黄豆大金属钾 | 大金属钾游动更加剧烈 | 金属钾比钠活泼 |
| B | 向氨水和Mg(OH)2的悬浊液中滴加少量FeCl3溶液 | 得到红褐色悬浊液 | Ksp:Fe(OH)3<Mg(OH)2 |
| C | 使石蜡油蒸汽通过炽热的碎瓷片,再将产生的气体通过酸性KMnO4溶液 | KMnO4溶液褪色 | 石蜡油蒸汽中含有烯烃 |
| D | 常温下,向等浓度、等体积的Na2CO3和NaHCO3溶液中滴加等量的酚酞试液 | Na2CO3溶液中红色更深 | Kh:CO32->HCO3- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


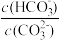 增大
增大 溶液性质。
溶液性质。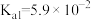 ,
,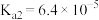
 溶液中滴加
溶液中滴加