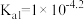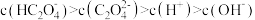乙二胺( ,简写为X)为二元弱碱。25℃时,向
,简写为X)为二元弱碱。25℃时,向 其盐酸盐溶液
其盐酸盐溶液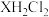 中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中
中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中 、
、 、X三种粒子浓度的对数值(
、X三种粒子浓度的对数值( )与
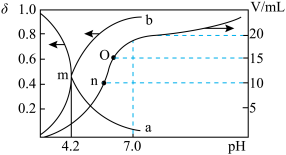
)与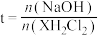 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 ,简写为X)为二元弱碱。25℃时,向
,简写为X)为二元弱碱。25℃时,向 其盐酸盐溶液
其盐酸盐溶液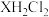 中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中
中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中 、
、 、X三种粒子浓度的对数值(
、X三种粒子浓度的对数值( )与
)与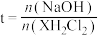 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是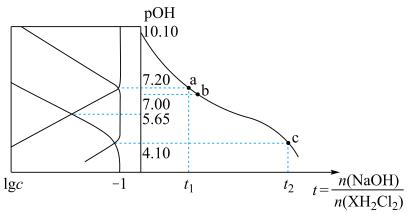
A.乙二胺第一、二步电离常数的数量级分别为 、 、 |
B.当 时, 时, |
C.b点时,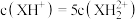 |
D.c点时,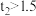 |
2024·全国·二模 查看更多[2]
更新时间:2024-04-30 23:44:26
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】常温下有H2RO4=H++HRO4-、HRO4- H++RO42-,现有物质的量浓度都为0.1mol/L的三种溶液:①NaHRO4溶液; ②H2RO4溶液; ③Na2RO4溶液。下列说法正确的是
H++RO42-,现有物质的量浓度都为0.1mol/L的三种溶液:①NaHRO4溶液; ②H2RO4溶液; ③Na2RO4溶液。下列说法正确的是
 H++RO42-,现有物质的量浓度都为0.1mol/L的三种溶液:①NaHRO4溶液; ②H2RO4溶液; ③Na2RO4溶液。下列说法正确的是
H++RO42-,现有物质的量浓度都为0.1mol/L的三种溶液:①NaHRO4溶液; ②H2RO4溶液; ③Na2RO4溶液。下列说法正确的是| A.②和③等体积混合后的溶液中: c( Na+)= c( HRO4-)+c(H2RO4) +c(RO42-) |
| B.100mL①溶液中: n(HRO4-)+n(RO42-)+n(OH-)-n(H+)= 0.01 |
| C.①和②等体积混合后的溶液中可能的离子浓度为c( HRO4-)>c(H+)>c(Na+) |
| D.若①和③等体积混合后,会抑制水的电离,则HRO4-的电离程度肯定大于RO42-的水解程度 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】向 溶液中滴加
溶液中滴加 溶液,
溶液, 的百分含量
的百分含量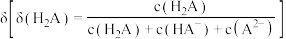 随溶液
随溶液 的变化如图所示:
的变化如图所示:
 溶液中滴加
溶液中滴加 溶液,
溶液, 的百分含量
的百分含量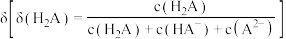 随溶液
随溶液 的变化如图所示:
的变化如图所示:
A. 的数量级为 的数量级为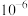 | B.a点对应的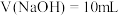 |
C.b点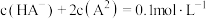 | D.c点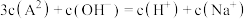 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】25℃时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.2mol·L-1的NaOH溶液,所得溶液pH与NaOH溶液体积的关系如图所示。下列说法错误的是
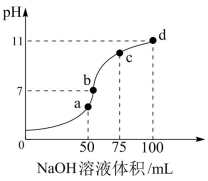

| A.25℃时,K(NH3·H2O)约为2×10-5 |
| B.溶液的导电能力:a>b |
C.c点对应溶液中:c(NH )<c(NH3·H2O) )<c(NH3·H2O) |
| D.水的电离程度:c>d |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25℃时,在浓度都为1 mol·L-1的(NH4)2SO4、NH4H CO3、NH4HSO4、NH4Cl的四种溶液中,测得c(NH4+)分别为a、b、c、d(单位为mol·L-1)。下列判断正确的是
| A.a=2b=2c=2d | B.a>b>c> d | C.a>c>d>b | D.a>c>b>d |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】室温下,将0.lmol/L'的NaOH 溶液分别滴入体积均为0.01L、物成的量浓度均为cmol/L的盐酸和醋酸中,溶液pH 随加入NaOH 溶液体积变化的曲线如图所示。下列有关说法正确的是
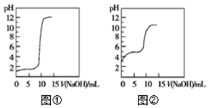

| A.滴定前 c(CH3COOH)=0.001mol/L |
| B.图①中V(NaOH)=10mL时,溶液中由水电离出的c(H+)=1.0×10-14mol/L |
| C.图②中V(NaOH)=5 mL 时,溶液中2c(Na+)=c(CH3COO-)+c(CH3COOH) |
| D.图②中V(NaOH)=10 mL 时,溶液中c(CH3COO-)> c(Na+)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】现有常温下的四种溶液(如下表):
下列有关叙述中正确的是
① | ② | ③ | ④ | |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
pH =11 | pH =11 | C=0.002mol/L | C=0.002mol/L |
| A.分别加水稀释10倍,四种溶液的pH:①>②>④>③ |
| B.在④、②两种溶液等体积混合,所得溶液pH=3 |
| C.四种溶液由水电离出氢离子的浓度从大到小的顺序是③>①>②>④ |
| D.将①、④两种溶液等体积混合,溶液中c(OH-) >c(H+ ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】化学上常用AG表示溶液中的 。25°C时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
。25°C时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
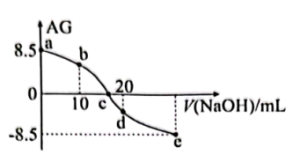
 。25°C时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
。25°C时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
A.随着NaOH溶液的加入, 减小 减小 |
| B.25°C时,HNO2的电离常数Ka的数量级为10-6 |
C.b点溶液中存在:2c(H+)-2c(OH-)=c( )-c(HNO2) )-c(HNO2) |
| D.a、b、c、d、e五点的溶液中,水的电离程度最大的点是d |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下将NaOH溶液滴加到 和HB的混合溶液中,溶液中
和HB的混合溶液中,溶液中 、
、 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ,
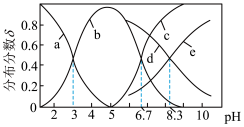
,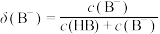 ]随pH变化的关系如图所示。下列说法正确的是
]随pH变化的关系如图所示。下列说法正确的是
 和HB的混合溶液中,溶液中
和HB的混合溶液中,溶液中 、
、 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ,
,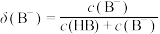 ]随pH变化的关系如图所示。下列说法正确的是
]随pH变化的关系如图所示。下列说法正确的是
A.曲线b、d分别表示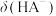 、 、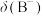 随pH变化的关系 随pH变化的关系 |
B.NaB的水解常数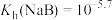 ,NaHA溶液中 ,NaHA溶液中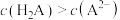 |
C.NaHA溶液与NaB溶液混合过程中发生反应的离子方程式为 |
D.当溶液呈中性时,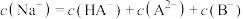 |
您最近一年使用:0次

 ]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是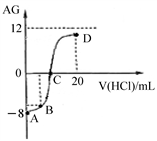
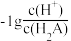 和-1gc(HA-)或
和-1gc(HA-)或 和
和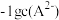 关系如图所示,下列说法正确的是
关系如图所示,下列说法正确的是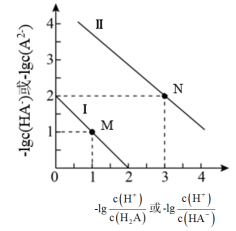






 为二元弱酸,常温下将
为二元弱酸,常温下将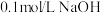 溶液滴入
溶液滴入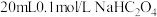 溶液中,测得溶液中
溶液中,测得溶液中 (或
(或 )的分布系数(
)的分布系数( )、滴入
)、滴入 溶液体积(V)分别与
溶液体积(V)分别与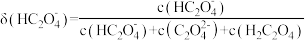 ]。
]。