(1)甘油
 、水蒸气、氧气自热式催化重整制氢时无需加热,主要反应如下:
、水蒸气、氧气自热式催化重整制氢时无需加热,主要反应如下:反应I:
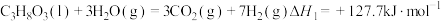
反应Ⅱ:
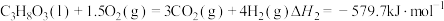
①

②除
 外,可能还会产生
外,可能还会产生 等副产物,为了提高原子利用率,最需要抑制
等副产物,为了提高原子利用率,最需要抑制 的生成,原因是
的生成,原因是(2)“表面改性铝粉分解水制氢”因
 储量丰富和较强的还原活性得到广泛应用。铝粉表面的致密氧化膜是影响
储量丰富和较强的还原活性得到广泛应用。铝粉表面的致密氧化膜是影响 还原活性的主要因素,工业上常用
还原活性的主要因素,工业上常用 溶液或锡酸钠
溶液或锡酸钠 溶液作为
溶液作为 粉的改性试剂。已知:
粉的改性试剂。已知: 。
。①利用
 溶液改性
溶液改性 粉的原理可用化学方程式表示为
粉的原理可用化学方程式表示为②
 下,向两份质量和粒径均相同的
下,向两份质量和粒径均相同的 粉中,分别加入等体积
粉中,分别加入等体积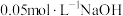 溶液和
溶液和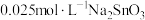 溶液来改性
溶液来改性 粉,氢气产率随时间的变化关系如图1所示。
粉,氢气产率随时间的变化关系如图1所示。 溶液改性效果明显优于
溶液改性效果明显优于 溶液的可能原因是
溶液的可能原因是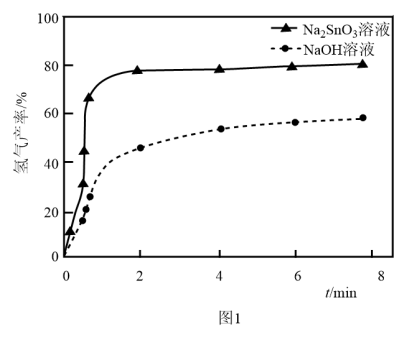
 溶液浓度的变化关系如图2所示。当
溶液浓度的变化关系如图2所示。当 溶液浓度为
溶液浓度为 时,氢气产率接近
时,氢气产率接近 。但
。但 溶液过大或过小会大大降低氢气产率,其可能原因分别是
溶液过大或过小会大大降低氢气产率,其可能原因分别是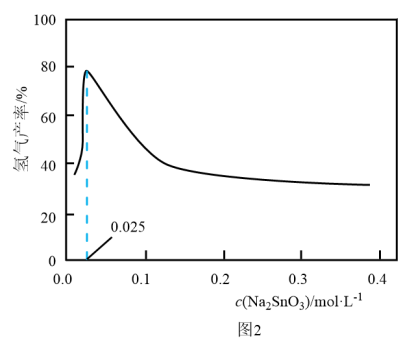
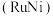 催化氨硼烷水解制氢”主要经过吸附和还原的过程,其反应机理如图所示(每个步骤只画出了可能参与该步反应的1个水分子,氨硼烷中与
催化氨硼烷水解制氢”主要经过吸附和还原的过程,其反应机理如图所示(每个步骤只画出了可能参与该步反应的1个水分子,氨硼烷中与 原子相连的3个
原子相连的3个 原子分别用
原子分别用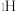 、
、 和
和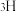 标记)。根据元素电负性的变化规律推测题图的虚线框内微粒
标记)。根据元素电负性的变化规律推测题图的虚线框内微粒 和
和 的化学式分别为
的化学式分别为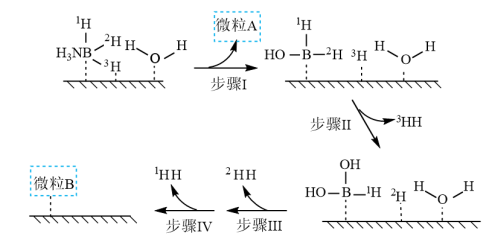
相似题推荐
(1)C的电子式
(2)A的化学式
(3)反应③的化学方程式
(4)反应④的离子方程式
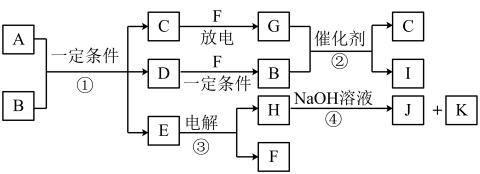
(1)铝灰用“水洗”的目的是:
(2)“过滤1”所得滤渣主要成分为:
(3)用下图装置制备CO2时,适宜的药品A为:
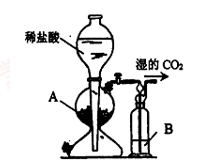
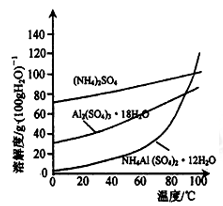
(4)请设计从“过滤2”所得滤渣制取铵明矾的实验方案:称取一定质量“过滤2”的滤渣,放入烧杯中,
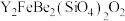 ],工业上通过如下生产流程可获得氧化钇。
],工业上通过如下生产流程可获得氧化钇。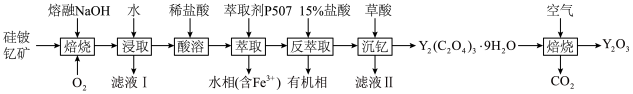
已知:
 元素与
元素与 元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;(1)在自然界中,钇只有一种稳定同位素
 ,Y位于元素周期表的第
,Y位于元素周期表的第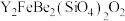 ]中Y的化合价为+3价,
]中Y的化合价为+3价, 的化合价为
的化合价为(2)焙烧的目的是将矿石中的Y元素转化为
 ,并将
,并将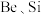 元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是(3)“萃取分液”实验需要的玻璃仪器有
(4)滤液Ⅱ中的
(5)反应过程中,测得Y的沉淀率随
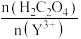 的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是
的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是
(6)“焙烧”过程生成
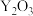 的化学方程式为
的化学方程式为 )是重要的化工原料,也是一种清洁的能源,可用
)是重要的化工原料,也是一种清洁的能源,可用 和
和 制得,由合成气制备二甲醚的主要原理如下:
制得,由合成气制备二甲醚的主要原理如下:①

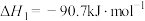

②

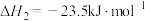

③

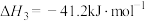

(1)反应
 的
的
 ;该反应的平衡常数
;该反应的平衡常数
 、
、 、
、 表示)。
表示)。(2)下列措施中,能提高①中
 产率的有_______。
产率的有_______。A.使用过量的 | B.升高温度 | C.增大压强 | D.使用催化剂 |
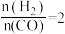 通入
通入 的反应器中,一定条件下发生反应:
的反应器中,一定条件下发生反应:
 ,其中
,其中 的平衡转化率随温度、压强的变化关系如图所示,下列说法正确的是
的平衡转化率随温度、压强的变化关系如图所示,下列说法正确的是
A.

B.
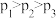
C. 若在
 和316℃时,起始时
和316℃时,起始时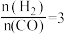 ,则平衡时,
,则平衡时,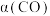 小于50%
小于50%(4)采用一种新型的催化剂(主要成分是
 的合金),利用
的合金),利用 和
和 制备二甲醚(DME)。观察图,当
制备二甲醚(DME)。观察图,当 约为
约为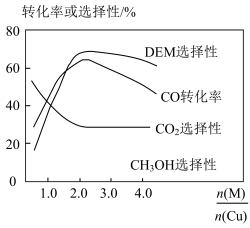
(5)下图为绿色电源“二甲醚燃料电池”的工作原理示意图,a极生成的气体是

(6)甲醇液相脱水法制二甲醚的原理是:
 ,
, 。与合成气制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是
。与合成气制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是 、
、 、
、 等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的
等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的 和
和 。
。(1)
 和
和 在Cu/ZnO催化下发生反应可合成清洁能源甲醇:
在Cu/ZnO催化下发生反应可合成清洁能源甲醇: ,该反应实际上分两步进行。
,该反应实际上分两步进行。断开(或形成)1mol化学键的能量变化数据如下表所示,利用下表中的数据可知,该反应每生成1mol甲醇,需要
| 化学键 | H-H | C-O | C=O | O-H | C-H |
 | 436 | 326 | 803 | 464 | 414 |
(2)可利用
 热分解制备
热分解制备 ,已知下列反应的热化学方程式:
,已知下列反应的热化学方程式:①

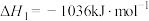
②

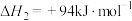
③

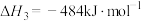
计算
 热分解反应④
热分解反应④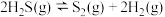

 。
。(3)
 重整技术是实现“碳中和”的一种理想的
重整技术是实现“碳中和”的一种理想的 利用技术,反应为:
利用技术,反应为: 。在pMPa时,将
。在pMPa时,将 和
和 按物质的量之为1:1:充入密闭容器中,分别在无催化剂及
按物质的量之为1:1:充入密闭容器中,分别在无催化剂及 催化下反应相同时间,测得
催化下反应相同时间,测得 的转化率与温度的关系如图所示:
的转化率与温度的关系如图所示:在pMPa、900℃、
 催化条件下,将
催化条件下,将 、
、 、
、 按物质的量之比为
按物质的量之比为 充入密闭容器,
充入密闭容器, 的平衡转化率为
的平衡转化率为 ,此时平衡常数
,此时平衡常数
 、
、 、
、 的计算表达式)。
的计算表达式)。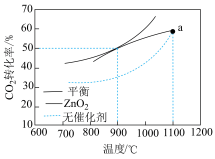
Ⅱ.回收利用工业废气中的
 和
和 ,实验原理示意图如下。
,实验原理示意图如下。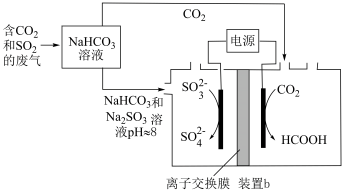
(4)①装置b中
 参与反应的电极为
参与反应的电极为②反应后装置b中溶液pH变化
③装置b中的总反应的离子方程式为
(1)重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下;
①BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=+571.2 kJ·mol-1
②BaS(s)=Ba(s)+S(s)ΔH=+460 kJ·mol-1
已知:③2C(s)+O2(g)=2CO(g)ΔH=-221kJ·mol-1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH =
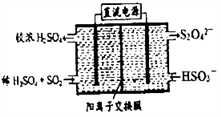
(2)利用下图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。
①阳极的电极反应式为
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成。该反应中氧化剂与还原剂的物质的量之比为
Ⅱ.乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产。哈斯特研究得出当甲烷分解时,几种气体平衡时分压(Pa)与温度(℃)的关系如图所示。
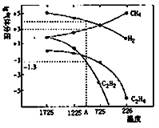
(3)T2℃时,向1L恒容密闭容器中充入0.3molCH4只发生反应2CH4(g)
 C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH
C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH(4)计算反应2CH4(g) =C2H2(g)+3H2(g)在图中A点温度时的平衡常数K=
 ≈-1.3)
≈-1.3)
资料:i.草酸(H2C2O4)为二元弱酸。
ii.三水三草酸合铁酸钾K3 Fe(C2O4)3·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:
[Fe(C2O4)3]3-
 Fe3++3C2O42- K=6.3×10-21
Fe3++3C2O42- K=6.3×10-21iii. FeC2O4·2H2O为黄色固体,微溶于水,可溶于强酸。
[实验1]通过Fe3+和C2O42-在溶液中的反应比较Fe2+和C2O42-的还原性强弱。
| 操作 | 现象 |
| 在避光处,向10 mL 0.5 mol·L-1 FeCl3溶液中缓慢加入0.5 mol·L-1 K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤 | 得到翠绿色溶液和翠绿色晶体 |
(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是
(3)经检验,翠绿色晶体为K3 Fe(C2O4)3·3H2O设计实验,确认实验1中没有发生氧化还原反应的操作和现象是
(4)取实验1中的翠绿色溶液光照一段时间,产生黄色浑浊且有气泡产生。补全反应的离子方程式:
[实验2]通过比较H2O2与Fe2+、C2O42-反应的难易,判断二者还原性的强弱。
| 步骤 | 操作 | 现象 |
| I | 向l mL 0.5 mol·L-1 FeSO4溶液中加入1 mL 0.5 mol·L-1 K2C2O4溶液,过滤 | 立即产生黄色沉淀 |
| II | 洗涤Ⅰ中的黄色沉淀,向其中加入过量的6%H2O2溶液,振荡,静置 | 剧烈放热,产生大量的红褐色沉淀和无色气体 |
| III | 待充分反应后,向其中加入稀硫酸,调节pH约为4 | 得到翠绿色溶液 |
(6)以上现象能否说明C2O42-没有被氧化。请判断并说明理由:
(7)用FeC13溶液、K2C2O4溶液和其他试剂,设计实验方案比较Fe2+和C2O42-的还原性强弱。画出装置图并描述预期现象:
已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
金属离子 | Fe3+ | Fe2+ | In3+ |
开始沉淀pH(离子浓度为0.1mol·L-1时) | 1.3 | 6 | 3 |
完全沉淀pH | 2.7 | 8 | 4.3 |
(1)In2O3中In的化合价是
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为
 ,该反应的离子方程式为
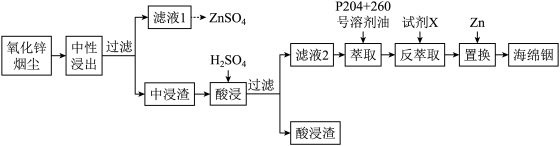
,该反应的离子方程式为③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为
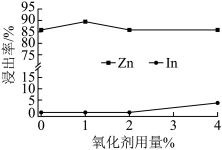
④“中浸渣”的主要成分为In(OH)3、
(3)萃取时,发生反应In3+ +3H2A2
 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。①反萃取时,宜选用的试剂X为
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有
(4)“置换”后的滤液可返回
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉
【推荐3】氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理和化学平衡对于消除环境污染有重要意义。
(1)NO在空气中存在如下反应:2NO(g)+O2(g) 2NO2(g)ΔH。上述反应分两步完成,其反应历程如图所示。
2NO2(g)ΔH。上述反应分两步完成,其反应历程如图所示。

请回答下列问题:
①写出反应II的热化学方程式
②反应I和反应II中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g) 2NO2(g)反应速率的是
2NO2(g)反应速率的是
(2)用活性炭还原法处理氮氧化物的有关反应为:C(s)+2NO(g) N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及12min和15min时各物质的平衡浓度如表所示:
N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及12min和15min时各物质的平衡浓度如表所示:
浓度(mol·L-1) 时间(min) | NO | CO2 | N2 |
0 | 0.200 | 0 | 0 |
12 | 0.050 | 0.075 | 0.075 |
15 | 0.100 | 0.050 | 0.450 |
①T℃时,该反应的平衡常数为
②在12min时,若只改变某一条件使平衡发生移动,15min时重新达到平衡,则改变的条件是
③在15min时,保持温度和容器体积不变再充入NO和N2,使NO、N2的浓度分别增加至原来的2倍4倍,此时反应v正
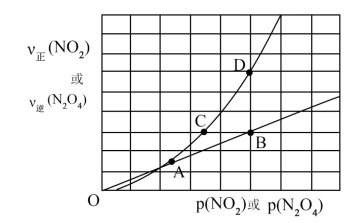
(3)NO2存在如下平衡:2NO2(g) N2O4(g)△H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系式:v正(NO2)=k1·P2(NO2),v逆(N2O4)=k2·P(N2O4),速率与分压关系如图所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是Kp=
N2O4(g)△H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系式:v正(NO2)=k1·P2(NO2),v逆(N2O4)=k2·P(N2O4),速率与分压关系如图所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是Kp=
(1)第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为
(2)铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有
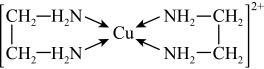
(3)CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
①H、N、O三种元素的电负性由大到小的顺序是
②SO2分子的空间构型为
③乙二胺分子中氮原子轨道的杂化类型为
④中所形成的配离子中含有的化学键类型有
A.配位键 B.极性键 C.离子键 D.非极性键
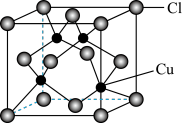
⑤CuCl的晶胞结构如图所示,其中Cl原子的配位数为

(1)卟吩中N原子采用的轨道杂化方式是
(2)下列有关叶绿素分子的说法正确的是_________(填选项序号)。
| A.图中1—5号C中有三个具有手性 |
| B.分子中存在配位键 |
| C.图中1、2、3、4号C共面 |
| D.N的第一电离能大于O |
(4)氰化氢(HCN)是一种含氮剧毒化合物,其分子中
 键与
键与 键的个数比为
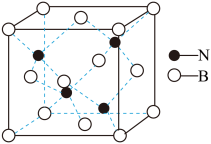
键的个数比为(5)N与B能够形成一种硬度接近金刚石的物质,其晶体结构如图,若其晶胞边长为a pm,则其密度为
(1)基态镍原子的价电子排布图为
(2)四羰基合镍是一种无色挥发性液体,熔点-25℃,沸点43℃。则四羟基合镍中σ键和π键数目之比为
(3)[Ni(NH3)
4]SO4中N原子的杂化方式为
NH3)4]SO4中H-N-H键之间的夹角
(4)已知NiO的晶体结构(如图1),可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中,则NiO晶体中原子填充在氧原子形成的
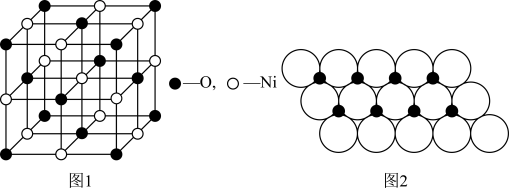
(5)一定温度下,NiO晶体可分散形成“单分子层”,O2-作单层密置排列,Ni2+填充O2-形成的正三角形空隙中(如图2),已知O2-的半径为αm,每平方米面积上分数的NiO的质量为



