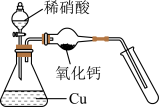
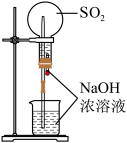
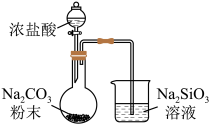
根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确的是
实验目的 | 方案设计 | 现象 | 结论 | |
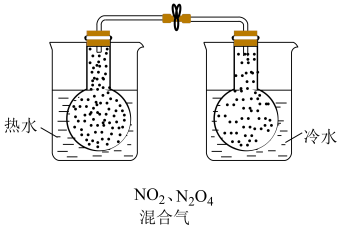
A | 探究温度对 化学平衡的影响 化学平衡的影响 |
| ①浸泡在热水中的烧瓶内红棕色加深 ②浸泡在冷水中的烧瓶内红棕色变浅 | ①升高温度, 的浓度增大,平衡逆向移动; 的浓度增大,平衡逆向移动;②降低温度,  的浓度减小,平衡正向移动 的浓度减小,平衡正向移动 |
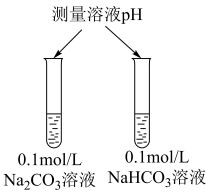
B | 验证 的水解程度比 的水解程度比 大 大 |
|  溶液 溶液 大于 大于 溶液 溶液 |  的水解程度比 的水解程度比 大 大 |
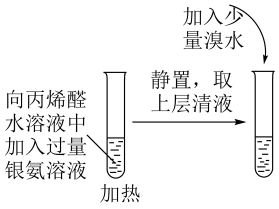
C | 检验 有碳碳双键 有碳碳双键 |
| 溴水褪色 |  有碳碳双键 有碳碳双键 |
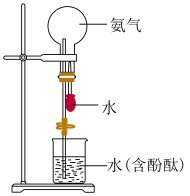
D | 探究 的性质 的性质 |
| 圆底烧瓶中形成喷泉,溶液显红色 | 氨气极易溶于水,氨水显碱性 |
| A.A | B.B | C.C | D.D |
更新时间:2024-04-18 11:16:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示的装置中,烧瓶中充满干燥的气体a,将滴管内的液体b挤入烧瓶内,打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
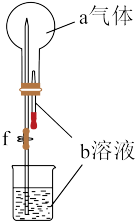

| a(干燥气体) | b(溶液) | |
| A | NO2 | 水 |
| B | SO2 | NaOH溶液 |
| C | NH3 | CCl4 |
| D | Cl2 | 饱和NaCl溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】同温同压下,两个等体积的干燥圆底烧瓶中分别充满:①NH3,②NO2,进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度为


| A.①=②=③=④ | B.①>②>③>④ |
| C.①=②>③>④ | D.①=②>③=④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用下列装置进行实验,能达到相应实验目的的是
|
|
|
|
| A.制取并收集纯净的NO | B.完成喷泉实验 | C.比较酸性强弱: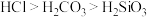 | D.实验室制备 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知: 。向一恒温恒容的密闭容器中充入1molA和3molB发生反应,t1时达到平衡状态Ⅰ。在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
。向一恒温恒容的密闭容器中充入1molA和3molB发生反应,t1时达到平衡状态Ⅰ。在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
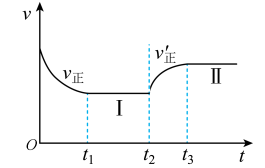
 。向一恒温恒容的密闭容器中充入1molA和3molB发生反应,t1时达到平衡状态Ⅰ。在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
。向一恒温恒容的密闭容器中充入1molA和3molB发生反应,t1时达到平衡状态Ⅰ。在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
| A.t2时改变的条件可能是升温 |
| B.平衡常数K:K(Ⅱ)>K(Ⅰ) |
| C.t2~t3时反应向正反应方向移动 |
| D.平衡时A的体积分数φ:φ(Ⅱ)>φ(Ⅰ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】乙酸甲酯的催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式:CH3COOCH3(l)+C6H13OH(l) CH3COOC6H13(l)+CH3OH(l),已知
CH3COOC6H13(l)+CH3OH(l),已知 正=k正·x(CH3COOCH3)·x(C6H13OH),
正=k正·x(CH3COOCH3)·x(C6H13OH), 逆=k逆·x(CH3COOC6H13)·x(CH3OH),其中k正、k逆为速率常数(受温度影响) ,x为各组分的物质的量分数。反应开始时,CH3COOCH3和C6H13OH按物质的量之比1∶1投料,测得338 K、343 K、348 K三个温度下CH3COOCH3转化率(α)随时间(t)的变化关系如图所示。下列说法正确的是
逆=k逆·x(CH3COOC6H13)·x(CH3OH),其中k正、k逆为速率常数(受温度影响) ,x为各组分的物质的量分数。反应开始时,CH3COOCH3和C6H13OH按物质的量之比1∶1投料,测得338 K、343 K、348 K三个温度下CH3COOCH3转化率(α)随时间(t)的变化关系如图所示。下列说法正确的是

 CH3COOC6H13(l)+CH3OH(l),已知
CH3COOC6H13(l)+CH3OH(l),已知 正=k正·x(CH3COOCH3)·x(C6H13OH),
正=k正·x(CH3COOCH3)·x(C6H13OH), 逆=k逆·x(CH3COOC6H13)·x(CH3OH),其中k正、k逆为速率常数(受温度影响) ,x为各组分的物质的量分数。反应开始时,CH3COOCH3和C6H13OH按物质的量之比1∶1投料,测得338 K、343 K、348 K三个温度下CH3COOCH3转化率(α)随时间(t)的变化关系如图所示。下列说法正确的是
逆=k逆·x(CH3COOC6H13)·x(CH3OH),其中k正、k逆为速率常数(受温度影响) ,x为各组分的物质的量分数。反应开始时,CH3COOCH3和C6H13OH按物质的量之比1∶1投料,测得338 K、343 K、348 K三个温度下CH3COOCH3转化率(α)随时间(t)的变化关系如图所示。下列说法正确的是
| A.该反应的ΔH<0 |
| B.348 K时,该反应的平衡常数为1.8 |
C.A、B、C、D四点中, 正最大的是D 正最大的是D |
D.在曲线①、②、③中, 最大的曲线是① 最大的曲线是① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 相同温度下,同时向 ①4 mL 0.1 mol▪L-1 KMnO4酸性溶液和②4 mL 0.2 mol▪L-1 KMnO4酸性溶液中,分别加入4 mL 1 mol▪L-1 H2C2O4溶液 | ①中溶液先褪色 | 该实验条件下,KMnO4浓度越小,反应速率越快 |
| B | 向煤炉中灼热的煤炭上洒少量水 | 产生淡蓝色火焰,煤炭燃烧更旺 | 加少量水后,可使煤炭燃烧放出更多的热量 |
| C | 加热2NO2(g)  N2O4(g)平衡体系 N2O4(g)平衡体系 | 颜色加深 | 证明正反应是放热反应 |
| D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH | 后者较大 | 证明非金属性 S>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】设 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是
 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是A.向1L0.1  溶液中滴加 溶液中滴加 溶液至中性,所得溶液中 溶液至中性,所得溶液中 的数目小于0.1 的数目小于0.1 |
B.10g质量分数为92%的乙醇溶液与足量金属钠充分反应,产生 的分子数为0.1 的分子数为0.1 |
C.常温常压下,46g 中的分子数目小于 中的分子数目小于 |
D.1  晶体所含离子总数为2 晶体所含离子总数为2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】弱电解质的电离平衡、盐类的水解平衡都是重要的化学平衡。已知H2A在水中存在以下电离:H2A=H++HA-,HA- H++A2-。下列说法正确的是
H++A2-。下列说法正确的是
 H++A2-。下列说法正确的是
H++A2-。下列说法正确的是| A.0.01mol·L-1H2A溶液的pH等于2 |
| B.在NaHA溶液显酸性,溶液中所有微粒浓度大小:c(Na+)>c(HA- )>c(H+)>c(A2-)>c(H2A)>c(OH-) |
| C.Na2A溶液中部分微粒浓度大小:c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) |
| D.NaHA溶液中水的电离度大于等浓度Na2A溶液中水的电离度 |
您最近一年使用:0次
【推荐3】下列离子组中加(或通)入相应试剂后,判断和分析均正确的是
| 选项 | 离子组 | 加(或通)入试剂 | 判断和分析 |
| A | Na+、K+、 、Cl- 、Cl- | 足量NaHCO3溶液 | 不能大量共存,因 和 和 之间会发生完全双水解生成CO2气体和Al(OH)3沉淀 之间会发生完全双水解生成CO2气体和Al(OH)3沉淀 |
| B | Na+、Mg2+、 、 、 | 足量NaOH溶液 | 不能大量共存,会发生下列反应 |
| C |  、Ca2+、Cl-、 、Ca2+、Cl-、 | 足量CO2 | 能大量共存,粒子间不反应 |
| D | Na+、K+、ClO-、Cl- | 少量SO2 | 不能大量共存,会发生下列氧化还原反应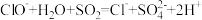 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法不正确的是
A.激素类药物乙烯雌酚的结构简式为: ,它的分子式是:C18H20O2 ,它的分子式是:C18H20O2 |
| B.等质量的甲烷、乙烯、乙醇分别充分燃烧,所耗用氧气的量依次减少 |
C.聚乳酸( )是由单体之间通过加聚反应合成的 )是由单体之间通过加聚反应合成的 |
D.实验证实 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】关于化合物2一呋喃甲醛(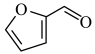 )下列说法不正确的是
)下列说法不正确的是
 )下列说法不正确的是
)下列说法不正确的是| A.能使酸性高锰酸钾溶液褪色 | B.含有三种官能团 |
| C.分子式为C5H4O2 | D.所有原子一定不共平面 |
您最近一年使用:0次