重铬酸钾是一种重要的化工原料,工业上以某含铬矿(主要成分为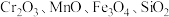 等)为主要原料制备重铬酸钾的工艺流程如图所示:
等)为主要原料制备重铬酸钾的工艺流程如图所示: 的条件下,
的条件下, (III)不能被氧化,高锰酸钾的还原产物是
(III)不能被氧化,高锰酸钾的还原产物是 。
。
回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有_______ (任写两条)。
(2)浸渣的主要成分为_______ (填化学式);“除铁、除锰”时沉锰的离子方程式为_______ 。
(3)“焙烧”时发生反应的化学方程式为_______ 。
(4)调 ”的目的是为了完成
”的目的是为了完成 和
和 的转换,涉及反应:
的转换,涉及反应: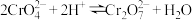 ;常温下,某
;常温下,某 溶液中含铬元素
溶液中含铬元素 ,调节溶液的
,调节溶液的 后两种离子的变化曲线如图所示,
后两种离子的变化曲线如图所示,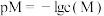 ,其中
,其中 可表示
可表示 或
或 ,图中表示
,图中表示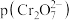 随
随 变化的曲线为
变化的曲线为_______ (填“X”或“Y”);其中反应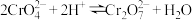 的平衡常数
的平衡常数
_______ 。 ”,在完成转换的同时制备
”,在完成转换的同时制备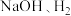 和
和 (装置如图所示):
(装置如图所示):_______ (填化学式),离子交换膜为_______ (填“阴离子”“质子”或“阳离子”)交换膜。
(6)“交换”过程中有关物质的溶解度如图所示,有同学认为结晶过滤的温度应是 和
和 溶解度相差最大的时候,你认为这个观点是否正确并说明理由:
溶解度相差最大的时候,你认为这个观点是否正确并说明理由:_______ 。
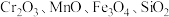 等)为主要原料制备重铬酸钾的工艺流程如图所示:
等)为主要原料制备重铬酸钾的工艺流程如图所示: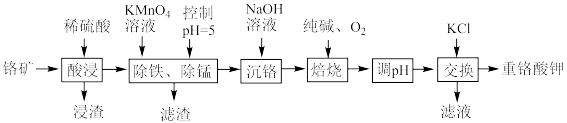
 的条件下,
的条件下, (III)不能被氧化,高锰酸钾的还原产物是
(III)不能被氧化,高锰酸钾的还原产物是 。
。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有
(2)浸渣的主要成分为
(3)“焙烧”时发生反应的化学方程式为
(4)调
 ”的目的是为了完成
”的目的是为了完成 和
和 的转换,涉及反应:
的转换,涉及反应: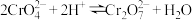 ;常温下,某
;常温下,某 溶液中含铬元素
溶液中含铬元素 ,调节溶液的
,调节溶液的 后两种离子的变化曲线如图所示,
后两种离子的变化曲线如图所示,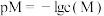 ,其中
,其中 可表示
可表示 或
或 ,图中表示
,图中表示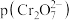 随
随 变化的曲线为
变化的曲线为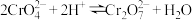 的平衡常数
的平衡常数

 ”,在完成转换的同时制备
”,在完成转换的同时制备 和
和 (装置如图所示):
(装置如图所示):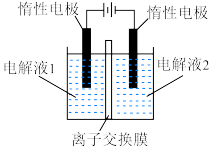
(6)“交换”过程中有关物质的溶解度如图所示,有同学认为结晶过滤的温度应是
 和
和 溶解度相差最大的时候,你认为这个观点是否正确并说明理由:
溶解度相差最大的时候,你认为这个观点是否正确并说明理由: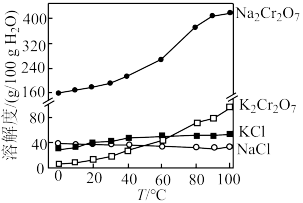
更新时间:2024-04-30 16:53:15
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩中10种元素用元素符号或化学式填空回答以下问题:
Ⅰ.填写下列空白:
(1)非金属性最强的元素是___________ (填元素符号),
(2)写出①与③形成原子个数比为1:1化合物的电子式:____________ ,该化合物酸性条件下与高锰酸钾反应的离子方程式:__________________________
(3)最高价氧化物对应的水化物中碱性最强的是_______ (填化学式),写出该物质与⑦的最高价氧化物对应的水化物反应的离子方程式为:____________ 。
(4)由①②③⑩四种元素中的三种组成的一种强酸,该强酸的稀溶液与铜反应的离子方程式____________________________
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂,X是一种氢化物,常温下为液体。则:
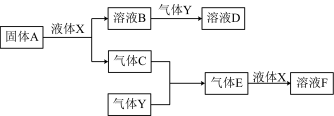
(1)A与液体X反应的化学方程式:____________________________ ;
(2)气体Y是一种大气污染物,无色、有刺激性气味的气体,直接排放会形成酸雨。写出气体Y与氯水反应的离子方程式:___________________________ ;
(3)在100 mL 18 mol/L的F浓溶液中加入过量铜片,加热使之充分反应,产生气体的体积为11.2 L(标况下),则反应过程中转移的电子数为__________ (用“NA”表示)
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(1)非金属性最强的元素是
(2)写出①与③形成原子个数比为1:1化合物的电子式:
(3)最高价氧化物对应的水化物中碱性最强的是
(4)由①②③⑩四种元素中的三种组成的一种强酸,该强酸的稀溶液与铜反应的离子方程式
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂,X是一种氢化物,常温下为液体。则:

(1)A与液体X反应的化学方程式:
(2)气体Y是一种大气污染物,无色、有刺激性气味的气体,直接排放会形成酸雨。写出气体Y与氯水反应的离子方程式:
(3)在100 mL 18 mol/L的F浓溶液中加入过量铜片,加热使之充分反应,产生气体的体积为11.2 L(标况下),则反应过程中转移的电子数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】高锰酸钾在化工生产和环境保护等领域应用十分广泛。以软锰矿(主要成分是MnO2,含有Fe2O3和SiO2等杂质)为原料制备高锰酸钾的工艺流程如图:
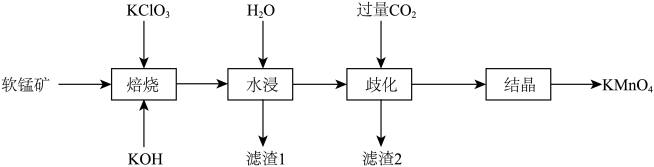
回答下列问题:
(1)基态Mn原子的价电子轨道表示式为______ 。
(2)“焙烧”中有K2MnO4生成,该步骤主要反应的化学方程式为_______ 。
(3)若“焙烧”时未加入KClO3,“水浸”后所得溶液中也含有K2MnO4,原因可能是______ 。
(4)“水浸”时需要加热,其目的是______ 。
(5)“滤渣2”含有MnO2和______ ,“歧化”过程中主要反应的离子方程式为_____ 。
(6)KMnO4可通过电解K2MnO4溶液的方法直接制得,相比“歧化法”,电解法的优点是______ 。

回答下列问题:
(1)基态Mn原子的价电子轨道表示式为
(2)“焙烧”中有K2MnO4生成,该步骤主要反应的化学方程式为
(3)若“焙烧”时未加入KClO3,“水浸”后所得溶液中也含有K2MnO4,原因可能是
(4)“水浸”时需要加热,其目的是
(5)“滤渣2”含有MnO2和
(6)KMnO4可通过电解K2MnO4溶液的方法直接制得,相比“歧化法”,电解法的优点是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某课外小组探究Cu(Ⅱ)盐与Na2S2O3溶液的反应。
【查阅资料】
ⅰ. 2 +Cu2+
+Cu2+ [Cu(S2O3)2]2-(绿色),2
[Cu(S2O3)2]2-(绿色),2 +Cu+
+Cu+ [Cu(S2O3)2]3-(无色):
[Cu(S2O3)2]3-(无色):
ⅱ. 2NH3+Cu+ [Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+ (蓝色);
[Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+ (蓝色);
ⅲ. 易被氧化为
易被氧化为 或
或 。
。
【猜想假设】
同学们根据资料认为Cu(Ⅱ)盐与Na2S2O3可能会发生两种反应:
假设1:Cu2+与 在溶液中发生配合反应生成[Cu(S2O3)2]2-;
在溶液中发生配合反应生成[Cu(S2O3)2]2-;
假设2:Cu(Ⅱ)有氧化性,Cu2+与 在溶液中发生氧化还原反应。
在溶液中发生氧化还原反应。
【实验操作及现象分析】
实验一:探究CuSO4与Na2S2O3溶液的反应。
(1)根据实验a的现象可推测溶液中生成的含Cu微粒是___________ (填化学式)。
(2)甲同学认为实验一可证明假设2成立,他的理由是___________ 。
实验二:探究CuCl2与Na2S2O3的反应。___________ (补全实验方案),则说明含Cu(Ⅰ)。
(4)经检验白色沉淀中含CuCl,请写出继续加Na2S2O3溶液后CuCl沉淀溶解的离子方程式:___________ 。
(5)经检验氧化产物以 形式存在,写出Cu2+与
形式存在,写出Cu2+与 发生氧化还原反应得到无色溶液的离子方程式:
发生氧化还原反应得到无色溶液的离子方程式:___________ 。
【获得结论】
(6)综合以上实验,同学们认为Cu(Ⅱ)盐与Na2S2O3在溶液中的反应与多种因素有关,得到实验结论,选择合适的选项填入下面的横线中。
A配合反应 B.氧化还原反应 C.置换反应 D.复分解反应
①随n( ):n(Cu2+)的增大,二者发生
):n(Cu2+)的增大,二者发生___________ 的趋势减弱;
②Cu(Ⅱ)盐的阴离子为Cl-时能增大Cu2+和 发生
发生___________ 的趋势。
【查阅资料】
ⅰ. 2
 +Cu2+
+Cu2+ [Cu(S2O3)2]2-(绿色),2
[Cu(S2O3)2]2-(绿色),2 +Cu+
+Cu+ [Cu(S2O3)2]3-(无色):
[Cu(S2O3)2]3-(无色):ⅱ. 2NH3+Cu+
 [Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+ (蓝色);
[Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+ (蓝色);ⅲ.
 易被氧化为
易被氧化为 或
或 。
。【猜想假设】
同学们根据资料认为Cu(Ⅱ)盐与Na2S2O3可能会发生两种反应:
假设1:Cu2+与
 在溶液中发生配合反应生成[Cu(S2O3)2]2-;
在溶液中发生配合反应生成[Cu(S2O3)2]2-;假设2:Cu(Ⅱ)有氧化性,Cu2+与
 在溶液中发生氧化还原反应。
在溶液中发生氧化还原反应。【实验操作及现象分析】
实验一:探究CuSO4与Na2S2O3溶液的反应。
| 实验操作 | 实验序号 | V1(mL) | V2(mL) | 逐滴加入Na2S2O3溶液时的实验现象 |
| a | 1.5 | 0.5 | 溶液逐渐变为绿色,静置无变化 |
| b | 1.0 | 1.0 | 溶液先变为绿色,后逐渐变成浅绿色,静置无变化 | |
| c | 0 | 2.0 | 溶液先变为绿色,后逐渐变浅至无色,静置无变化 |
(1)根据实验a的现象可推测溶液中生成的含Cu微粒是
(2)甲同学认为实验一可证明假设2成立,他的理由是
实验二:探究CuCl2与Na2S2O3的反应。
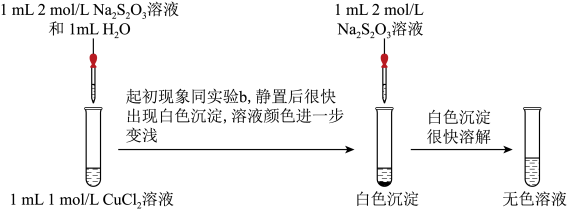
(4)经检验白色沉淀中含CuCl,请写出继续加Na2S2O3溶液后CuCl沉淀溶解的离子方程式:
(5)经检验氧化产物以
 形式存在,写出Cu2+与
形式存在,写出Cu2+与 发生氧化还原反应得到无色溶液的离子方程式:
发生氧化还原反应得到无色溶液的离子方程式:【获得结论】
(6)综合以上实验,同学们认为Cu(Ⅱ)盐与Na2S2O3在溶液中的反应与多种因素有关,得到实验结论,选择合适的选项填入下面的横线中。
A配合反应 B.氧化还原反应 C.置换反应 D.复分解反应
①随n(
 ):n(Cu2+)的增大,二者发生
):n(Cu2+)的增大,二者发生②Cu(Ⅱ)盐的阴离子为Cl-时能增大Cu2+和
 发生
发生
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】一碳化学是指以分子中只含一个碳原子的化合物为原料,用化工的方法制造产品的化学体系的名称。甲烷、一氧化碳是常见的一碳化学的原料。已知反应:
①
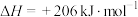
②
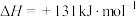
③
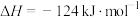
(1)工业制炭黑的方法之一是将甲烷隔绝空气加热到1300℃进行裂解。该反应的热化学方程式为_______ 。
(2)已知反应①中相关的化学键键能数据如下:
可知CO中C≡O键的键能为_______  。
。
(3)向恒容绝热的密闭容器中充入a mol 与2a mol
与2a mol  (g),进行反应①,下列能判断反应已达化学平衡状态的是
(g),进行反应①,下列能判断反应已达化学平衡状态的是_______ 。
a.容器中混合气体密度不变 b.混合气体中 与
与 之比不变
之比不变
c.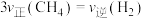 d.容器内温度不变
d.容器内温度不变
(4)反应②的正反应活化能为 ,则逆反应的活化能为
,则逆反应的活化能为_______  。对反应②的自发性进行判断并说明理由。
。对反应②的自发性进行判断并说明理由。_______
(5)向容积固定为1L的密闭容器内充入2mol CO和4mol ,保持250℃发生反应③,用压力计监测反应过程中容器内压强的变化如下表:
,保持250℃发生反应③,用压力计监测反应过程中容器内压强的变化如下表:
①从开始到20min时,以CO浓度变化表示的平均反应速率
_______ 。
②25℃时反应③平衡常数 的值为
的值为_______ 。
③在容器容积不变的前提下,欲提高反应③中 的平衡转化率,可采取的措施有
的平衡转化率,可采取的措施有_______ 、_______ (任写两项)。
①

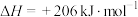
②

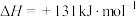
③

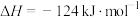
(1)工业制炭黑的方法之一是将甲烷隔绝空气加热到1300℃进行裂解。该反应的热化学方程式为
(2)已知反应①中相关的化学键键能数据如下:
| 化学键 | C-H | O-H | H-H |
键能/ | 413 | 465 | 436 |
 。
。(3)向恒容绝热的密闭容器中充入a mol
 与2a mol
与2a mol  (g),进行反应①,下列能判断反应已达化学平衡状态的是
(g),进行反应①,下列能判断反应已达化学平衡状态的是a.容器中混合气体密度不变 b.混合气体中
 与
与 之比不变
之比不变c.
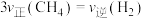 d.容器内温度不变
d.容器内温度不变(4)反应②的正反应活化能为
 ,则逆反应的活化能为
,则逆反应的活化能为 。对反应②的自发性进行判断并说明理由。
。对反应②的自发性进行判断并说明理由。(5)向容积固定为1L的密闭容器内充入2mol CO和4mol
 ,保持250℃发生反应③,用压力计监测反应过程中容器内压强的变化如下表:
,保持250℃发生反应③,用压力计监测反应过程中容器内压强的变化如下表:| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | p | 0.82p | 0.68p | 0.56p | 0.50p | 0.50p |

②25℃时反应③平衡常数
 的值为
的值为③在容器容积不变的前提下,欲提高反应③中
 的平衡转化率,可采取的措施有
的平衡转化率,可采取的措施有
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】“碳达峰”“碳中和”是推动我国经济社会高质量发展的内在要求。通过二氧化碳催化加氢制备甲醇是一种重要的转化方法,其反应过程的机理和相对能量如下(已知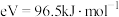 ,吸附在催化剂表面上的物种用*标注):
,吸附在催化剂表面上的物种用*标注):
反应I: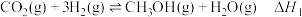
反应Ⅱ: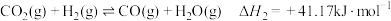
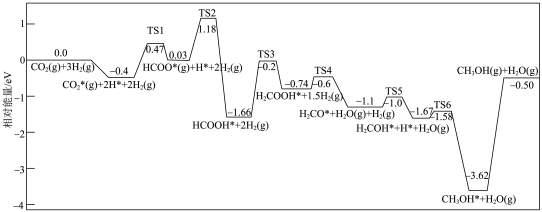
回答下列问题:
(1)该反应历程中决速反应的方程式为___________ 。
(2)反应Ⅱ的正反应活化能
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)反应 的
的
___________ 。
(4)一定条件下,起始投料为 不变,若只发生反应I.研究不同温度、压强下,平衡时甲醇的物质的量分数
不变,若只发生反应I.研究不同温度、压强下,平衡时甲醇的物质的量分数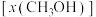 的变化规律,如图所示。其中,
的变化规律,如图所示。其中,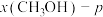 图在
图在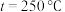 下测得,
下测得,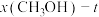 图在
图在 下测得。
下测得。
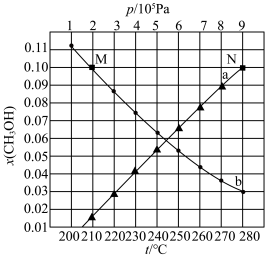
图中等温过程的曲线是___________ (填“a”或“b”)。平衡常数:
___________ 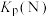 (填“>”“<”或“=”),其中
(填“>”“<”或“=”),其中
___________  (用分数表示)。
(用分数表示)。
(5)我国科学家研发的水系可逆 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:
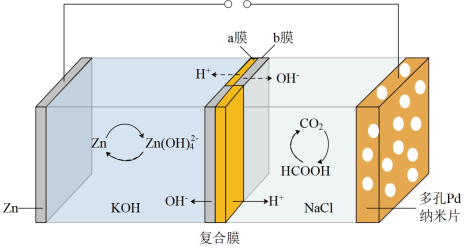
请写出放电时正极的电极反应式:___________ 。
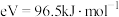 ,吸附在催化剂表面上的物种用*标注):
,吸附在催化剂表面上的物种用*标注):反应I:
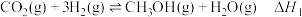
反应Ⅱ:
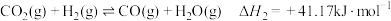

回答下列问题:
(1)该反应历程中决速反应的方程式为
(2)反应Ⅱ的正反应活化能

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)反应
 的
的
(4)一定条件下,起始投料为
 不变,若只发生反应I.研究不同温度、压强下,平衡时甲醇的物质的量分数
不变,若只发生反应I.研究不同温度、压强下,平衡时甲醇的物质的量分数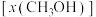 的变化规律,如图所示。其中,
的变化规律,如图所示。其中,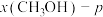 图在
图在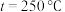 下测得,
下测得,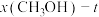 图在
图在 下测得。
下测得。
图中等温过程的曲线是

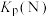 (填“>”“<”或“=”),其中
(填“>”“<”或“=”),其中
 (用分数表示)。
(用分数表示)。(5)我国科学家研发的水系可逆
 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:
请写出放电时正极的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】 是石油化工行业产生的污染性气体,工业上采取多种方式进行处理。
是石油化工行业产生的污染性气体,工业上采取多种方式进行处理。
Ⅰ.干法脱硫
(1)已知 的燃烧热
的燃烧热 (a>0),S的燃烧热
(a>0),S的燃烧热 (b>0),则常温下空气直接氧化脱除
(b>0),则常温下空气直接氧化脱除 的反应:
的反应: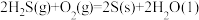

___________ kJ/mol。
(2)常用脱硫剂反应条件如下表,最佳脱硫剂为___________ 。
Ⅱ.热分解法脱硫
在密闭容器中,充入一定量的 气体,发生分解反应
气体,发生分解反应 ,控制不同的温度和压强,实验结果如图。
,控制不同的温度和压强,实验结果如图。
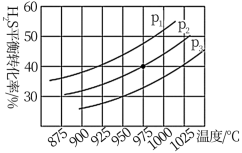
(3)图中压强P1、P2、P3由大到小的顺序为___________ ,该反应为___________ (填吸热”或“放热”)反应,若要进一步提高 的平衡转化率,可以采取的措施有
的平衡转化率,可以采取的措施有___________ (任写一种)。
(4)若压强为P2、温度为975℃, 的平衡常数
的平衡常数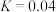 ,则起始
,则起始 的物质的量浓度c=
的物质的量浓度c=___________ mol/L,若向容器中再加入 气体,相同温度下再次达到平衡时,K
气体,相同温度下再次达到平衡时,K___________ 0.04(填“>”“<”或“=”)。
Ⅲ.间接电解法脱硫
通过 溶液吸收并氧化
溶液吸收并氧化 气体,再通过电解再生,实现循环使用,该法处理过程如图。
气体,再通过电解再生,实现循环使用,该法处理过程如图。
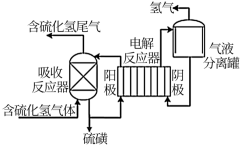
(5)电解反应器中总反应的离子方程式为___________ 。
 是石油化工行业产生的污染性气体,工业上采取多种方式进行处理。
是石油化工行业产生的污染性气体,工业上采取多种方式进行处理。Ⅰ.干法脱硫
(1)已知
 的燃烧热
的燃烧热 (a>0),S的燃烧热
(a>0),S的燃烧热 (b>0),则常温下空气直接氧化脱除
(b>0),则常温下空气直接氧化脱除 的反应:
的反应: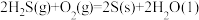

(2)常用脱硫剂反应条件如下表,最佳脱硫剂为
| 脱硫剂 | 出口硫(mg/m3) | 脱硫温度 | 操作压力 | 再生条件 |
| 一氧化碳 | <1.33 | 300~400 | 0~3.0 | 蒸气再生 |
| 活性炭 | <1.33 | 常温 | 0~3.0 | 蒸气再生 |
| 氧化锌 | <1.33 | 350~400 | 0~3.0 | 不再生 |
在密闭容器中,充入一定量的
 气体,发生分解反应
气体,发生分解反应 ,控制不同的温度和压强,实验结果如图。
,控制不同的温度和压强,实验结果如图。
(3)图中压强P1、P2、P3由大到小的顺序为
 的平衡转化率,可以采取的措施有
的平衡转化率,可以采取的措施有(4)若压强为P2、温度为975℃,
 的平衡常数
的平衡常数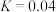 ,则起始
,则起始 的物质的量浓度c=
的物质的量浓度c= 气体,相同温度下再次达到平衡时,K
气体,相同温度下再次达到平衡时,KⅢ.间接电解法脱硫
通过
 溶液吸收并氧化
溶液吸收并氧化 气体,再通过电解再生,实现循环使用,该法处理过程如图。
气体,再通过电解再生,实现循环使用,该法处理过程如图。
(5)电解反应器中总反应的离子方程式为
您最近一年使用:0次
【推荐1】将天然气(主要成分为CH4)中的CO2、H2S资源化转化在能源利用、环境保护等方面意义重大。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=﹣530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是___________ 。
(2)CO2性质稳定,是一种“惰性”分子。对于反应ⅲ,通过设计合适的催化剂可以降低______ ,提高反应速率。
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应ⅲ,工作原理如下所示。
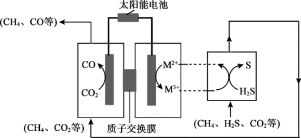
【方案1】若M3+/M2+=Fe3+/Fe2+
①所含Fe3+、Fe2+的溶液需为较强的酸性,原因是___________ 。
②结合反应式说明生成S、CO的原理:___________ 。
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+(配合物)
已知:电解效率η的定义:
③测得η(EDTA-Fe3+)≈100%,η(CO)≈80%。阴极放电的物质有___________ 。
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1:CO2通过电极反应产生CO
来源2:电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是___________ 。
结论:方案2明显优于方案1,该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=﹣530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是
(2)CO2性质稳定,是一种“惰性”分子。对于反应ⅲ,通过设计合适的催化剂可以降低
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应ⅲ,工作原理如下所示。

【方案1】若M3+/M2+=Fe3+/Fe2+
①所含Fe3+、Fe2+的溶液需为较强的酸性,原因是
②结合反应式说明生成S、CO的原理:
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+(配合物)
已知:电解效率η的定义:

③测得η(EDTA-Fe3+)≈100%,η(CO)≈80%。阴极放电的物质有
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1:CO2通过电极反应产生CO
来源2:电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是
结论:方案2明显优于方案1,该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】煤炭燃烧后产生大量的 和
和 等气体,采用适当方法吸收后可将
等气体,采用适当方法吸收后可将 和
和 变废为宝。方法之一是利用饱和碳酸钠溶液吸收含有一定体积比的
变废为宝。方法之一是利用饱和碳酸钠溶液吸收含有一定体积比的 和
和 的烟气。已知:
的烟气。已知:
(1)当通入少量烟气时,发生的离子方程式为___________ ;___________ 。
(2)当吸收一定量烟气后,测定 ,则此时溶液的
,则此时溶液的
___________ ,测得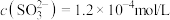 ,则
,则
___________ 。
(3)库仑测硫仪可测定烟气中 气体含量。已知:库仑测硫仪中电解原理示意图如下。检测前,电解质溶液中
气体含量。已知:库仑测硫仪中电解原理示意图如下。检测前,电解质溶液中 保持定值时,电解池不工作。待测气体进入电解池后,
保持定值时,电解池不工作。待测气体进入电解池后, 溶解并将
溶解并将 还原:
还原: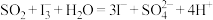 ,测硫仪便立即自动进行电解到
,测硫仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量。
又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量。
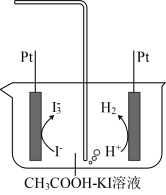
①通入 的Pt电极连接电源的
的Pt电极连接电源的___________ (填正极或负极)。
②测硫仪工作时电解池的阴极反应式为___________ 。
③当通入a升烟气(已折算成标准状况下,下同)时,电解池中溢出的 为2.0升,则烟气中
为2.0升,则烟气中 的体积分数为
的体积分数为___________ 。
 和
和 等气体,采用适当方法吸收后可将
等气体,采用适当方法吸收后可将 和
和 变废为宝。方法之一是利用饱和碳酸钠溶液吸收含有一定体积比的
变废为宝。方法之一是利用饱和碳酸钠溶液吸收含有一定体积比的 和
和 的烟气。已知:
的烟气。已知:| 弱酸 |  |  |
| 电离平衡常数(25℃) |  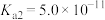 | 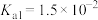  |
(2)当吸收一定量烟气后,测定
 ,则此时溶液的
,则此时溶液的
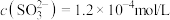 ,则
,则
(3)库仑测硫仪可测定烟气中
 气体含量。已知:库仑测硫仪中电解原理示意图如下。检测前,电解质溶液中
气体含量。已知:库仑测硫仪中电解原理示意图如下。检测前,电解质溶液中 保持定值时,电解池不工作。待测气体进入电解池后,
保持定值时,电解池不工作。待测气体进入电解池后, 溶解并将
溶解并将 还原:
还原: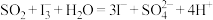 ,测硫仪便立即自动进行电解到
,测硫仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量。
又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量。
①通入
 的Pt电极连接电源的
的Pt电极连接电源的②测硫仪工作时电解池的阴极反应式为
③当通入a升烟气(已折算成标准状况下,下同)时,电解池中溢出的
 为2.0升,则烟气中
为2.0升,则烟气中 的体积分数为
的体积分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】碲被誉为现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁。工业上从某电镀污泥(含有Cu2Te、Cr2O3以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。
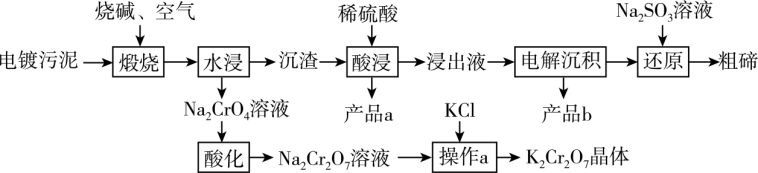
已知:①沉淀时c(Cr3+)与pH的关系,
②溶解度。
回答下列问题:
(1)“煅烧”时气体与固体原料逆流而行,目的为_____ ;此时Cr2O3发生反应的化学方程式为_____ 。
(2)已知浸出液中含有TeOSO4,每得到25.6g碲,理论上消耗0.8mol•L-1Na2SO3溶液的体积为_____ mL。产品b的基态原子核外电子排布式为_____ 。
(3)请补充“操作a”的实验方案:向Na2Cr2O7溶液中加入KCl固体,_____ ,得到K2Cr2O7晶体。
(4)铬(VI)毒性很高,工业上常用铁和石墨作电极,处理含Cr2O 的酸性废水。通电后Cr2O
的酸性废水。通电后Cr2O 先转变为Cr3+,一段时间后变成Cr(OH)3沉淀而被除去。其中铁电极的作用是电子导体和
先转变为Cr3+,一段时间后变成Cr(OH)3沉淀而被除去。其中铁电极的作用是电子导体和_____ 。当电解后溶液中Cr3+浓度为0.01mol•L-1时,其开始沉降时废水的pH为_____ 。

已知:①沉淀时c(Cr3+)与pH的关系,
| c(Cr3+) | pH | |
| 开始沉淀 | 0.1mol•L-1 | 3.68 |
| 沉淀完全 | 1×10-5mol•L-1 | 5 |
| 溶解度 | K2Cr2O7 | NaCl |
| 100℃ | 95.1g | 39.8g |
| 25℃ | 4.6g | 36g |
(1)“煅烧”时气体与固体原料逆流而行,目的为
(2)已知浸出液中含有TeOSO4,每得到25.6g碲,理论上消耗0.8mol•L-1Na2SO3溶液的体积为
(3)请补充“操作a”的实验方案:向Na2Cr2O7溶液中加入KCl固体,
(4)铬(VI)毒性很高,工业上常用铁和石墨作电极,处理含Cr2O
 的酸性废水。通电后Cr2O
的酸性废水。通电后Cr2O 先转变为Cr3+,一段时间后变成Cr(OH)3沉淀而被除去。其中铁电极的作用是电子导体和
先转变为Cr3+,一段时间后变成Cr(OH)3沉淀而被除去。其中铁电极的作用是电子导体和
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料生产铝和氮化铝的一种工艺流程如下【已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀】。
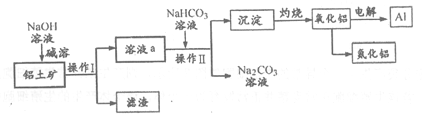
(1)操作I、Ⅱ的名称为____________ 。
(2)用氧化物的形式表示铝硅酸钠的化学式_____________ 。
(3)溶液a中加入NaHCO3后,生成沉淀的离子方程式为____________ 。
(4)Al2O3比另外一种铝的化合物AlCl3熔点高出很多,原因是_________ ; 有人考虑用熔融态AlCl3电解制备铝,你觉得是否可行,____ (选填“可行”或“不可行”),试分析原因_________ 。
(5)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开K2,加入NaOH浓溶液,至不再产生NH3。打开K1,通入N2一段时间。
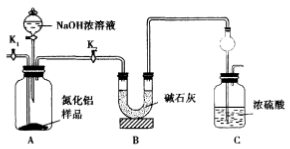
①实验中需要测定的数据是___________ 。
②由于装置存在缺陷,导致测定结果偏高,请提出改进方法:___________ 。

(1)操作I、Ⅱ的名称为
(2)用氧化物的形式表示铝硅酸钠的化学式
(3)溶液a中加入NaHCO3后,生成沉淀的离子方程式为
(4)Al2O3比另外一种铝的化合物AlCl3熔点高出很多,原因是
(5)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开K2,加入NaOH浓溶液,至不再产生NH3。打开K1,通入N2一段时间。

①实验中需要测定的数据是
②由于装置存在缺陷,导致测定结果偏高,请提出改进方法:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】氯化亚铜是一种应用较广的催化剂,易水解。以低品位铜矿砂(主要成分CuS)为原料制备氯化亚铜的路线如下:
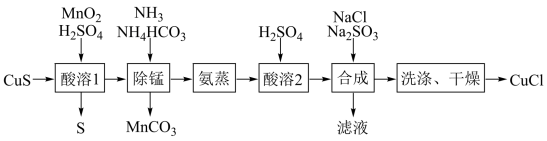
(1)酸溶1步骤中加入MnO2的作用是______ 。
(2)除锰步骤Mn2+转化为MnCO3沉淀,该反应的离子方程式为______ 。溶液中CuSO4转变为Cu(NH3)4CO3留在溶液中。
(3)蒸氨步骤会得到CuO固体,该步骤在减压条件下进行的原因是______ 。
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生SO2气体,除可能与酸溶时硫酸过量有关,还可能的原因是______ 。
(5)有工艺将合成步骤的NaCl与Na2SO3换为NH4Cl和(NH4)2SO3,则可获得一种可作为氮肥的副产品,其化学式为_____ 。
(6)洗涤步骤先用______ 洗,再用无水乙醇洗涤。

(1)酸溶1步骤中加入MnO2的作用是
(2)除锰步骤Mn2+转化为MnCO3沉淀,该反应的离子方程式为
(3)蒸氨步骤会得到CuO固体,该步骤在减压条件下进行的原因是
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生SO2气体,除可能与酸溶时硫酸过量有关,还可能的原因是
(5)有工艺将合成步骤的NaCl与Na2SO3换为NH4Cl和(NH4)2SO3,则可获得一种可作为氮肥的副产品,其化学式为
(6)洗涤步骤先用
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】磷石膏是磷氨厂生产硫酸和磷酸所排放的废渣 主要成分为
主要成分为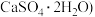 ,大量堆积既占用土地,又易造成环境污染和硫资源的浪费,所以可从资源综合利用的角度将磷石膏转化成硫酸钾和氯化钙晶体,工艺流程如下:
,大量堆积既占用土地,又易造成环境污染和硫资源的浪费,所以可从资源综合利用的角度将磷石膏转化成硫酸钾和氯化钙晶体,工艺流程如下:
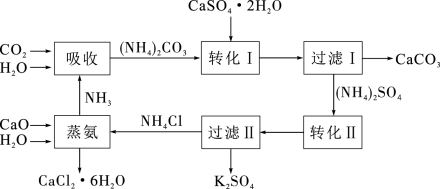
请回答以下问题:
 为了提高原料的利用率,吸收流程中通入
为了提高原料的利用率,吸收流程中通入 和
和 的先后顺序最好为
的先后顺序最好为______ 。
 碳酸铵溶液与磷石膏悬浊溶液混合后发生转化I的离子反应方程式为
碳酸铵溶液与磷石膏悬浊溶液混合后发生转化I的离子反应方程式为______ 。
 工艺流程中除了所给出的
工艺流程中除了所给出的 、
、 、
、 、
、 等原料外,在转化Ⅱ的过程中还需要加入
等原料外,在转化Ⅱ的过程中还需要加入______ 原料。
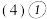 过滤Ⅱ后所得滤液
过滤Ⅱ后所得滤液 溶液,确认其中含有
溶液,确认其中含有 的方法是:
的方法是:______ ;
 氯化钙结晶水合物
氯化钙结晶水合物 是目前常用的无机储热材料,选择的依据是因为
是目前常用的无机储热材料,选择的依据是因为______  选填序号
选填序号 ;
;
A.熔点较低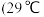 熔化
熔化
 能导电
能导电  能制冷
能制冷  无毒
无毒
 已知不同温度下
已知不同温度下 在100g水中达到饱和时溶解的量如下表:
在100g水中达到饱和时溶解的量如下表:
 时
时 的饱和溶液
的饱和溶液 冷却到
冷却到 ,可析出
,可析出 晶体
晶体______ g。
 上述工艺流程中循环利用的物质是
上述工艺流程中循环利用的物质是______ ;还有一种物质,只要其纯净,也可以被循环利用,它是______  均填化学式
均填化学式 。
。
 主要成分为
主要成分为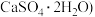 ,大量堆积既占用土地,又易造成环境污染和硫资源的浪费,所以可从资源综合利用的角度将磷石膏转化成硫酸钾和氯化钙晶体,工艺流程如下:
,大量堆积既占用土地,又易造成环境污染和硫资源的浪费,所以可从资源综合利用的角度将磷石膏转化成硫酸钾和氯化钙晶体,工艺流程如下:
请回答以下问题:
 为了提高原料的利用率,吸收流程中通入
为了提高原料的利用率,吸收流程中通入 和
和 的先后顺序最好为
的先后顺序最好为 碳酸铵溶液与磷石膏悬浊溶液混合后发生转化I的离子反应方程式为
碳酸铵溶液与磷石膏悬浊溶液混合后发生转化I的离子反应方程式为 工艺流程中除了所给出的
工艺流程中除了所给出的 、
、 、
、 、
、 等原料外,在转化Ⅱ的过程中还需要加入
等原料外,在转化Ⅱ的过程中还需要加入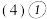 过滤Ⅱ后所得滤液
过滤Ⅱ后所得滤液 溶液,确认其中含有
溶液,确认其中含有 的方法是:
的方法是: 氯化钙结晶水合物
氯化钙结晶水合物 是目前常用的无机储热材料,选择的依据是因为
是目前常用的无机储热材料,选择的依据是因为 选填序号
选填序号 ;
;A.熔点较低
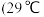 熔化
熔化
 能导电
能导电  能制冷
能制冷  无毒
无毒 已知不同温度下
已知不同温度下 在100g水中达到饱和时溶解的量如下表:
在100g水中达到饱和时溶解的量如下表:温度 | 0 | 20 | 60 |
 溶解的量 溶解的量 | 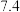 | 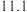 | 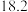 |
 时
时 的饱和溶液
的饱和溶液 冷却到
冷却到 ,可析出
,可析出 晶体
晶体 上述工艺流程中循环利用的物质是
上述工艺流程中循环利用的物质是 均填化学式
均填化学式 。
。
您最近一年使用:0次




