以软锰矿(主要成分为 ,还含少量Fe、Si、Al、Ca、Mg等的氧化物)和硫铁矿(主要成分
,还含少量Fe、Si、Al、Ca、Mg等的氧化物)和硫铁矿(主要成分 )为原料,两矿联合浸取可制备大颗粒的电池用
)为原料,两矿联合浸取可制备大颗粒的电池用 。
。 和
和 颗粒构成两个原电池反应,其原理如图1所示(部分产物未标出)。
颗粒构成两个原电池反应,其原理如图1所示(部分产物未标出)。 的电子排布式为:
的电子排布式为:___________ 。
②若 原电池中生成单质S,其电池总反应的离子方程式为
原电池中生成单质S,其电池总反应的离子方程式为___________ 。
③随硫铁矿的增加,锰的浸出率降低,可能的原因是___________ 。
(2)除钙镁:向已除去Fe、Al、Si元素的 溶液中(pH约为5)加入
溶液中(pH约为5)加入 溶液,将
溶液,将 、
、 转化为氟化物沉淀。则
转化为氟化物沉淀。则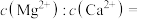
___________ 。
[已知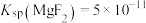 ,
,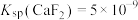 ]
]
(3)氧化:将“沉淀”步骤所得含少量 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得 。
。
①写出由 反应得到
反应得到 的化学方程式
的化学方程式___________ 。
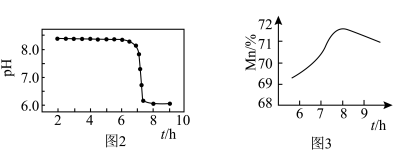
②沉淀加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是___________ 。___________ 。
 ,还含少量Fe、Si、Al、Ca、Mg等的氧化物)和硫铁矿(主要成分
,还含少量Fe、Si、Al、Ca、Mg等的氧化物)和硫铁矿(主要成分 )为原料,两矿联合浸取可制备大颗粒的电池用
)为原料,两矿联合浸取可制备大颗粒的电池用 。
。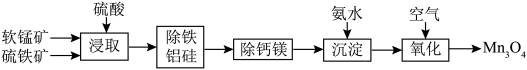
 和
和 颗粒构成两个原电池反应,其原理如图1所示(部分产物未标出)。
颗粒构成两个原电池反应,其原理如图1所示(部分产物未标出)。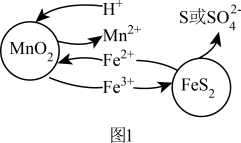
 的电子排布式为:
的电子排布式为:②若
 原电池中生成单质S,其电池总反应的离子方程式为
原电池中生成单质S,其电池总反应的离子方程式为③随硫铁矿的增加,锰的浸出率降低,可能的原因是
(2)除钙镁:向已除去Fe、Al、Si元素的
 溶液中(pH约为5)加入
溶液中(pH约为5)加入 溶液,将
溶液,将 、
、 转化为氟化物沉淀。则
转化为氟化物沉淀。则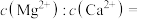
[已知
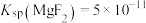 ,
,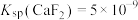 ]
](3)氧化:将“沉淀”步骤所得含少量
 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得 。
。①写出由
 反应得到
反应得到 的化学方程式
的化学方程式②沉淀加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是
更新时间:2024-04-26 11:41:54
|
相似题推荐
【推荐1】金属钴、镍作为重要的战略资源,有“工业味精”之称,工业上利用红土镍矿(主要成分为Ni、Co、Fe、Al、Si等元素的氧化物)生产中间品MSP(硫化钴镍),并利用MSP进一步生产NiSO4的流程如图。
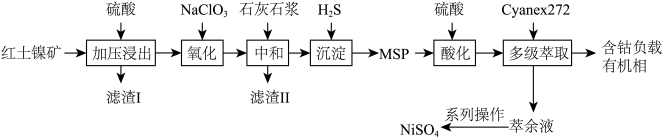
ii.氧化前后,溶液中Ni、Co元素的化合价均为+2价。
回答下列问题:
(1)“加压浸出”时,滤渣I的主要成分为______ (填化学式)。
(2)“氧化”时,加入NaClO3的目的是______ (用离子方程式表示),NaClO3中阴离子的空间结构为______ 。
(3)“中和”时,应控制的pH范围是_____ 。
(4)Cyanex272(RH)是一种有机萃取剂,其作用原理为nRH+Mn+ RnM+nH+(Mn+表示金属阳离子),从“含钴负载有机相”中重新获取Cyanex272的方法是
RnM+nH+(Mn+表示金属阳离子),从“含钴负载有机相”中重新获取Cyanex272的方法是_____ 。
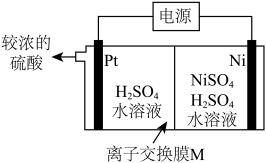
(5)工业上利用电解NiSO4溶液制备Ni的同时可获得较浓的硫酸,电解装置如图所示,离子交换膜M为_____ (填“阳”或“阴”)离子交换膜,阳极反应式为_____ 。
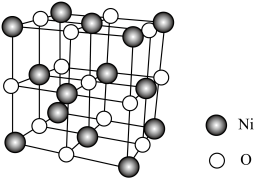
(6)NiSO4在一定条件下分解可得到镍的某种氧化物,其晶胞如图所示。该晶体中与O距离最近且相等的Ni的个数为_____ 。已知晶胞内Ni和O的最短距离为apm,设NA为阿伏加德罗常数的值,则该晶体的密度为_____ g•cm-3。

| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀的pH | 2.3 | 7.0 | 3.1 | 6.9 | 7.1 |
| 沉淀完全的pH | 3.7 | 9.0 | 4.5 | 8.9 | 9.1 |
回答下列问题:
(1)“加压浸出”时,滤渣I的主要成分为
(2)“氧化”时,加入NaClO3的目的是
(3)“中和”时,应控制的pH范围是
(4)Cyanex272(RH)是一种有机萃取剂,其作用原理为nRH+Mn+
 RnM+nH+(Mn+表示金属阳离子),从“含钴负载有机相”中重新获取Cyanex272的方法是
RnM+nH+(Mn+表示金属阳离子),从“含钴负载有机相”中重新获取Cyanex272的方法是(5)工业上利用电解NiSO4溶液制备Ni的同时可获得较浓的硫酸,电解装置如图所示,离子交换膜M为

(6)NiSO4在一定条件下分解可得到镍的某种氧化物,其晶胞如图所示。该晶体中与O距离最近且相等的Ni的个数为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】按要求回答问题
(1)给有机物命名,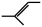 名称
名称________________________ 。
(2) 写出符合分子式C3H8O的有机物的结构简式(如乙酸结构简式为CH3COOH):CH3CH2CH2OH,__________________________________________________ 。
(3)配平下列反应离子方程式:
As2S3 + H2O + NO3- AsO
AsO + SO
+ SO + NO↑ + (未配平)
+ NO↑ + (未配平)
___________________________________________________________
(4)某地污水中的有机污染物主要成分是三氯乙烯(C2HCl3),向污水中加入KMnO4(其还原产物为MnO2)可将三氯乙烯除去,其生成物不污染环境,写出该反应的化学方程式:_____ 。
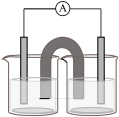
(5)根据氧化还原反应:2 Fe3+ + Cu = 2Fe2+ +Cu2+,设计一个盐桥原电池。画出原电池结构图(需注明电极、电解质溶液、盐桥)。___
(1)给有机物命名,
 名称
名称(2) 写出符合分子式C3H8O的有机物的结构简式(如乙酸结构简式为CH3COOH):CH3CH2CH2OH,
(3)配平下列反应离子方程式:
As2S3 + H2O + NO3-
 AsO
AsO + SO
+ SO + NO↑ + (未配平)
+ NO↑ + (未配平)(4)某地污水中的有机污染物主要成分是三氯乙烯(C2HCl3),向污水中加入KMnO4(其还原产物为MnO2)可将三氯乙烯除去,其生成物不污染环境,写出该反应的化学方程式:
(5)根据氧化还原反应:2 Fe3+ + Cu = 2Fe2+ +Cu2+,设计一个盐桥原电池。画出原电池结构图(需注明电极、电解质溶液、盐桥)。

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂。回答下列问题:
(1)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为________ 。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
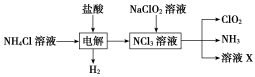
①电解时发生反应的化学方程式为________________ 。
②溶液X中大量存在的阴离子有________ 。
③除去ClO2中的NH3可选用的试剂是________ (填标号)。
a.水 b.碱石灰
c.浓硫酸 d.饱和食盐水
(3)用ClO2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是________ (填标号)。
a.明矾 b.碘化钾
c.盐酸 d.硫酸亚铁
(1)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

①电解时发生反应的化学方程式为
②溶液X中大量存在的阴离子有
③除去ClO2中的NH3可选用的试剂是
a.水 b.碱石灰
c.浓硫酸 d.饱和食盐水
(3)用ClO2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是
a.明矾 b.碘化钾
c.盐酸 d.硫酸亚铁
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】重铬酸盐广泛用作氧化剂、皮革制作等。以铬矿石(主要成分是Cr2O3,含FeO、Al2O3、 SiO2等杂质)为原料制取重铬酸钠的流程如下:

请回答下列问题:
(1) 固体残渣主要是含________ 元素的氧化物。
(2)写出Cr2O3与纯碱在高温焙烧时反应的化学方程式_______________________ 。
(3)高温焙烧后粉碎的目的是_____________________________ ,调节pH时形成的沉淀的成分是_______________________________________________ 。
(4)写出硫酸酸化使Na2CrO4转化为Na2Cr2O7的离子方程式______________________ 。
(5)某工厂采用石墨电极电解Na2CrO4溶液,实 现了 Na2CrO4到Na2Cr2O7的转化,其原理如图所示。写出阳极的电极反应式____________________ 。

(6)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化 所需要O2的质量)。现有某水样100.00 mL,酸化后加入C1 mol/L的Na2Cr2O7溶液 V1 mL,使水中的还原性物质完全被氧化(Cr2O72-还原为Cr3+);再用C2mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2 mL。
①该水样的COD为________________ mg/L;
②假设上述反应后所得溶液中Fe3+和Cr3+的物质的量浓度均为0.1 mol/L,要使Fe3 +沉 淀完全而Cr3+还未开始沉淀.则需调节溶液pH的范围是______________ 。(可能用到的数据:KSPFe(OH)3=4.0×10-38, KSPCr(OH)3=6.0×10-31,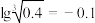 ,
,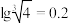 ,
,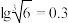 ,
, )
)

请回答下列问题:
(1) 固体残渣主要是含
(2)写出Cr2O3与纯碱在高温焙烧时反应的化学方程式
(3)高温焙烧后粉碎的目的是
(4)写出硫酸酸化使Na2CrO4转化为Na2Cr2O7的离子方程式
(5)某工厂采用石墨电极电解Na2CrO4溶液,实 现了 Na2CrO4到Na2Cr2O7的转化,其原理如图所示。写出阳极的电极反应式

(6)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化 所需要O2的质量)。现有某水样100.00 mL,酸化后加入C1 mol/L的Na2Cr2O7溶液 V1 mL,使水中的还原性物质完全被氧化(Cr2O72-还原为Cr3+);再用C2mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2 mL。
①该水样的COD为
②假设上述反应后所得溶液中Fe3+和Cr3+的物质的量浓度均为0.1 mol/L,要使Fe3 +沉 淀完全而Cr3+还未开始沉淀.则需调节溶液pH的范围是
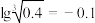 ,
,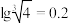 ,
,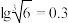 ,
, )
)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】CoC2O4是制备金属钴的原料。利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:

(1) “550℃焙烧”目的是_______ ,过滤用到的玻璃仪器除了烧杯、玻璃棒还有_______ 。
(2)“碱浸”时主要反应的化学方程式为_______ 。
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为_______ 。
(4)“净化除杂1”过程中,需在40~50℃加入H2O2溶液,其目的是_______ ;再升温至80~85℃,加入Na2CO3溶液,调pH至4.5,产生“滤渣1”主要成分为_______ (填化学式)。
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Mg2+)=7.0×10-6mol/L,则滤液中c(Ca2+)=_______ [已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10]。

(1) “550℃焙烧”目的是
(2)“碱浸”时主要反应的化学方程式为
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为
(4)“净化除杂1”过程中,需在40~50℃加入H2O2溶液,其目的是
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Mg2+)=7.0×10-6mol/L,则滤液中c(Ca2+)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】以钴渣(主要成分是 ,含少量
,含少量 、CuO、CdO、
、CuO、CdO、 等)为原料制备钴和钴酸锂的流程如图:
等)为原料制备钴和钴酸锂的流程如图:
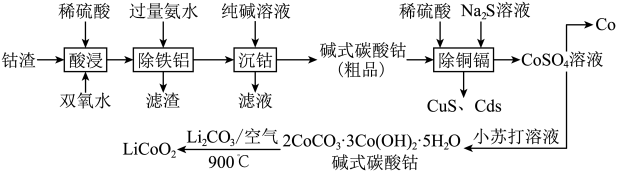
已知:①常温下,几种物质的溶度积如表所示。
②常温下, 的电离常数
的电离常数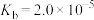 。
。
请回答下列问题:
(1)“酸浸”前需要将钴渣粉碎,原因是___________ 。
(2)“酸浸”时双氧水的作用是___________ 。
(3)“酸浸”时钴的浸出率与液固比的关系如图1所示。最佳液固比为___________ mL·g-1;当液固比一定时,相同时间内钴的浸出率与温度的关系如图2所示,解释40℃时钴的浸出率达到峰值的原因:___________ 。

(4)“除铁铝”中,如果 、
、 浓度相等,先产生沉淀的离子是
浓度相等,先产生沉淀的离子是___________ (填离子符号), 的平衡常数
的平衡常数
___________
(5)在“除铜镉”中,如果溶液中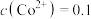 mol/L,当
mol/L,当 mol/L时,
mol/L时,___________ (填“有”或“没有”)CoS生成。
(6)在 溶液中加入小苏打溶液产生碱式碳酸钴并放出气体,写出反应的离子方程式:
溶液中加入小苏打溶液产生碱式碳酸钴并放出气体,写出反应的离子方程式:___________ 。
 ,含少量
,含少量 、CuO、CdO、
、CuO、CdO、 等)为原料制备钴和钴酸锂的流程如图:
等)为原料制备钴和钴酸锂的流程如图:
已知:①常温下,几种物质的溶度积如表所示。
| 物质 |  |  | CuS | CdS | CoS |
 的近似值 的近似值 | 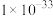 | 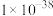 | 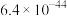 | 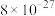 |  |
 的电离常数
的电离常数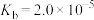 。
。请回答下列问题:
(1)“酸浸”前需要将钴渣粉碎,原因是
(2)“酸浸”时双氧水的作用是
(3)“酸浸”时钴的浸出率与液固比的关系如图1所示。最佳液固比为

(4)“除铁铝”中,如果
 、
、 浓度相等,先产生沉淀的离子是
浓度相等,先产生沉淀的离子是 的平衡常数
的平衡常数
(5)在“除铜镉”中,如果溶液中
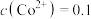 mol/L,当
mol/L,当 mol/L时,
mol/L时,(6)在
 溶液中加入小苏打溶液产生碱式碳酸钴并放出气体,写出反应的离子方程式:
溶液中加入小苏打溶液产生碱式碳酸钴并放出气体,写出反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题。
(1)基态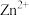 的核外电子排布式为
的核外电子排布式为_______ 。
(2)在醋酸溶液中 可与四苯硼化钠作用生成四苯硼化钾
可与四苯硼化钠作用生成四苯硼化钾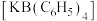 白色沉淀。若将“
白色沉淀。若将“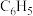 ”(苯基)视为一个整体,则阴离子
”(苯基)视为一个整体,则阴离子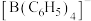 的空间构型是
的空间构型是_______ ,在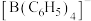 中不存在的化学键是
中不存在的化学键是_______ (填字母)。
A.配位键 B.非极性键 C.π键 D.离子键
(3)已知物质间的转化关系如图所示,其中a、c均大于0。
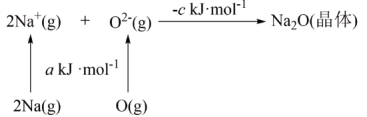
①基态钠原子的第一电离能为_______  。
。
②相同条件下, 的晶格能
的晶格能_______ (填“>”“<”或“=”)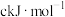 ,原因为
,原因为_______ 。
(4) 的立方晶胞结构如图所示。若紧邻的两个
的立方晶胞结构如图所示。若紧邻的两个 之间的距离为dpm,阿伏加德罗常数的值为
之间的距离为dpm,阿伏加德罗常数的值为 ,晶体的密度为
,晶体的密度为 ,则A原子的分数坐标为
,则A原子的分数坐标为_____ ;Na的摩尔质量可表示为____  (用含有d、ρ、
(用含有d、ρ、 的代数式表示)。
的代数式表示)。

(1)基态
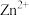 的核外电子排布式为
的核外电子排布式为(2)在醋酸溶液中
 可与四苯硼化钠作用生成四苯硼化钾
可与四苯硼化钠作用生成四苯硼化钾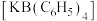 白色沉淀。若将“
白色沉淀。若将“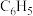 ”(苯基)视为一个整体,则阴离子
”(苯基)视为一个整体,则阴离子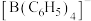 的空间构型是
的空间构型是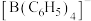 中不存在的化学键是
中不存在的化学键是A.配位键 B.非极性键 C.π键 D.离子键
(3)已知物质间的转化关系如图所示,其中a、c均大于0。

①基态钠原子的第一电离能为
 。
。②相同条件下,
 的晶格能
的晶格能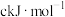 ,原因为
,原因为(4)
 的立方晶胞结构如图所示。若紧邻的两个
的立方晶胞结构如图所示。若紧邻的两个 之间的距离为dpm,阿伏加德罗常数的值为
之间的距离为dpm,阿伏加德罗常数的值为 ,晶体的密度为
,晶体的密度为 ,则A原子的分数坐标为
,则A原子的分数坐标为 (用含有d、ρ、
(用含有d、ρ、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】已知A,B,C,D都是周期表中的短周期元素,它们的核电荷数依次增大。A原子,C原子的L能层中,都有两个未成对的电子,C,D同主族。E,F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号___ ,该能层具有的原子轨道数为__ ;
(2)E2+离子的价层电子排布图是__ ;
(3)A的最高价氧化物对应的水化物,其中心原子采取的轨道杂化方式为__ ,B的气态氢化物的VSEPR模型为__ 。
(4)DAB-的电子式为___ ;
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6。甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程式为__ 。
(1)基态D原子中,电子占据的最高能层符号
(2)E2+离子的价层电子排布图是
(3)A的最高价氧化物对应的水化物,其中心原子采取的轨道杂化方式为
(4)DAB-的电子式为
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6。甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有A、B、C、D、E、F六种短周期元素,其原子序数依次增大,A元素基态原子的p能级上的电子数等于次外层电子数,C元素基态原子的s能级与p能级上的电子数相等,D是短周期中电负性最小的元素,E原子的第一电离能至第四电离能分别为578、1817、2745、11575(单位:kJ·mol-1),F原子的价电子构型与C原子的相同。请回答下列问题:
(1)推测B的电负性___________ (填“>”或“<”)F的电负性。
(2)写出D原子的电子排布图:___________ ,该原子的能层数为___________ 。
(3)写出元素E与D的最高价氧化物对应的水化物的水溶液反应的离子方程式:___________ 。
(1)推测B的电负性
(2)写出D原子的电子排布图:
(3)写出元素E与D的最高价氧化物对应的水化物的水溶液反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】无水氯化铝 是有机化工中常用的催化剂,升华温度为
是有机化工中常用的催化剂,升华温度为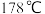 ,极易潮解,遇水后会发热并产生白雾,某兴趣小组利用重铬酸钾
,极易潮解,遇水后会发热并产生白雾,某兴趣小组利用重铬酸钾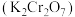 和浓盐酸反应制得的
和浓盐酸反应制得的 与
与 ,炭粉反应制取无水氯化铝,实验装置如图。
,炭粉反应制取无水氯化铝,实验装置如图。

已知:① 与浓盐酸反应被还原为
与浓盐酸反应被还原为 ;
;
②装置C中发生的反应为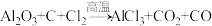 (未配平)。
(未配平)。
回答下列问题:
(1)装置A的圆底烧瓶中发生反应的离子方程式为___________ ;按气流方向从左到右,仪器接口的连接顺序为
___________ (填字母)。
(2)连接好装置后部分实验操作如下:
①装药品 ②检查装置气密性 ③点燃装置C处的酒精灯 ④打开分液漏斗的活塞滴加浓盐酸。实验时,正确的操作顺序是___________ (填序号)。
(3)若装置C漏气,可观察到硬质玻璃管管口附近产生“白雾”( 与水蒸气相遇),产生
与水蒸气相遇),产生 的原因是
的原因是___________ (用化学方程式表示)。
(4)装置B采用冰水浴的目的是___________ ;装置E的作用是___________ ,经过装置E处理后的尾气中对环境有害的气体是___________ (用分子式表示)。
(5)装置C出口导管X用粗短导管的目的是___________(填标号)。
(6)在高温下,向足量 粉末与
粉末与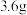 炭粉的混合物中通入
炭粉的混合物中通入 ,炭粉与
,炭粉与 (标准状况)
(标准状况) 恰好完全反应。则反应
恰好完全反应。则反应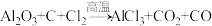 (未配平)中生成的
(未配平)中生成的 与
与 的物质的量之比
的物质的量之比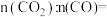
___________ 。
 是有机化工中常用的催化剂,升华温度为
是有机化工中常用的催化剂,升华温度为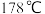 ,极易潮解,遇水后会发热并产生白雾,某兴趣小组利用重铬酸钾
,极易潮解,遇水后会发热并产生白雾,某兴趣小组利用重铬酸钾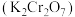 和浓盐酸反应制得的
和浓盐酸反应制得的 与
与 ,炭粉反应制取无水氯化铝,实验装置如图。
,炭粉反应制取无水氯化铝,实验装置如图。
已知:①
 与浓盐酸反应被还原为
与浓盐酸反应被还原为 ;
;②装置C中发生的反应为
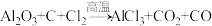 (未配平)。
(未配平)。回答下列问题:
(1)装置A的圆底烧瓶中发生反应的离子方程式为

(2)连接好装置后部分实验操作如下:
①装药品 ②检查装置气密性 ③点燃装置C处的酒精灯 ④打开分液漏斗的活塞滴加浓盐酸。实验时,正确的操作顺序是
(3)若装置C漏气,可观察到硬质玻璃管管口附近产生“白雾”(
 与水蒸气相遇),产生
与水蒸气相遇),产生 的原因是
的原因是(4)装置B采用冰水浴的目的是
(5)装置C出口导管X用粗短导管的目的是___________(填标号)。
| A.防堵塞 | B.防倒吸 | C.平衡气压 | D.冷凝回流 |
 粉末与
粉末与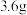 炭粉的混合物中通入
炭粉的混合物中通入 ,炭粉与
,炭粉与 (标准状况)
(标准状况) 恰好完全反应。则反应
恰好完全反应。则反应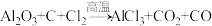 (未配平)中生成的
(未配平)中生成的 与
与 的物质的量之比
的物质的量之比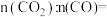
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】孔雀石主要成分是Cu2(OH)2CO3,还含少量FeCO3及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如图:

有关物质沉淀的pH数据如表:
(1)步骤Ⅰ加稀硫酸充分反应,过滤得到滤渣的主要成分是___ (填化学式)。
(2)步骤Ⅱ中试剂①应选用试剂__ (填代号)。
a.KMnO4 b.稀HNO3 c.双氧水 d.氯水
相关反应的离子方程式为:___ 。
(3)步骤Ⅲ加入CuO调节溶液的pH至3.2≤pH<4.7,目的是__ 。
(4)步骤IV获得硫酸铜晶体的操作中,必须采取的实验措施是__ 。
(5)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10-3mol/L,必须将溶液调节至pH=__ 。
(6)用NH3和孔雀石反应可以制得金属铜,则该反应的化学方程式为__ 。

有关物质沉淀的pH数据如表:
| 物质 | pH(开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
(1)步骤Ⅰ加稀硫酸充分反应,过滤得到滤渣的主要成分是
(2)步骤Ⅱ中试剂①应选用试剂
a.KMnO4 b.稀HNO3 c.双氧水 d.氯水
相关反应的离子方程式为:
(3)步骤Ⅲ加入CuO调节溶液的pH至3.2≤pH<4.7,目的是
(4)步骤IV获得硫酸铜晶体的操作中,必须采取的实验措施是
(5)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10-3mol/L,必须将溶液调节至pH=
(6)用NH3和孔雀石反应可以制得金属铜,则该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】有兴趣研究小组用工业废渣(主要成分为Cu2S和Fe2O3)制取氯化亚铜并同时生成电路板蚀刻液。资料显示:氯化亚铜(化学式为CuCl)常用作有机合成工业中的催化剂,通常是一种白色粉末,微溶于水、不溶于乙醇,在潮湿空气中易水解氧化成绿色;见光则分解。
他们设计流程如下:

据此流程和以上信息回答下列问题:
(1)验证焙烧气体产物是SO2的方法______________________________________ ;溶解固体A对应的化学方程式为_____________________________________ 。
(2)SO2吸收用NaOH溶液,为得到纯净的Na2SO3溶液,其操作应为_____________________________________________________________________ 。
(3)在Na2SO3的水溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸混匀,倾出清液,抽滤即得CuCl沉淀.写出该反应的离子方程式______ 。
(4)CuCl沉淀的洗涤需要经过酸洗、水洗和醇洗,水洗操作为____________________ ;醇洗不能省略,原因是______ 。
(5)得到CuCl沉淀要迅速真空干燥、冷却,密封包装。这样操作的目的是_______________________________________________________ 。
(6)氯化亚铜在热水中迅速与水反应生成砖红色固体,写出该反应的化学方程式_________________ 。
他们设计流程如下:

据此流程和以上信息回答下列问题:
(1)验证焙烧气体产物是SO2的方法
(2)SO2吸收用NaOH溶液,为得到纯净的Na2SO3溶液,其操作应为
(3)在Na2SO3的水溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸混匀,倾出清液,抽滤即得CuCl沉淀.写出该反应的离子方程式
(4)CuCl沉淀的洗涤需要经过酸洗、水洗和醇洗,水洗操作为
(5)得到CuCl沉淀要迅速真空干燥、冷却,密封包装。这样操作的目的是
(6)氯化亚铜在热水中迅速与水反应生成砖红色固体,写出该反应的化学方程式
您最近一年使用:0次



