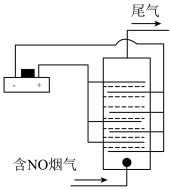
硝酸是重要的化工原料。如图是以合成氨为基础的传统硝酸生产工艺流程(其中空气等基础原料已略去)。_____________ (填序号)。
 .合成氨是一种重要的人工固氮方法
.合成氨是一种重要的人工固氮方法
 .该反应过程中氮元素被氧化
.该反应过程中氮元素被氧化
 .合成的氨气还可以用于化肥工业
.合成的氨气还可以用于化肥工业
 .该反应采用高温、高压等苛刻条件,与
.该反应采用高温、高压等苛刻条件,与 化学性质很稳定有关
化学性质很稳定有关
(2)氨氧化装置中,产生的含氮物质主要为 ,反应的化学方程式为
,反应的化学方程式为_________ 。
(3)聚合、吸收装置中,含氮物质转化的主要反应包括① ;②
;②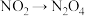 ;③
;③ ,其中属于氧化还原反应的是
,其中属于氧化还原反应的是_________ (填序号)。
(4)吸收装置中,发生的反应为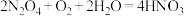 ,若用
,若用 稀硝酸作为吸收液,反应后得到
稀硝酸作为吸收液,反应后得到 的浓硝酸,则理论上吸收装置中需消耗的
的浓硝酸,则理论上吸收装置中需消耗的 的物质的量为
的物质的量为_________  (写出计算式)。
(写出计算式)。
(5)为实现制硝酸的绿色化改进,技术人员将①分离液态空气、②电解水等工艺整合在上述流程中。请在①、②中任选一种,说明该工艺的产物如何应用于硝酸生产流程:_____________ 。
(6) 催化还原氮氧化物
催化还原氮氧化物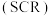 技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示:
技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示: 和
和 物质的量之比为
物质的量之比为 ,则总反应的化学方程式为
,则总反应的化学方程式为_________ 。
(7)据报道,意大利科学家获得了极具研究价值的 ,其分子结构如图所示。已知:Ⅰ.断裂
,其分子结构如图所示。已知:Ⅰ.断裂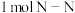 键吸收
键吸收 热量,形成
热量,形成 键放出
键放出 热量
热量
Ⅱ.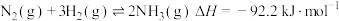
写出 和
和 反应合成
反应合成 的热化学方程式
的热化学方程式_____________________________ 。

 .合成氨是一种重要的人工固氮方法
.合成氨是一种重要的人工固氮方法 .该反应过程中氮元素被氧化
.该反应过程中氮元素被氧化 .合成的氨气还可以用于化肥工业
.合成的氨气还可以用于化肥工业 .该反应采用高温、高压等苛刻条件,与
.该反应采用高温、高压等苛刻条件,与 化学性质很稳定有关
化学性质很稳定有关(2)氨氧化装置中,产生的含氮物质主要为
 ,反应的化学方程式为
,反应的化学方程式为(3)聚合、吸收装置中,含氮物质转化的主要反应包括①
 ;②
;②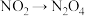 ;③
;③ ,其中属于氧化还原反应的是
,其中属于氧化还原反应的是(4)吸收装置中,发生的反应为
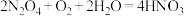 ,若用
,若用 稀硝酸作为吸收液,反应后得到
稀硝酸作为吸收液,反应后得到 的浓硝酸,则理论上吸收装置中需消耗的
的浓硝酸,则理论上吸收装置中需消耗的 的物质的量为
的物质的量为 (写出计算式)。
(写出计算式)。(5)为实现制硝酸的绿色化改进,技术人员将①分离液态空气、②电解水等工艺整合在上述流程中。请在①、②中任选一种,说明该工艺的产物如何应用于硝酸生产流程:
(6)
 催化还原氮氧化物
催化还原氮氧化物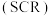 技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示:
技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示: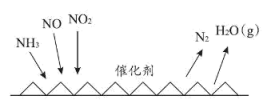
 和
和 物质的量之比为
物质的量之比为 ,则总反应的化学方程式为
,则总反应的化学方程式为(7)据报道,意大利科学家获得了极具研究价值的
 ,其分子结构如图所示。已知:Ⅰ.断裂
,其分子结构如图所示。已知:Ⅰ.断裂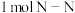 键吸收
键吸收 热量,形成
热量,形成 键放出
键放出 热量
热量Ⅱ.
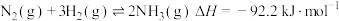
写出
 和
和 反应合成
反应合成 的热化学方程式
的热化学方程式
更新时间:2024-04-30 15:47:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)按如图所示操作,充分反应后:
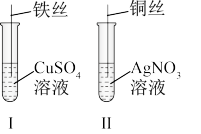
①Ⅰ中发生反应的离子方程式为_______ ;
②Ⅱ中铜丝上观察到的现象是_______ ;
③结合Ⅰ、Ⅱ实验现象可知 、
、 、
、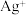 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(2)某一反应体系中有反应物和生成物共5种物质:S、 、
、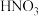 、NO、
、NO、 。该反应物中还原产物是
。该反应物中还原产物是_______ ;若反应方程式中转移了0.3mol电子,则氧化产物的质量是_______ 。
(3)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:_____
_______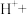 _______
_______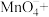 _______
_______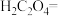 _______
_______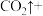 _______
_______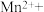 _______
_______
(1)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为
②Ⅱ中铜丝上观察到的现象是
③结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、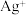 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(2)某一反应体系中有反应物和生成物共5种物质:S、
 、
、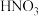 、NO、
、NO、 。该反应物中还原产物是
。该反应物中还原产物是(3)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:
_______
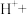 _______
_______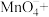 _______
_______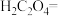 _______
_______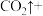 _______
_______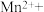 _______
_______
您最近一年使用:0次
【推荐2】氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)“维生素C可以将食物中的 转化为
转化为 ”,说明维生素C具有
”,说明维生素C具有_____ (填“氧化性”或“还原性”)。
(2) 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下:
_____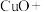 _____
_____
 _____
_____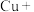 _____
_____ _____
_____ _____
_____
①配平上述氧化还原反应_____ 。
②该反应中,氧化剂是_____ (填化学式),被氧化的元素是_____ (填元素名称)。
(3)二氧化氯是一种高效消毒剂。工业上制备 的反应为
的反应为
①该反应中的还原产物是_____ (写化学式),反应中每生成1个 分子,转移电子的数目为
分子,转移电子的数目为_____ 。
②用双线桥标出反应中电子转移的方向和数目_____ 。
③ 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是_____ (填序号)
A. B.
B. C.KI D.
C.KI D.
(4)双氧水是公认的绿色氧化剂。已知氧化性强弱顺序为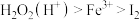 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为_____ 。
(1)“维生素C可以将食物中的
 转化为
转化为 ”,说明维生素C具有
”,说明维生素C具有(2)
 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下:_____
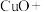 _____
_____
 _____
_____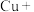 _____
_____ _____
_____ _____
_____
①配平上述氧化还原反应
②该反应中,氧化剂是
(3)二氧化氯是一种高效消毒剂。工业上制备
 的反应为
的反应为
①该反应中的还原产物是
 分子,转移电子的数目为
分子,转移电子的数目为②用双线桥标出反应中电子转移的方向和数目
③
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是A.
 B.
B. C.KI D.
C.KI D.
(4)双氧水是公认的绿色氧化剂。已知氧化性强弱顺序为
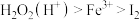 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)在反应 KMnO4+ HCl= MnCl2+ KCl+ Cl2↑+ H2O中,MnCl2为易溶于水的强电解质,回答下列问题:
①氧化剂是___________ ,还原剂是__________ ;
②配平上述方程式并用双线桥法标明电子转移的方向和数目:______________ ;
③写出上述反应的离子方程式:_________________________________________ ;
④若生成71gCl2,被氧化的HCl是_________________ g。
(2)单质铁与稀HNO3可发生多种反应,当8/3n(Fe)<n(HNO3)≤4n(Fe)时,反应方程式可用下列通式表示:aFe+bHNO3(稀)=cNO十dFe(NO3)2+eFe(NO3)3十fH2O。
①假设a=16,且b、c、d、e、f均取正整数时,共有_______ 组系数配比。
②若a、b、c、d、e、f符合上述系数的配比关系,则b与C的关系为:b=____ c。
①氧化剂是
②配平上述方程式并用双线桥法标明电子转移的方向和数目:
③写出上述反应的离子方程式:
④若生成71gCl2,被氧化的HCl是
(2)单质铁与稀HNO3可发生多种反应,当8/3n(Fe)<n(HNO3)≤4n(Fe)时,反应方程式可用下列通式表示:aFe+bHNO3(稀)=cNO十dFe(NO3)2+eFe(NO3)3十fH2O。
①假设a=16,且b、c、d、e、f均取正整数时,共有
②若a、b、c、d、e、f符合上述系数的配比关系,则b与C的关系为:b=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
I.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比 Cl2、O2、ClO2、KMnO4 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH 至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是_____ 。(填化学式)
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式_____ 。
②每生成1molFeO 转移
转移_____ 个电子。
(3) 是一种有毒气体,如果泄漏会造成严重的危害。已知
是一种有毒气体,如果泄漏会造成严重的危害。已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。反应中被氧化和未被氧化的
是否泄漏。反应中被氧化和未被氧化的 分子个数比为
分子个数比为_____ 。
Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质—碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为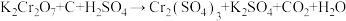 。
。
(4)配平该反应方程式:_____ 。
(5)此反应的氧化产物为_____ 。
(6)KMnO4在加热的条件下与硫酸酸化的Na2C2O4溶液反应,生成Mn2+和CO2,该反应的离子方程式为:_____ 。
(7)某条件下, 氧气所占的体积为
氧气所占的体积为 ,则在该条件下的气体摩尔体积为
,则在该条件下的气体摩尔体积为_____ 。
I.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比 Cl2、O2、ClO2、KMnO4 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH 至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式
②每生成1molFeO
 转移
转移(3)
 是一种有毒气体,如果泄漏会造成严重的危害。已知
是一种有毒气体,如果泄漏会造成严重的危害。已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。反应中被氧化和未被氧化的
是否泄漏。反应中被氧化和未被氧化的 分子个数比为
分子个数比为Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质—碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为
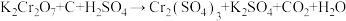 。
。(4)配平该反应方程式:
(5)此反应的氧化产物为
(6)KMnO4在加热的条件下与硫酸酸化的Na2C2O4溶液反应,生成Mn2+和CO2,该反应的离子方程式为:
(7)某条件下,
 氧气所占的体积为
氧气所占的体积为 ,则在该条件下的气体摩尔体积为
,则在该条件下的气体摩尔体积为
您最近一年使用:0次
【推荐2】医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:
( ) H++( ) MnO4-+( ) H2C2O4→( ) CO2↑+ ( ) Mn2++( ) ____
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是_____________ (填化学式)。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为_________ mol。
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是__________________________ 。
②溶解沉淀时______ (填“能”或“不能”)用稀盐酸,原因是________________ 。
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙_____ g。
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式_____________________ 。
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:______ 。
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是
②溶解沉淀时
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。
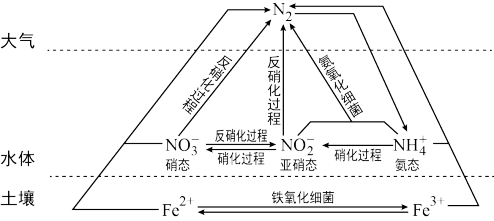
(1)如图所示氮循环中,属于氮的固定的有_____ (填字母序号)。
a.N2转化为氨态氮
b.硝化过程
c.反硝化过程
(2)氮肥是水体中 的主要来源之一,检验氮肥中
的主要来源之一,检验氮肥中 的实验方案是
的实验方案是_____ 。
(3)硝化过程中,含氮物质发生_____ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为_____ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理_____ 。

(1)如图所示氮循环中,属于氮的固定的有
a.N2转化为氨态氮
b.硝化过程
c.反硝化过程
(2)氮肥是水体中
 的主要来源之一,检验氮肥中
的主要来源之一,检验氮肥中 的实验方案是
的实验方案是(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出N2的电子式:__ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮,则下列属于固氮过程的是__ (填字母)。
A.NH3经过催化氧化生成NO
B.NH3和HNO3反应生成NH4NO3
C.N2和H2在一定条件下反应生成NH3
D.雷雨闪电时空气中的N2和O2化合生成NO
(3)如图是实验室制取氨气的装置和选用试剂,其中错误的是__ (填字母)。
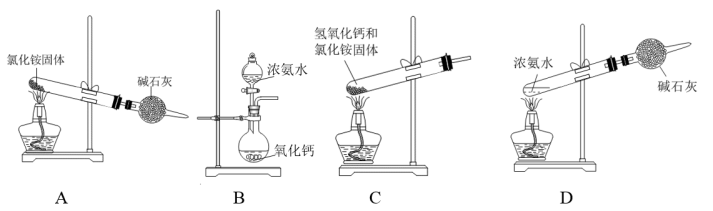
选取了正确的制备装置后,若想收集一试管氨气,可用___ 排空气法。
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放出氨气而降低肥效。检验其中 的方法是将固体溶于水配制浓溶液,加入浓
的方法是将固体溶于水配制浓溶液,加入浓__ 溶液、加热,再用__ 试纸检验产生的气体,若试纸变蓝则表明含有 。
。
(1)写出N2的电子式:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮,则下列属于固氮过程的是
A.NH3经过催化氧化生成NO
B.NH3和HNO3反应生成NH4NO3
C.N2和H2在一定条件下反应生成NH3
D.雷雨闪电时空气中的N2和O2化合生成NO
(3)如图是实验室制取氨气的装置和选用试剂,其中错误的是

选取了正确的制备装置后,若想收集一试管氨气,可用
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放出氨气而降低肥效。检验其中
 的方法是将固体溶于水配制浓溶液,加入浓
的方法是将固体溶于水配制浓溶液,加入浓 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮和氮的化合物与人类有密切关系,回答以下问题:
(1)氮是植物生长的必需元素。有关说法中错误的是_______。
(2)下列说法正确的是_______。
(3)甲、乙两组同学用干燥的圆底烧瓶各收集一瓶氨气,根据下图喷泉实验的装置进行实验都观察到美丽的红色喷泉。
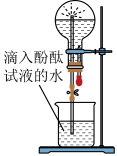
根据实验现象说明氨气具有的性质是_______ ,并用相应的方程式解释:_______ 。
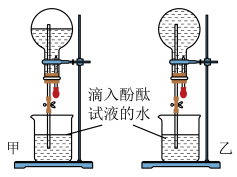
(4)甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图所示。请通过分析确认:甲组同学所得氨水的物质的量浓度_______ (填“大于”、“小于”或“等于”)乙组同学所得氨水的物质的量浓度。
(5)贮存铵态氮肥时要密封保存,并放在阴凉通风处,其原因是_______ 。写出 ”的检验方法:
”的检验方法:_______ 。
(1)氮是植物生长的必需元素。有关说法中错误的是_______。
| A.氮气分子很稳定 | B.尿素属于铵态氮肥 |
| C.工业合成氨是人工固氮 | D.闪电实现了大气固氮 |
| A.可用稀HNO3与FeS固体反应制取H2S |
| B.SO2能使酸性KMnO4、氯水褪色,说明SO2具有漂白作用 |
| C.少量NO2和足量SO2混合气体通入BaCl2溶液中,产生的沉淀只有BaSO4 |
D.向某溶液中滴加几滴盐酸酸化的BaCl2溶液,产生不溶于稀硝酸的白色沉淀则该溶液中一定含有 |

根据实验现象说明氨气具有的性质是
(4)甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图所示。请通过分析确认:甲组同学所得氨水的物质的量浓度

(5)贮存铵态氮肥时要密封保存,并放在阴凉通风处,其原因是
 ”的检验方法:
”的检验方法:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(2017·江苏如皋市高三调研)将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急。
(1)根据键能数据估算CH4+4F2=CF4+4HF的反应热ΔH=______________ 。
(2)甲醇、二甲醚(CH3OCH3)被称为21世纪的新型燃料,均可利用CO和H2反应合成。
某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:CH3OCH3+6 ‒12e‒=8CO2+3H2O。写出该燃料电池的正极反应式:
‒12e‒=8CO2+3H2O。写出该燃料电池的正极反应式:____________ 。
(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生的H2S废气。
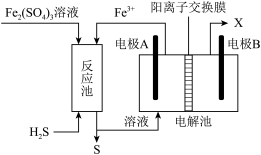
①电解池中电极A、B均为惰性电极,其中A为电解池的____________ 极;电极B所得到的物质X的分子式为_______________ 。
②反应池中发生的离子反应方程式为_______________ 。
(1)根据键能数据估算CH4+4F2=CF4+4HF的反应热ΔH=
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/(kJ·mol‒1) | 414 | 489 | 565 | 155 |
(2)甲醇、二甲醚(CH3OCH3)被称为21世纪的新型燃料,均可利用CO和H2反应合成。
某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:CH3OCH3+6
 ‒12e‒=8CO2+3H2O。写出该燃料电池的正极反应式:
‒12e‒=8CO2+3H2O。写出该燃料电池的正极反应式:(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生的H2S废气。

①电解池中电极A、B均为惰性电极,其中A为电解池的
②反应池中发生的离子反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】甲胺铅碘(CH3NH3PbI3)可用作全固态钙钛矿敏化太阳能电池的敏化剂,由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g) CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
则该反应的ΔH=________ kJ/mol。
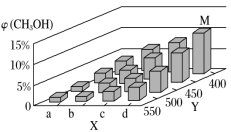
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为CO(g)+2H2(g) CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
①下列说法不能判断该反应达到化学平衡状态的是________ 。
A.体系中气体的密度保持不变
B.CO的消耗速率与CH3OH的消耗速率相等
C.体系中CO的转化率和H2的转化率相等
D.体系中CH3OH的体积分数保持不变
②平衡时,M点CH3OH的体积分数为10%,则CO的转化率为________ 。
③某同学认为上图中Y轴表示温度,你认为他判断的理由是______________________ 。
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,同时生成I2,写出发生的化学反应方程式__________________ 。
(4)HI的制备:将0.8molI2(g)和1.2molH2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) 2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:
2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:
①该反应的平衡常数K=_____________ 。
②反应达到平衡后,在7min时将容器体积压缩为原来的一半,请在图中画出c(HI)随时间变化的曲线_______________ 。

(1)制取甲胺的反应为CH3OH(g)+NH3(g)
 CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:| 共价键 | C—O | H—O | N—H | C—N |
| 键能/(kJ/mol) | 351.5 | 463 | 393 | 293 |
则该反应的ΔH=
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为CO(g)+2H2(g)
 CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
①下列说法不能判断该反应达到化学平衡状态的是
A.体系中气体的密度保持不变
B.CO的消耗速率与CH3OH的消耗速率相等
C.体系中CO的转化率和H2的转化率相等
D.体系中CH3OH的体积分数保持不变
②平衡时,M点CH3OH的体积分数为10%,则CO的转化率为
③某同学认为上图中Y轴表示温度,你认为他判断的理由是
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,同时生成I2,写出发生的化学反应方程式
(4)HI的制备:将0.8molI2(g)和1.2molH2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)
 2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:
2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| HI体积分数 | 26% | 42% | 52% | 57% | 60% | 60% | 60% |
①该反应的平衡常数K=
②反应达到平衡后,在7min时将容器体积压缩为原来的一半,请在图中画出c(HI)随时间变化的曲线

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求填空:
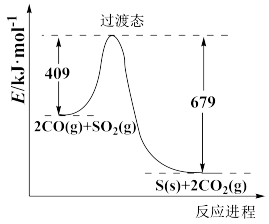
(1)对烟道气中的SO2进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下由SO2和CO反应生成S和CO2的能量变化如图所示,若反应中有48g S(s)生成,则该反应___________ (填“放出”或“吸收”)的热量为___________ 。
(2)汽车尾气中排放的NOx和CO污染环境,在汽车尾气中安装催化转化器,可有效降低NOx和CO的排放。已知:
a.2CO(g)+O2(g) 2CO2(g) ∆H=-566.0kJ·mol-1
2CO2(g) ∆H=-566.0kJ·mol-1
b.N2(g)+O2(g) 2NO(g) ∆H=+180.5kJ·mol-1
2NO(g) ∆H=+180.5kJ·mol-1
回答下列问题
①CO的燃烧热为___________ 。
②CO将NO还原为N2的热化学方程式为___________ 。
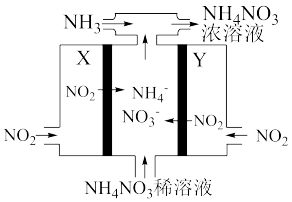
(3)电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。电解NO2制备NH4NO3原理如图所示。阳极为___________ (填“X”或“Y”),Y的电极反应式为___________ 。
(1)对烟道气中的SO2进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下由SO2和CO反应生成S和CO2的能量变化如图所示,若反应中有48g S(s)生成,则该反应

(2)汽车尾气中排放的NOx和CO污染环境,在汽车尾气中安装催化转化器,可有效降低NOx和CO的排放。已知:
a.2CO(g)+O2(g)
 2CO2(g) ∆H=-566.0kJ·mol-1
2CO2(g) ∆H=-566.0kJ·mol-1b.N2(g)+O2(g)
 2NO(g) ∆H=+180.5kJ·mol-1
2NO(g) ∆H=+180.5kJ·mol-1回答下列问题
①CO的燃烧热为
②CO将NO还原为N2的热化学方程式为
(3)电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。电解NO2制备NH4NO3原理如图所示。阳极为

您最近一年使用:0次

 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的原理为