乙烯、丙烯是石油产业的核心,工业上可利用甲醇制备乙烯、丙烯,所涉及的反应如下:
主反应: ;
;
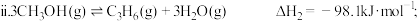
副反应: 。
。
回答下列问题:
(1)已知相关化学键的键能数据如下:

_______  。
。
(2)下列关于反应 的说法正确的是_______(填字母)。
的说法正确的是_______(填字母)。
(3)T℃时,在压强恒定的相同容器中填装催化剂,以恒定的流速通入 ,测得甲醇的转化率与乙烯和丙烯的选择性(选择性:转化的甲醇中生成乙烯和丙烯的百分比)与反应时间的关系如图所示。
,测得甲醇的转化率与乙烯和丙烯的选择性(选择性:转化的甲醇中生成乙烯和丙烯的百分比)与反应时间的关系如图所示。_______ 。
②3h后乙烯和丙烯的选择性均明显下降,可能的原因是_______ 。
(4)只研究温度对反应的影响,向压强恒定为 的密闭容器中通入
的密闭容器中通入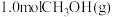 只发生反应
只发生反应 和
和 ,经过相同时间
,经过相同时间 ,乙烯和丙烯的物质的量随温度的变化如图所示。
,乙烯和丙烯的物质的量随温度的变化如图所示。 前,乙烯和丙烯的物质的量随温度升高逐渐增大的原因为
前,乙烯和丙烯的物质的量随温度升高逐渐增大的原因为_______ 。
② 时,
时, 的平衡转化率为
的平衡转化率为_______ 。
③ 时,反应
时,反应 的平衡常数
的平衡常数
_______  (列出计算式即可,用平衡分压代替平衡浓度计算,分压=总压
(列出计算式即可,用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。
(5)若反应ⅲ的速率方程为 ,其中
,其中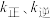 分别表示正、逆反应速率常数,只与温度有关。如图为反应ⅲ的速率常数的对数
分别表示正、逆反应速率常数,只与温度有关。如图为反应ⅲ的速率常数的对数 与温度的倒数
与温度的倒数 之间的关系,则
之间的关系,则 时,反应ⅲ的化学平衡常数
时,反应ⅲ的化学平衡常数
_______ 。
主反应:
 ;
;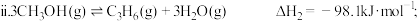
副反应:
 。
。回答下列问题:
(1)已知相关化学键的键能数据如下:
| 化学键 | C-H | C-O | C=C | O-H |
键能 | 413 | 351 | 615 | 463 |

 。
。(2)下列关于反应
 的说法正确的是_______(填字母)。
的说法正确的是_______(填字母)。| A.主反应均为熵增反应 |
| B.乙烯和丙烯的体积分数相等,说明体系达到了平衡状态 |
| C.及时将水蒸气液化并分离,有利于提高甲醇的平衡转化率 |
| D.其他条件相同,反应i分别在恒容和恒压条件下进行,前者甲醇的平衡转化率更高 |
(3)T℃时,在压强恒定的相同容器中填装催化剂,以恒定的流速通入
 ,测得甲醇的转化率与乙烯和丙烯的选择性(选择性:转化的甲醇中生成乙烯和丙烯的百分比)与反应时间的关系如图所示。
,测得甲醇的转化率与乙烯和丙烯的选择性(选择性:转化的甲醇中生成乙烯和丙烯的百分比)与反应时间的关系如图所示。
②3h后乙烯和丙烯的选择性均明显下降,可能的原因是
(4)只研究温度对反应的影响,向压强恒定为
 的密闭容器中通入
的密闭容器中通入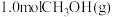 只发生反应
只发生反应 和
和 ,经过相同时间
,经过相同时间 ,乙烯和丙烯的物质的量随温度的变化如图所示。
,乙烯和丙烯的物质的量随温度的变化如图所示。
 前,乙烯和丙烯的物质的量随温度升高逐渐增大的原因为
前,乙烯和丙烯的物质的量随温度升高逐渐增大的原因为②
 时,
时, 的平衡转化率为
的平衡转化率为③
 时,反应
时,反应 的平衡常数
的平衡常数
 (列出计算式即可,用平衡分压代替平衡浓度计算,分压=总压
(列出计算式即可,用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。(5)若反应ⅲ的速率方程为
 ,其中
,其中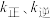 分别表示正、逆反应速率常数,只与温度有关。如图为反应ⅲ的速率常数的对数
分别表示正、逆反应速率常数,只与温度有关。如图为反应ⅲ的速率常数的对数 与温度的倒数
与温度的倒数 之间的关系,则
之间的关系,则 时,反应ⅲ的化学平衡常数
时,反应ⅲ的化学平衡常数

更新时间:2024-06-03 22:26:14
|
相似题推荐
【推荐1】I. 依据事实写出下列反应的热化学方程式。
① 在25℃、101kPa下,1g甲醇CH3OH燃烧生成CO2和液态水时放热22.68kJ。
则表示甲醇燃烧热的热化学方程式为__________________ 。
② 若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量_____________ 。
II. 盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式
①Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8 kJ.mol -1
②3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2 kJ.mol -1
③Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5 kJ.mol -1
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式________________ 。
III.已知反应 2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、 1molI2(g)分子中化学键断裂时分别需要吸收 436KJ、151KJ 的能量,则 1molHI(g)分子中化学键断裂时需吸收的能量为______________ kJ。
① 在25℃、101kPa下,1g甲醇CH3OH燃烧生成CO2和液态水时放热22.68kJ。
则表示甲醇燃烧热的热化学方程式为
② 若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量
II. 盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式
①Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8 kJ.mol -1
②3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2 kJ.mol -1
③Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5 kJ.mol -1
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式
III.已知反应 2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、 1molI2(g)分子中化学键断裂时分别需要吸收 436KJ、151KJ 的能量,则 1molHI(g)分子中化学键断裂时需吸收的能量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】断开1molAB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称A-B键的键能E:

请回答下列问题:
Ⅰ.(1)如图表示某反应的能量变化关系,则此反应为_________ (填“吸热”或“放热”)反应,其中△H=_________ (用含有a、b的关系式表示)
(2)若图中表示反应H2(g)+ O2(g)=H2O(g) △H=-241.8 kJ·mol-1,x=
O2(g)=H2O(g) △H=-241.8 kJ·mol-1,x=______________ ;若忽略温度和压强对反应热的影响,当反应中有1 mol电子转移时,反应的热量变化为______________
(3)处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知:CO(g)+ O 2(g)=CO2(g) ∆H=- 283.0 kJ·mol-1
O 2(g)=CO2(g) ∆H=- 283.0 kJ·mol-1
S(s)+O2(g)=SO2 (g) ∆H=-296.0 kJ·mol-1
写出CO和SO2转化为单质硫的反应热化学方程式是_____________________ 。
Ⅱ.将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=_____________________ mol/L
(2)前5 min内用B表示的平均反应速率v(B)=_____________________ mol/(L·min);
(3)化学反应方程式中x的值为_____________________ 。
| 化学键 | H‒H | Cl‒Cl | O=O | C‒Cl | C‒H | O‒H | H‒Cl |
| E/kJ·mol-1 | 436 | 247 | x | 330 | 413 | 463 | 431 |

请回答下列问题:
Ⅰ.(1)如图表示某反应的能量变化关系,则此反应为
(2)若图中表示反应H2(g)+
 O2(g)=H2O(g) △H=-241.8 kJ·mol-1,x=
O2(g)=H2O(g) △H=-241.8 kJ·mol-1,x=(3)处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知:CO(g)+
 O 2(g)=CO2(g) ∆H=- 283.0 kJ·mol-1
O 2(g)=CO2(g) ∆H=- 283.0 kJ·mol-1S(s)+O2(g)=SO2 (g) ∆H=-296.0 kJ·mol-1
写出CO和SO2转化为单质硫的反应热化学方程式是
Ⅱ.将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=
(2)前5 min内用B表示的平均反应速率v(B)=
(3)化学反应方程式中x的值为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】雾霾严重危害人类健康和生态环境,开发稳定高效的脱硫脱硝工艺是当前国内外研究的热点。
(1)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
请写出该条件下反应的热化学方程式:_______ 。
(2)已知物质的氧化性或还原性强弱与溶液的pH有关。利用 NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝,将NO、SO2氧化为硝酸和硫酸而除去。在温度一定时, 、溶液pH对脱硫脱硝的影响如图所示:
、溶液pH对脱硫脱硝的影响如图所示:
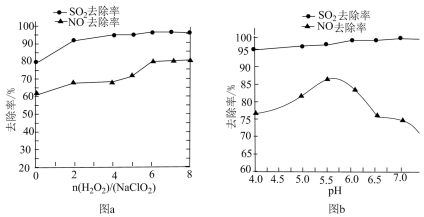
①从图a和图b中可知脱硫脱硝最佳 是
是_______ 、最佳pH是_______ 。
②图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因_______ 。
(3)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g) N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
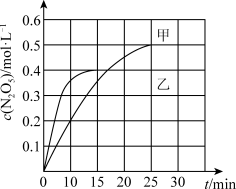
0~10 min内甲容器中反应的平均速率:v(NO2)=_______ mol·L-1·min-1
(1)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
| 化学键 | H-S | O=O | H-O | SO2中共价键 |
| 键能/(kJ▪mol-1) | 339 | 498 | 464 | 1083 |
请写出该条件下反应的热化学方程式:
(2)已知物质的氧化性或还原性强弱与溶液的pH有关。利用 NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝,将NO、SO2氧化为硝酸和硫酸而除去。在温度一定时,
 、溶液pH对脱硫脱硝的影响如图所示:
、溶液pH对脱硫脱硝的影响如图所示:
①从图a和图b中可知脱硫脱硝最佳
 是
是②图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因
(3)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g)
 N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
0~10 min内甲容器中反应的平均速率:v(NO2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】NO、NO2是大气污染物,但只要合理利用,NO、NO2也是重要的资源。回答下列问题:
(1)氨的合成。已知:N2和H2生成NH3的反应为: N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g) ΔH=-46.2kJ·mol-1
NH3(g) ΔH=-46.2kJ·mol-1
在Fe催化剂作用下的反应历程为(※表示吸附态):
化学吸附:N2(g)→2N※;H2(g) 2H※;
2H※;
表面反应:N※+H※ NH※;NH※+H※
NH※;NH※+H※ NH2※;NH2※+H※
NH2※;NH2※+H※ NH3※;
NH3※;
脱附:NH3※ NH3(g)
NH3(g)
其中N2的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。则利于提高合成氨平衡产率的条件有( )
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)NH3还原法可将NO还原为N2进行脱除。已知:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-1530kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol-1
写出NH3还原NO的热化学方程式__ 。
(3)亚硝酰氯(ClNO)是合成有机物的中间体。将一定量的NO与Cl2充入一密闭容器中,发生反应:2NO(g)+Cl2(g) 2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是
2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是__ (填字母代号)。

a.温度 b.压强 c.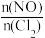 d.与催化剂的接触面积
d.与催化剂的接触面积
(4)在密闭容器中充入4molCO和5molNO发生反应2NO(g)+2CO(g) N2(g)+2CO2(g) △H=-746.5kJ•mol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。
N2(g)+2CO2(g) △H=-746.5kJ•mol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。
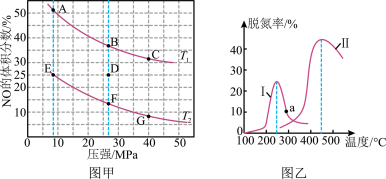
①温度T1__ T2(填“>”或“<”)。
②若反应在D点达到平衡,此时对反应进行升温且同时扩大容器体积使平衡压强减小,则重新达到平衡时,D点应向图中A~G点中的__ 点移动。
③探究催化剂对CO、NO转化的影响。某研究小组将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如图乙所示。温度低于200℃时,图中曲线I脱氮率随温度升高而变化不大的主要原因为__ ;a点__ (填“是”或“不是”)对应温度下的平衡脱氮率,说明其理由__ 。
(1)氨的合成。已知:N2和H2生成NH3的反应为:
 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g) ΔH=-46.2kJ·mol-1
NH3(g) ΔH=-46.2kJ·mol-1在Fe催化剂作用下的反应历程为(※表示吸附态):
化学吸附:N2(g)→2N※;H2(g)
 2H※;
2H※;表面反应:N※+H※
 NH※;NH※+H※
NH※;NH※+H※ NH2※;NH2※+H※
NH2※;NH2※+H※ NH3※;
NH3※;脱附:NH3※
 NH3(g)
NH3(g)其中N2的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。则利于提高合成氨平衡产率的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)NH3还原法可将NO还原为N2进行脱除。已知:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-1530kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol-1
写出NH3还原NO的热化学方程式
(3)亚硝酰氯(ClNO)是合成有机物的中间体。将一定量的NO与Cl2充入一密闭容器中,发生反应:2NO(g)+Cl2(g)
 2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是
2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是
a.温度 b.压强 c.
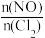 d.与催化剂的接触面积
d.与催化剂的接触面积(4)在密闭容器中充入4molCO和5molNO发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H=-746.5kJ•mol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。
N2(g)+2CO2(g) △H=-746.5kJ•mol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。
①温度T1
②若反应在D点达到平衡,此时对反应进行升温且同时扩大容器体积使平衡压强减小,则重新达到平衡时,D点应向图中A~G点中的
③探究催化剂对CO、NO转化的影响。某研究小组将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如图乙所示。温度低于200℃时,图中曲线I脱氮率随温度升高而变化不大的主要原因为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】根据要求回答下列有关问题。
(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ∆H=-28.5kJ/mol
2Fe(s)+3CO2(g) ∆H=-28.5kJ/mol
冶炼铁反应的平衡常数表达式K=____________ ,温度升高后,K 值________ (填“增大”、“不变”或“减小”)。
(2)已知:①Fe2O3(s)+3C(石墨)2Fe(s)+3CO(g) ∆H1=+489.0kJ/mol
②Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ∆H2=-28.5kJ/mol
2Fe(s)+3CO2(g) ∆H2=-28.5kJ/mol
③C(石墨)+ CO2(g)=2CO(g) ∆H3=akJ/mol
则a=__________ kJ/mol。
(3)在T℃时,反应Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知
2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知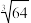 =4)
=4)
①平衡时CO 的转化率为___________ 。
②下列情况标志反应达到平衡状态正确的是________ (填字母)。
a.容器内气体密度保持不变
b.容器内气体压强保持不变
c.CO的消耗速率和CO2的生成速率相等
(4)一定条件下发生反应:N2(g)+ 3H2(g) 2NH3(g)∆H<0。
2NH3(g)∆H<0。
① 在某温度时,向容积固定的容器中加入1mol N2和3mol H2,达到平衡后:
a.若向容器中通入N2,则N2的转化率将___________ (填“增大”、“减小”或“不变”,下同)。
b.若再通入1mol N2和3mol H2,氮气的转化率将________ 。
②三个相同的容器中各充入1molN2和3molH2,在不同条件下分别达到平衡,氨气的体积分数随时间变化如图,下列说法正确的是___________ 。

a.图Ⅰ可能是不同温度对反应的影响,且T1>T2
b.图Ⅱ可能是同温同压下有无催化剂, 1表示没加入催化剂, 2表示加入了催化剂
c.图Ⅲ可能是不同压强对反应的影响,且p1>p2
(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g) ∆H=-28.5kJ/mol
2Fe(s)+3CO2(g) ∆H=-28.5kJ/mol冶炼铁反应的平衡常数表达式K=
(2)已知:①Fe2O3(s)+3C(石墨)2Fe(s)+3CO(g) ∆H1=+489.0kJ/mol
②Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g) ∆H2=-28.5kJ/mol
2Fe(s)+3CO2(g) ∆H2=-28.5kJ/mol③C(石墨)+ CO2(g)=2CO(g) ∆H3=akJ/mol
则a=
(3)在T℃时,反应Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知
2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知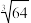 =4)
=4)| Fe2O3 | CO | Fe | CO2 | |
| 始态mol | 1.0 | 1.0 | 1.0 | 1.0 |
①平衡时CO 的转化率为
②下列情况标志反应达到平衡状态正确的是
a.容器内气体密度保持不变
b.容器内气体压强保持不变
c.CO的消耗速率和CO2的生成速率相等
(4)一定条件下发生反应:N2(g)+ 3H2(g)
 2NH3(g)∆H<0。
2NH3(g)∆H<0。① 在某温度时,向容积固定的容器中加入1mol N2和3mol H2,达到平衡后:
a.若向容器中通入N2,则N2的转化率将
b.若再通入1mol N2和3mol H2,氮气的转化率将
②三个相同的容器中各充入1molN2和3molH2,在不同条件下分别达到平衡,氨气的体积分数随时间变化如图,下列说法正确的是

a.图Ⅰ可能是不同温度对反应的影响,且T1>T2
b.图Ⅱ可能是同温同压下有无催化剂, 1表示没加入催化剂, 2表示加入了催化剂
c.图Ⅲ可能是不同压强对反应的影响,且p1>p2
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】工业上利用C2H2制取C2H4的反应为C2H2(g)+H2(g) C2H4(g) △H。回答下列问题:
C2H4(g) △H。回答下列问题:
(1)H2可通过反应CH4(g)+H2O(g) CO(g)+3H2(g)获取。T℃时,向2L恒容密闭容器中充入1.2mol水蒸气和1.2molCH4(g),经过2min反应达平衡,平衡后测得CO的浓度为0.3mol•L-1,则0~2min内H2的平均反应速率为
CO(g)+3H2(g)获取。T℃时,向2L恒容密闭容器中充入1.2mol水蒸气和1.2molCH4(g),经过2min反应达平衡,平衡后测得CO的浓度为0.3mol•L-1,则0~2min内H2的平均反应速率为______ ,平衡时CH4的转化率为______ 。
(2)对于反应C2H2(g)+H2(g) C2H4(g),其他条件一定时,温度、压强对平衡时混合气体中C2H4体积分数的影响如图所示。
C2H4(g),其他条件一定时,温度、压强对平衡时混合气体中C2H4体积分数的影响如图所示。
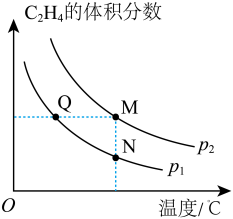
①该反应为______ 反应(填“吸热”或“放热”),压强:p1______ p2(填“>”“=”或“<”)。
②Q、M、N三点的平衡常数KQ、KM、KN的大小关系为______ 。
(3)对于反应C2H2(g)+H2(g) C2H4(g),为了增大反应速率,且增大H2的平衡转化率,下列措施一定可行的是
C2H4(g),为了增大反应速率,且增大H2的平衡转化率,下列措施一定可行的是_____ (填字母)。
a.降低温度 b.使用合适的催化剂
c.缩小容器容积 d.减小原料气中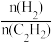 的比值
的比值
 C2H4(g) △H。回答下列问题:
C2H4(g) △H。回答下列问题:(1)H2可通过反应CH4(g)+H2O(g)
 CO(g)+3H2(g)获取。T℃时,向2L恒容密闭容器中充入1.2mol水蒸气和1.2molCH4(g),经过2min反应达平衡,平衡后测得CO的浓度为0.3mol•L-1,则0~2min内H2的平均反应速率为
CO(g)+3H2(g)获取。T℃时,向2L恒容密闭容器中充入1.2mol水蒸气和1.2molCH4(g),经过2min反应达平衡,平衡后测得CO的浓度为0.3mol•L-1,则0~2min内H2的平均反应速率为(2)对于反应C2H2(g)+H2(g)
 C2H4(g),其他条件一定时,温度、压强对平衡时混合气体中C2H4体积分数的影响如图所示。
C2H4(g),其他条件一定时,温度、压强对平衡时混合气体中C2H4体积分数的影响如图所示。
①该反应为
②Q、M、N三点的平衡常数KQ、KM、KN的大小关系为
(3)对于反应C2H2(g)+H2(g)
 C2H4(g),为了增大反应速率,且增大H2的平衡转化率,下列措施一定可行的是
C2H4(g),为了增大反应速率,且增大H2的平衡转化率,下列措施一定可行的是a.降低温度 b.使用合适的催化剂
c.缩小容器容积 d.减小原料气中
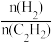 的比值
的比值
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】大气污染越来越成为人们关注的问题,烟气中的NOx必须脱除(即脱硝)后才能排放。臭氧是理想的烟气脱硝剂,其脱硝反应之一为:NO(g)+O3(g)  NO2(g)+O2(g) ∆H=−200.9 kJ∙mol−1
NO2(g)+O2(g) ∆H=−200.9 kJ∙mol−1
(1)若NO(g)+ O2(g) =NO2(g) ∆H= −58.2 kJ·mol-1,则反应3NO(g)+O3(g)=3NO2(g)的∆H=
O2(g) =NO2(g) ∆H= −58.2 kJ·mol-1,则反应3NO(g)+O3(g)=3NO2(g)的∆H=_______ kJ∙mol−1。
(2)对于反应NO(g)+O3(g) NO2(g)+O2(g),在不同温度下,分别向10L的恒容密闭容器中按1:1充入一定量的NO和O3发生反应,其中NO的物质的量随时间变化如图所示:
NO2(g)+O2(g),在不同温度下,分别向10L的恒容密闭容器中按1:1充入一定量的NO和O3发生反应,其中NO的物质的量随时间变化如图所示:_______ 。
②图中T1_______ T2(填“>”“<”或“=”)。
③温度为T1时,用NO表示t1~t2s内该反应的平均速率为_______ ,该反应的平衡常数K为_______ ,若NO的起始投入量为3a mol,则达到平衡时NO的残留量为_______ mol。
(3) NH3催化还原NO是重要的烟气脱硝技术,研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图。脱硝过程的总反应的化学方程式为_______ 。
 NO2(g)+O2(g) ∆H=−200.9 kJ∙mol−1
NO2(g)+O2(g) ∆H=−200.9 kJ∙mol−1(1)若NO(g)+
 O2(g) =NO2(g) ∆H= −58.2 kJ·mol-1,则反应3NO(g)+O3(g)=3NO2(g)的∆H=
O2(g) =NO2(g) ∆H= −58.2 kJ·mol-1,则反应3NO(g)+O3(g)=3NO2(g)的∆H=(2)对于反应NO(g)+O3(g)
 NO2(g)+O2(g),在不同温度下,分别向10L的恒容密闭容器中按1:1充入一定量的NO和O3发生反应,其中NO的物质的量随时间变化如图所示:
NO2(g)+O2(g),在不同温度下,分别向10L的恒容密闭容器中按1:1充入一定量的NO和O3发生反应,其中NO的物质的量随时间变化如图所示:
②图中T1
③温度为T1时,用NO表示t1~t2s内该反应的平均速率为
(3) NH3催化还原NO是重要的烟气脱硝技术,研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图。脱硝过程的总反应的化学方程式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】碳循环对地球的生态环境有着极其重要的影响,二氧化碳的过度排放会造成温室效应,引发气候、环境问题,有效利用二氧化碳则会造福人类。合成尿素是二氧化碳在工业上的重要应用,存在多种工艺。以CO2和NH3为原料,用水溶液全循环法合成尿素的反应过程为:
反应I:CO2(g)+2NH3(l) NH2COONH4(l) ΔH1=-117.2kJ/mol
NH2COONH4(l) ΔH1=-117.2kJ/mol
反应II:NH2COONH4(l) CO(NH2)2(l)+H2O(1) ΔH2=+21.7kJ/mol
CO(NH2)2(l)+H2O(1) ΔH2=+21.7kJ/mol
(1)已知:NH3(l) NH3(g) ΔH3=ckJ·mol-1。火电厂烟气脱硝所使用的还原剂氨气主要来自于尿素水解,则反应NH2CONH2(l)+H2O(l)
NH3(g) ΔH3=ckJ·mol-1。火电厂烟气脱硝所使用的还原剂氨气主要来自于尿素水解,则反应NH2CONH2(l)+H2O(l) 2NH3(g)+CO2(g)的ΔH4=
2NH3(g)+CO2(g)的ΔH4=_______ kJ/mol(用含c的式子表示),该反应能在常温下缓慢发生的主要原因是_______ 。
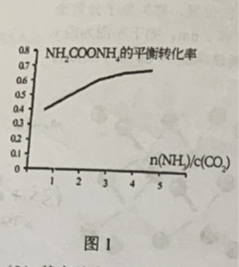
(2)一定条件下,n(NH3)/n(CO2)对NH2COONH4的平衡转化率会产生明显的影响,如图1所示。NH2COONH4的平衡转化率随n(NH3)/n(CO2)增大而上升,试分析其原因:_______ 。
(3)某实验小组模拟工业上合成尿素的条件,在体积为0.5L密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图2所示:
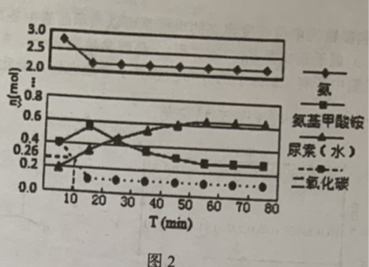
①反应进行到10min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)=_______ 。
②请绘制尿素的总反应,即“CO2(g)+2NH3(1)→NH2COONH4(l)→CO(NH2)2(l)+H2O(1)”的“能量~反应过程”示意图_______ 。
(4)该实验小组调查研究了化肥厂合成氨气的装置发现,反应I在氨基甲酸铵冷凝器中进行,条件是140°C和14MPa,反应II在尿素合成塔中进行,条件是185°C和13.6Mpa.请分析尿素合成塔中进行反应II需要高温高压的原因_______ 。
(5)另一实验小组模拟热气循环法合成尿素,T°C时,将5.6molNH3与5.2molCO2在容积恒定为0.5L的恒温密闭容器中发生反应:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ΔH1=-43kJ·mol-1。达到平衡状态时,NH3与CO2的平衡分压之比p(NH3):p(CO2)=2:13。[p(NH3)=x(NH3)·p,x(NH3)为平衡体系中NH3的物质的量分数,p为平衡总压]。
CO(NH2)2(s)+H2O(g) ΔH1=-43kJ·mol-1。达到平衡状态时,NH3与CO2的平衡分压之比p(NH3):p(CO2)=2:13。[p(NH3)=x(NH3)·p,x(NH3)为平衡体系中NH3的物质的量分数,p为平衡总压]。
①T°C时,该反应的平衡常数K=_______ 。
②若不考虑副反应,对于该反应体系,下列说法不正确的是_______ 。
A.当反应体系中气体分子的平均摩尔质量保持不变时,反应达到平衡状态
B.相同条件下,提高水碳比或降低氨碳比都会使NH3的平衡转化率降低
C.在容器中加入CaO,可与H2O反应,从而提高CO(NH2)2产率
D.反应开始后的一段时间内,适当升温可提高单位时间内CO2的转化率
反应I:CO2(g)+2NH3(l)
 NH2COONH4(l) ΔH1=-117.2kJ/mol
NH2COONH4(l) ΔH1=-117.2kJ/mol反应II:NH2COONH4(l)
 CO(NH2)2(l)+H2O(1) ΔH2=+21.7kJ/mol
CO(NH2)2(l)+H2O(1) ΔH2=+21.7kJ/mol(1)已知:NH3(l)
 NH3(g) ΔH3=ckJ·mol-1。火电厂烟气脱硝所使用的还原剂氨气主要来自于尿素水解,则反应NH2CONH2(l)+H2O(l)
NH3(g) ΔH3=ckJ·mol-1。火电厂烟气脱硝所使用的还原剂氨气主要来自于尿素水解,则反应NH2CONH2(l)+H2O(l) 2NH3(g)+CO2(g)的ΔH4=
2NH3(g)+CO2(g)的ΔH4=(2)一定条件下,n(NH3)/n(CO2)对NH2COONH4的平衡转化率会产生明显的影响,如图1所示。NH2COONH4的平衡转化率随n(NH3)/n(CO2)增大而上升,试分析其原因:

(3)某实验小组模拟工业上合成尿素的条件,在体积为0.5L密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图2所示:

①反应进行到10min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)=
②请绘制尿素的总反应,即“CO2(g)+2NH3(1)→NH2COONH4(l)→CO(NH2)2(l)+H2O(1)”的“能量~反应过程”示意图

(4)该实验小组调查研究了化肥厂合成氨气的装置发现,反应I在氨基甲酸铵冷凝器中进行,条件是140°C和14MPa,反应II在尿素合成塔中进行,条件是185°C和13.6Mpa.请分析尿素合成塔中进行反应II需要高温高压的原因
(5)另一实验小组模拟热气循环法合成尿素,T°C时,将5.6molNH3与5.2molCO2在容积恒定为0.5L的恒温密闭容器中发生反应:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ΔH1=-43kJ·mol-1。达到平衡状态时,NH3与CO2的平衡分压之比p(NH3):p(CO2)=2:13。[p(NH3)=x(NH3)·p,x(NH3)为平衡体系中NH3的物质的量分数,p为平衡总压]。
CO(NH2)2(s)+H2O(g) ΔH1=-43kJ·mol-1。达到平衡状态时,NH3与CO2的平衡分压之比p(NH3):p(CO2)=2:13。[p(NH3)=x(NH3)·p,x(NH3)为平衡体系中NH3的物质的量分数,p为平衡总压]。①T°C时,该反应的平衡常数K=
②若不考虑副反应,对于该反应体系,下列说法不正确的是
A.当反应体系中气体分子的平均摩尔质量保持不变时,反应达到平衡状态
B.相同条件下,提高水碳比或降低氨碳比都会使NH3的平衡转化率降低
C.在容器中加入CaO,可与H2O反应,从而提高CO(NH2)2产率
D.反应开始后的一段时间内,适当升温可提高单位时间内CO2的转化率
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】硫一碘循环分解水制氢主要涉及下列反应:
Ⅰ.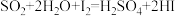
Ⅱ.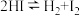
Ⅲ.
(1)分析上述反应,下列判断正确的是___________ 。
a.反应Ⅲ易在常温下进行 b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O d.循环过程产生1 mol O2的同时产生1 molH2
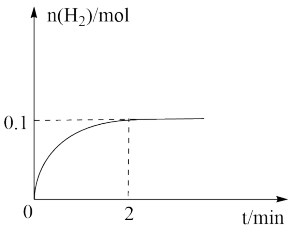
(2)一定温度下,向1L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。该温度下, 的平衡常数K=
的平衡常数K=___________ 。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则平衡后,_________ 是原来的2倍。
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡___________ 移动(填“向左”“向右”或“不”);若加入少量下列试剂中的___________ ,产生 的速率将增大。
的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(4)以H2为燃料可制作氢氧燃料电池。已知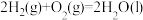
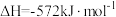 某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为
某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为___________ 。
Ⅰ.
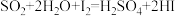
Ⅱ.
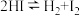
Ⅲ.

(1)分析上述反应,下列判断正确的是
a.反应Ⅲ易在常温下进行 b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O d.循环过程产生1 mol O2的同时产生1 molH2
(2)一定温度下,向1L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。该温度下,
 的平衡常数K=
的平衡常数K=
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡
 的速率将增大。
的速率将增大。a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(4)以H2为燃料可制作氢氧燃料电池。已知
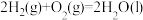
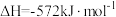 某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为
某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】I.实验室中有一未知浓度的稀盐酸,某学生测定盐酸的浓度在实验室中进行实验。请完成下列填空:
(1)配制400mL0.10mol/LNaOH标准溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、___________ 。
(2)取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
①量取待测溶液时,应用下图中的___________ (填“甲”或“乙”)量取。

②滴定达到终点的标志是___________ 。
③根据上述数据,可计算出该盐酸的浓度约为___________ (保留两位有效数字)。
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有,___________ 。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.碱式滴定管尖嘴部分有气泡,滴定后消失
II.某温度(T)下的溶液中,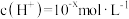 ,
,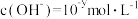 ,x与y的关系如图所示,请回答下列问题:
,x与y的关系如图所示,请回答下列问题:
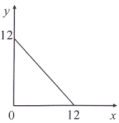
(3)此温度下,水的离子积Kw为______ ,则该温度T________ 25℃(填“>”“<”或“=”)。
(4)在此温度下,向 溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示:
溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示:
假设溶液混合前后的体积变化忽略不计,则a=______ ,实验②中由水电离产生的
___________  。
。
(5)在此温度下,将0.1 的
的 溶液与0.1
溶液与0.1 的
的 溶液按下表中甲、乙、丙、丁四种不同方式混合:
溶液按下表中甲、乙、丙、丁四种不同方式混合:
①按丁方式混合后,所得溶液显___________ (填“酸”“碱”或“中”)性。
②写出按乙方式混合反应的离子方程式:___________ 。
③按甲方式混合后所得溶液的pH为___________ 。
III.
(6)催化剂在一定条件下可直接光催化分解 ,发生反应:
,发生反应: ,该反应的
,该反应的
______ (填“>”或“<”,下同)0,
______ 0,在低温下,该反应_______ (填“能”或“不能”)自发进行。
(7)已知在100kPa、298K时石灰石分解反应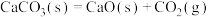 的△H>0、△S>0。
的△H>0、△S>0。
①常温下,该反应___________ (填“能”或“不能”自发进行。
②据本题反应数据分析温度___________ (填“能”或“不能”)成为反应进行方向的决定因素。
(1)配制400mL0.10mol/LNaOH标准溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、
(2)取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
| 实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 24.02 | 20.00 |
| 2 | 0.10 | 24.18 | 20.00 |
| 3 | 0.10 | 24.10 | 20.00 |

②滴定达到终点的标志是
③根据上述数据,可计算出该盐酸的浓度约为
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有,
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.碱式滴定管尖嘴部分有气泡,滴定后消失
II.某温度(T)下的溶液中,
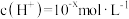 ,
,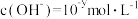 ,x与y的关系如图所示,请回答下列问题:
,x与y的关系如图所示,请回答下列问题:
(3)此温度下,水的离子积Kw为
(4)在此温度下,向
 溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示:
溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示:| 实验序号 |  溶液的体积/mL 溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |

 。
。(5)在此温度下,将0.1
 的
的 溶液与0.1
溶液与0.1 的
的 溶液按下表中甲、乙、丙、丁四种不同方式混合:
溶液按下表中甲、乙、丙、丁四种不同方式混合:| 甲 | 乙 | 丙 | 丁 | |
0.1  溶液体积/mL 溶液体积/mL | 10 | 10 | 10 | 10 |
0.1  溶液体积/mL 溶液体积/mL | 5 | 10 | 15 | 20 |
②写出按乙方式混合反应的离子方程式:
③按甲方式混合后所得溶液的pH为
III.
(6)催化剂在一定条件下可直接光催化分解
 ,发生反应:
,发生反应: ,该反应的
,该反应的

(7)已知在100kPa、298K时石灰石分解反应
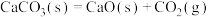 的△H>0、△S>0。
的△H>0、△S>0。①常温下,该反应
②据本题反应数据分析温度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】用尿素CO(NH2)2水解生成的NH3催化还原NO是柴油机车辆尾气净化的主要方法。

(1)上述反应的
_______ 0(填“>”或“<”)。
(2)尿素在140-160℃时平均水解产氨率可以达到98.73%,写出其水解反应方程式_______ 。
(3)实际应用中,并非加入尿素的量越多柴油机车辆排放的尾气对空气污染程度越小,其原因是_______ 。
(4)除了利用尿素水解生成氨气,工业制备氨气主要是以氮气、氢气作为原料合成。在下列合成氨的事实中,不能用勒夏特列原理来解释的是_______。
①使用铁催化剂有利于合成氨反应
②在500℃左右高温下反应比常温下更有利于合成氨
③增大体系的压强,可以提高混合物中氨的百分含量
④在合成氨生产中,要不断补充新鲜的高压氮、氢混合气
(5)碳铵分解也可获得氨气。一定温度下,将一定量NH4HCO3投入一个密闭容器中发生如下反应:NH4HCO3(s) NH3(g)+CO2(g)+H2O(g),达到平衡后c(CO2)=xmol/L,缩小容器体积,经过一段时间反应再次平衡时c(CO2)=ymol/L,下列有关x和y的关系判断正确的是_______。
NH3(g)+CO2(g)+H2O(g),达到平衡后c(CO2)=xmol/L,缩小容器体积,经过一段时间反应再次平衡时c(CO2)=ymol/L,下列有关x和y的关系判断正确的是_______。

(1)上述反应的

(2)尿素在140-160℃时平均水解产氨率可以达到98.73%,写出其水解反应方程式
(3)实际应用中,并非加入尿素的量越多柴油机车辆排放的尾气对空气污染程度越小,其原因是
(4)除了利用尿素水解生成氨气,工业制备氨气主要是以氮气、氢气作为原料合成。在下列合成氨的事实中,不能用勒夏特列原理来解释的是_______。
①使用铁催化剂有利于合成氨反应
②在500℃左右高温下反应比常温下更有利于合成氨
③增大体系的压强,可以提高混合物中氨的百分含量
④在合成氨生产中,要不断补充新鲜的高压氮、氢混合气
| A.①③ | B.②④ | C.①② | D.③④ |
 NH3(g)+CO2(g)+H2O(g),达到平衡后c(CO2)=xmol/L,缩小容器体积,经过一段时间反应再次平衡时c(CO2)=ymol/L,下列有关x和y的关系判断正确的是_______。
NH3(g)+CO2(g)+H2O(g),达到平衡后c(CO2)=xmol/L,缩小容器体积,经过一段时间反应再次平衡时c(CO2)=ymol/L,下列有关x和y的关系判断正确的是_______。A. | B. | C. | D.题中所给条件不足以判断 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】(1)已知H2S的燃烧热ΔH=-akJ·mol-1,写出表示H2S燃烧反应的热化学方程式__ ,表示H2S燃烧热的热化学方程式__ 。
(2)若将FeCl3溶液蒸干灼烧,最后得到的固体产物主要是__ (填化学式)。FeCl3水溶液呈__ (填“酸”、“中”、“碱”)性,原因为:__ (用离子方程式表示)。
(3)炒过菜的铁锅未及时洗净(残液中有NaCl),第二天便会被腐蚀而出现红褐色铁锈,试回答:铁锅的腐蚀属于电化腐蚀,其原因是__ 。此时铁锅锈蚀主要是吸氧腐蚀,电极反应方程式为:负极:__ ,正极__ 。
(4)估计下列各变化过程是熵增加还是熵减小。(用A、B、C填空)
NH4NO3爆炸:2NH4NO3(s)=2N2(g)+4H2O(g)+O2(g)__
水煤气转化:CO(g)+H2O(g)=CO2(g)+H2(g)__
臭氧的生成:3O2(g)=2O3(g)__
A.熵增大 B.熵减小 C.熵变很小
(2)若将FeCl3溶液蒸干灼烧,最后得到的固体产物主要是
(3)炒过菜的铁锅未及时洗净(残液中有NaCl),第二天便会被腐蚀而出现红褐色铁锈,试回答:铁锅的腐蚀属于电化腐蚀,其原因是
(4)估计下列各变化过程是熵增加还是熵减小。(用A、B、C填空)
NH4NO3爆炸:2NH4NO3(s)=2N2(g)+4H2O(g)+O2(g)
水煤气转化:CO(g)+H2O(g)=CO2(g)+H2(g)
臭氧的生成:3O2(g)=2O3(g)
A.熵增大 B.熵减小 C.熵变很小
您最近一年使用:0次



