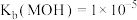丙氨酸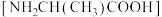 是人体内重要的氨基酸。25℃时,
是人体内重要的氨基酸。25℃时,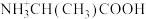 、
、 、
、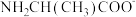 的分布分数[如
的分布分数[如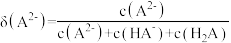 ]与
]与 关系如图。下列说法错误的是
关系如图。下列说法错误的是
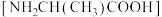 是人体内重要的氨基酸。25℃时,
是人体内重要的氨基酸。25℃时,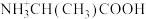 、
、 、
、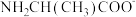 的分布分数[如
的分布分数[如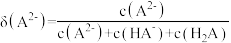 ]与
]与 关系如图。下列说法错误的是
关系如图。下列说法错误的是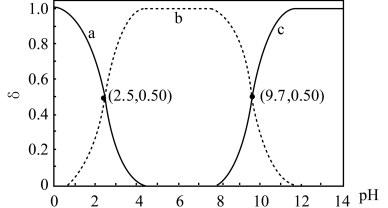
A.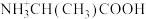 中 中 电离能力强于 电离能力强于 |
B. 时,丙氨酸微粒无法在电场作用下定向移动 时,丙氨酸微粒无法在电场作用下定向移动 |
C.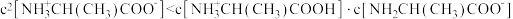 |
D.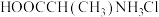 溶液中 溶液中 |
更新时间:2024/05/23 17:14:05
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法不正确 的是
| A.浓度均为0.1 mol·L-1的下列溶液:①(NH4)2SO4;②(NH4)2CO3;③(NH4)2Fe(SO4)2;溶液中c(NH4+)由大到小的顺序为:③>①>② |
| B.相同条件下用等pH的盐酸与醋酸溶液分别中和等量的NaOH,盐酸消耗的体积更多 |
| C.常温下,0.1mol·L-1的醋酸,加入水,溶液中c(CH3OOO-)/c(CH3OOOH)的值增大 |
| D.用标准硫酸溶液滴定久置的NaOH溶液可用酚酞作指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,下列说法不正确的是
| A.物质的量浓度相同的NaOH溶液和氨水:c(Na+)>c(NH4+) |
| B.物质的量浓度相同的盐酸和醋酸溶液,前者c(OH-)更小 |
| C.将相同体积相同物质的量浓度的NaOH溶液和醋酸溶液混合后呈碱性,说明醋酸是弱电解质 |
| D.pH=3的盐酸和pH=11的氨水混合后pH>7,说明氨水是弱电解质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】铬(VI)在溶液中可以多种形式存在。25℃时,调节初始浓度为0.1mol·L-1的Na2CrO4溶液的pH,平衡时铬(VI)在水溶液中各种存在形式的物质的量分数δ(X)与pH的关系如下图所示。已知溶液中存在反应2 +2H+⇌
+2H+⇌ +H2O
+H2O
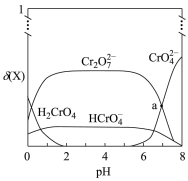
下列说法正确的是
 +2H+⇌
+2H+⇌ +H2O
+H2O
下列说法正确的是
| A.铬酸(H2CrO4)的第一步电离为完全电离 |
B.a点处,δ( )=δ( )=δ( )< )< |
| C.Ka2(H2CrO4)的数量级为10-6 |
D.若将Na2CrO4溶液加少量水稀释,则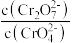 的值增大 的值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,CH3COOH(醋酸简写为HAc)和NH3·H2O的电离常数相等且Ka(HAc)=Kb(NH3·H2O)=1.8×10-5。将0.01mol NaAc和0.01mol NH4Ac配成200mL混液,然后加水稀释,测得稀释过程中pAc[pAc=-lgc(CH3COO-)]与溶液pH和物理量)的关系如图所示。下列叙述正确的是


| A.物理量Y是CH3COOH的浓度或水的电离程度 |
B.稀释过程中一直存在:2c( )+c(NH3·H2O)>c(Ac-) )+c(NH3·H2O)>c(Ac-) |
| C.室温下,NaAc溶液和NH4Cl溶液等体积混合后,混合溶液的pH=7 |
| D.室温下,将0.01mol NaAc和0.01mol HCl配成100mL混合液,该混合液的pH为8.9 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25℃时,分别向20 mL浓度均1.0 mol∙L-1的HA、NaA溶液中逐滴加入浓度均为1.0 mol∙L-1的NaOH、HCl溶液V mL,溶液的pH与lgY[Y= 或
或 ]的关系如图所示。下列说法不正确的是
]的关系如图所示。下列说法不正确的是
 或
或 ]的关系如图所示。下列说法不正确的是
]的关系如图所示。下列说法不正确的是
A.25℃时, 的数量级为 的数量级为 |
B.当 时: 时: |
C.曲线②中的 |
D.当滴入体积 mL时,溶液 mL时,溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,下列有关各溶液的叙述正确的是
A. 的溶液中不可能存在醋酸分子 的溶液中不可能存在醋酸分子 |
B. 的醋酸钠溶液与 的醋酸钠溶液与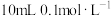 的盐酸混合后溶液显酸性: 的盐酸混合后溶液显酸性: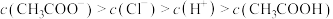 |
C. 醋酸的 醋酸的 , , 的醋酸的 的醋酸的 ,则 ,则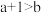 |
D.已知酸性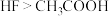 ,pH相等的 ,pH相等的 与 与 溶液中 溶液中 |
您最近一年使用:0次
单选题-题组
|
适中
(0.65)
名校
【推荐3】阅读下列资料,完成下列小题:
SO2是产生酸雨的主要原因,研究SO2等大气污染物的治理具有重要的意义。用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4.CO与SO2在一定条件下反应,可将SO2转化为S和CO2.
1.已知 2SO2(g)+ O2(g) = 2SO3(g) ΔH < 0,下列的说法正确的是
2.电解Na2SO3溶液的原理如下图所示,下列说法正确的是
3.25℃时,将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
SO2是产生酸雨的主要原因,研究SO2等大气污染物的治理具有重要的意义。用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4.CO与SO2在一定条件下反应,可将SO2转化为S和CO2.
1.已知 2SO2(g)+ O2(g) = 2SO3(g) ΔH < 0,下列的说法正确的是
| A.该反应的ΔS> 0 |
B.升高温度,该反应 (逆)增大, (逆)增大, (正)减小,平衡向逆反应方向移动 (正)减小,平衡向逆反应方向移动 |
| C.增大压强,反应物中活化分子百分数增大 |
| D.当消耗1mol SO2同时也消耗1mol SO3,说明反应达到了平衡状态 |
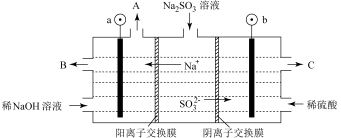
| A.从C口流出的物质是浓硫酸 |
| B.电极a连接电源的正极 |
| C.气体A为O2 |
D.电极b发生的电极反应式为:SO +2e-+H2O=SO +2e-+H2O=SO +2H+ +2H+ |
| A.c(OH-) | B.c(H+) | C. | D.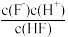 |
您最近一年使用:0次

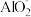 离子的数目为0.25NA
离子的数目为0.25NA
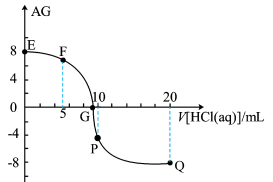
 MOH溶液中滴加pH=1的盐酸,溶液中AG(
MOH溶液中滴加pH=1的盐酸,溶液中AG(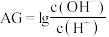 )与盐酸体积(V)之间的关系如图所示,下列说法不正确的是
)与盐酸体积(V)之间的关系如图所示,下列说法不正确的是