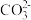草酸( 二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用。
二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用。
(1)常温下,pH=3的 溶液的物质的量浓度为
溶液的物质的量浓度为 ,pH=4的
,pH=4的 溶液的物质的量浓度为
溶液的物质的量浓度为 ,则
,则
______ 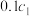 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2)已知: 的电离大于
的电离大于 的水解,常温下,用
的水解,常温下,用 溶液滴定20.00mL某未知浓度
溶液滴定20.00mL某未知浓度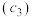 的
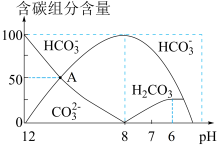
的 溶液,滴定曲线如图,c点所示溶液中:
溶液,滴定曲线如图,c点所示溶液中: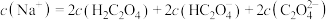 ,a点所示溶液中各离子的浓度由小到大的顺序为
,a点所示溶液中各离子的浓度由小到大的顺序为______ 。 酸性溶液滴定未知浓度
酸性溶液滴定未知浓度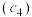 的无色
的无色 溶液,
溶液,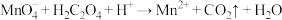 (未配平),滴定终点的判断方法是
(未配平),滴定终点的判断方法是______ 。
(4)乙学生按照滴定步骤进行了4次实验,分别记录有关数据如表:
依据上表数据计算法 溶液的物质的量浓度为
溶液的物质的量浓度为______ mol/L(保留4位有效数字)。
(5)下列操作中可能使测定结果偏高的是______(填字母)。
 二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用。
二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用。(1)常温下,pH=3的
 溶液的物质的量浓度为
溶液的物质的量浓度为 ,pH=4的
,pH=4的 溶液的物质的量浓度为
溶液的物质的量浓度为 ,则
,则
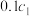 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)已知:
 的电离大于
的电离大于 的水解,常温下,用
的水解,常温下,用 溶液滴定20.00mL某未知浓度
溶液滴定20.00mL某未知浓度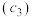 的
的 溶液,滴定曲线如图,c点所示溶液中:
溶液,滴定曲线如图,c点所示溶液中: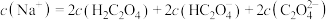 ,a点所示溶液中各离子的浓度由小到大的顺序为
,a点所示溶液中各离子的浓度由小到大的顺序为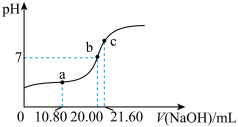
 酸性溶液滴定未知浓度
酸性溶液滴定未知浓度 的无色
的无色 溶液,
溶液,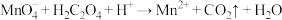 (未配平),滴定终点的判断方法是
(未配平),滴定终点的判断方法是(4)乙学生按照滴定步骤进行了4次实验,分别记录有关数据如表:
滴定次数 | 待测 |
| ||
滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
第一次 | 25.00 | 0.00 | 25.31 | 25.31 |
第二次 | 25.00 | 1.52 | 28.40 | 26.88 |
第三次 | 25.00 | 0.22 | 25.51 | 25.29 |
第四次 | 25.00 | 0.89 | 26.19 | 25.30 |
 溶液的物质的量浓度为
溶液的物质的量浓度为(5)下列操作中可能使测定结果偏高的是______(填字母)。
A.酸式滴定管未用标准液润洗就直接注入 标准液 标准液 |
| B.测定前盛放草酸溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管尖嘴部分在滴定前有气泡,滴定后没有气泡 |
D.读取 标准液时,开始仰视读数,滴定结束时俯视读数 标准液时,开始仰视读数,滴定结束时俯视读数 |
更新时间:2024-05-25 16:16:00
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O (g)。半水煤气经过下列步骤转化为合成氨的原料。完成下列填空:
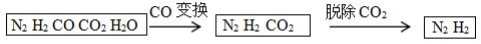
(1)半水煤气含有少量硫化氢。将半水煤气样品通入____________溶液中(填写试剂名称),出现___________,可以证明有硫化氢存在。
(2)写出半水煤气在铜催化下实现CO变换的反应方程式______________________;若半水煤气中V(H2): V(CO): V(N2)=9:7:4,经CO变换后的气体中:V(H2): V(N2)=__________。
(3)碱液吸收法是脱除二氧化碳的方法之一。有一吸收了二氧化碳的氢氧化钠洛液,为测定其溶液组成,采用双指示剂法进行滴定。
步骤:用移液管量取V0mL的该溶液于锥形瓶中,先滴入1-2滴酚酞做指示剂,滴定达到终点时用去c mol.L-1的标准盐酸溶液VlmL,此时再向溶液中滴入1-2滴__________做指示剂,达到滴定终点时又用去V2mL标准盐酸溶液。
第二次滴定达到终点时的现象是__________________________。
数据处理:通过Vl和V2的相对大小可以定性也可定量判断溶液的组成。
若V1>V2,写出此时的溶质的化学式_______________。
若2V1=V2,写出此时溶液中离子浓度由大到小的顺序_________________。
讨论:若V1<V2,在第一次滴定时未用标准盐酸润洗酸式滴定管,第二次滴定前发现并纠正了错误,则_________ (填化学式)浓度偏大。
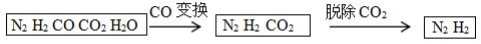
(1)半水煤气含有少量硫化氢。将半水煤气样品通入____________溶液中(填写试剂名称),出现___________,可以证明有硫化氢存在。
(2)写出半水煤气在铜催化下实现CO变换的反应方程式______________________;若半水煤气中V(H2): V(CO): V(N2)=9:7:4,经CO变换后的气体中:V(H2): V(N2)=__________。
(3)碱液吸收法是脱除二氧化碳的方法之一。有一吸收了二氧化碳的氢氧化钠洛液,为测定其溶液组成,采用双指示剂法进行滴定。
步骤:用移液管量取V0mL的该溶液于锥形瓶中,先滴入1-2滴酚酞做指示剂,滴定达到终点时用去c mol.L-1的标准盐酸溶液VlmL,此时再向溶液中滴入1-2滴__________做指示剂,达到滴定终点时又用去V2mL标准盐酸溶液。
第二次滴定达到终点时的现象是__________________________。
数据处理:通过Vl和V2的相对大小可以定性也可定量判断溶液的组成。
若V1>V2,写出此时的溶质的化学式_______________。
若2V1=V2,写出此时溶液中离子浓度由大到小的顺序_________________。
讨论:若V1<V2,在第一次滴定时未用标准盐酸润洗酸式滴定管,第二次滴定前发现并纠正了错误,则_________ (填化学式)浓度偏大。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。回答下列问题:
Ⅱ.NOx含量的测定
将V L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3−,加水稀释至100.00 mL。量取20.00 mL该溶液,加入V1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗V2 mL。
(1)NO被H2O2氧化为NO3−的离子方程式是___________ 。
(2)滴定过程中发生下列反应:
3Fe2++NO3−+4H+=NO↑+3Fe3++2H2O
Cr2O72− + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O
则气样中NOx折合成NO2的含量为_________ mg·m−3。
Ⅱ.NOx含量的测定
将V L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3−,加水稀释至100.00 mL。量取20.00 mL该溶液,加入V1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗V2 mL。
(1)NO被H2O2氧化为NO3−的离子方程式是
(2)滴定过程中发生下列反应:
3Fe2++NO3−+4H+=NO↑+3Fe3++2H2O
Cr2O72− + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O
则气样中NOx折合成NO2的含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图曲线所示,请回答:
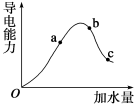
(1)“O”点为什么不导电:___________ 。
(2)a、b、c三点的氢离子浓度由小到大的顺序为___________ 。
(3)a、b、c三点中,醋酸的电离程度最大的一点是___________ 。
(4)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选择___________ (填字母)。
A.加热 B.加很稀的NaOH溶液 C.加固体KOH D.加水 E.加固体CH3COONa F.加Zn粒
(5)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是___________(填字母)。

(1)“O”点为什么不导电:
(2)a、b、c三点的氢离子浓度由小到大的顺序为
(3)a、b、c三点中,醋酸的电离程度最大的一点是
(4)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选择
A.加热 B.加很稀的NaOH溶液 C.加固体KOH D.加水 E.加固体CH3COONa F.加Zn粒
(5)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是___________(填字母)。
| A.c(H+) | B.H+个数 | C.CH3COOH分子数 | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据要求填写下列空白:
I.在氨水中存在下列电离平衡:NH3·H2O
 +OH-。
+OH-。
(1)下列情况能引起电离平衡正向移动的有_______ (填字母,下同)。
①加NH4Cl固体 ②加NaOH溶液 ③通入HCl ④加CH3COOH溶液 ⑤加水 ⑥加压
a.①③⑤ b.①④⑥ c.③④⑤ d.①②④
(2)在含有酚酞的0.1 mol· L-1氨水中加入少量的NH4Cl晶体,溶液颜色
a.变蓝色 b.变深 c.变浅 d.不变
(3)增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是 _______ (填字母)。
a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(4)在一定温度下,用水缓慢稀释1 mol·L-1氨水的过程中,溶液中随着水量的增加,
_______ (填“增大”“减小”或“不变”,下同),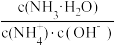
_______ 。
II.常温下,pH相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
(5)①加水稀释10倍后,醋酸溶液中的c(H+)_______ (填“>”“= ”或“<”,下同)盐酸溶液中的c(H+)。
②加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸_______ 盐酸。
③使温度都升高20°C ,溶液中c(H+):醋酸_______ 盐酸。
I.在氨水中存在下列电离平衡:NH3·H2O

 +OH-。
+OH-。(1)下列情况能引起电离平衡正向移动的有
①加NH4Cl固体 ②加NaOH溶液 ③通入HCl ④加CH3COOH溶液 ⑤加水 ⑥加压
a.①③⑤ b.①④⑥ c.③④⑤ d.①②④
(2)在含有酚酞的0.1 mol· L-1氨水中加入少量的NH4Cl晶体,溶液颜色
a.变蓝色 b.变深 c.变浅 d.不变
(3)增大
 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是 a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(4)在一定温度下,用水缓慢稀释1 mol·L-1氨水的过程中,溶液中随着水量的增加,

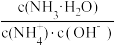
II.常温下,pH相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
(5)①加水稀释10倍后,醋酸溶液中的c(H+)
②加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸
③使温度都升高20°C ,溶液中c(H+):醋酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列水溶液中的离子反应与平衡相关问题:
(1)一定温度下,向NH3·H2O中加入NH4Cl固体,NH3·H2O的电离平衡将___________ 移动(填“向正反应方向”、“向逆反应方向”或“不发生”),c( )
)___________ (填“增大”、“减小”或“不变”),NH3·H2O的电离平衡常数___________ (填“增大”、“减小”或“不变”)。
(2)明矾化学式为KAl(SO4)2·12H2O,其净水原理用离子方程式表示为___________ 。
(3)室温下,将pH=2的HCl与pH=12的NH3·H2O混合至呈中性,则c(Cl-)___________ c(NH )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
(4)用HCl标准液滴定NaOH溶液时
①用___________ (填仪器名称)量取25.00 mLNaOH溶液,下图中,盛装待测液后排气泡动作正确的是___________ (填序号)。
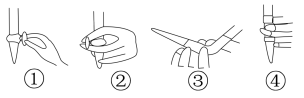
②下列操作(其他操作正确)造成测定结果偏低的是___________ (填字母)。
A.振荡过程中,锥形瓶内液体飞溅出瓶外
B.滴定起始时仰视读数
C.锥形瓶水洗后未干燥
D.酸式滴定管尖端部分有气泡,滴定后消失
(1)一定温度下,向NH3·H2O中加入NH4Cl固体,NH3·H2O的电离平衡将
 )
)(2)明矾化学式为KAl(SO4)2·12H2O,其净水原理用离子方程式表示为
(3)室温下,将pH=2的HCl与pH=12的NH3·H2O混合至呈中性,则c(Cl-)
 )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。(4)用HCl标准液滴定NaOH溶液时
①用

②下列操作(其他操作正确)造成测定结果偏低的是
A.振荡过程中,锥形瓶内液体飞溅出瓶外
B.滴定起始时仰视读数
C.锥形瓶水洗后未干燥
D.酸式滴定管尖端部分有气泡,滴定后消失
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。吸收液吸收SO2的过程中,pH随n( )∶n(HSO3−)变化关系如下表:
)∶n(HSO3−)变化关系如下表:
(1)由上表判断NaHSO3溶液显______ 性,用化学平衡原理解释原因:______________ 。
(2)当吸收液呈中性时,溶液中离子浓度关系正确的是________ (填字母)。
a.c(Na+)=2c( )+c(HSO3−)
)+c(HSO3−)
b.c(Na+)>c(HSO3−)>c( )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c( )+c(HSO3−)+c(OH-)
)+c(HSO3−)+c(OH-)
(3)已知:25 ℃时,H2SO3 HSO3−+H+的电离常数Ka=1×10-2,则该温度下NaHSO3的水解平衡常数Kh=
HSO3−+H+的电离常数Ka=1×10-2,则该温度下NaHSO3的水解平衡常数Kh=______ ,若向NaHSO3溶液中加入少量的I2,则溶液中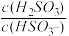 将
将______ (填“增大”“减小”或“不变”)。
 )∶n(HSO3−)变化关系如下表:
)∶n(HSO3−)变化关系如下表:n( )∶n(HSO3−) )∶n(HSO3−) | 91∶9 | 1∶1 | 9∶91 |
| pH | 8.2 | 7.2 | 6.2 |
(1)由上表判断NaHSO3溶液显
(2)当吸收液呈中性时,溶液中离子浓度关系正确的是
a.c(Na+)=2c(
 )+c(HSO3−)
)+c(HSO3−)b.c(Na+)>c(HSO3−)>c(
 )>c(H+)=c(OH-)
)>c(H+)=c(OH-)c.c(Na+)+c(H+)=c(
 )+c(HSO3−)+c(OH-)
)+c(HSO3−)+c(OH-)(3)已知:25 ℃时,H2SO3
 HSO3−+H+的电离常数Ka=1×10-2,则该温度下NaHSO3的水解平衡常数Kh=
HSO3−+H+的电离常数Ka=1×10-2,则该温度下NaHSO3的水解平衡常数Kh=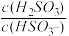 将
将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】砷(As)位于元素周期表的第四行与氮、磷同列。砷有多种化合物,用途广泛。完成下列填空:
(1)写出砷原子核外最外层电子的电子排布式。_______ 。
(2)1个砷的氢化物分子中含_______ 个化学键。
(3)砷化镓(GaAs)和氮化镓(GaN)都是原子间以共价键结合而成的晶体。GaAs熔点为1238°C、GaN熔点为1500°C,GaAs熔点低于GaN的原因是_______ 。
亚砷酸(H3AsO3) 可以用于治疗白血病。25°C,向0.1mol·L-1 H3AsO3溶液中滴加0.1mol·L-1KOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示。
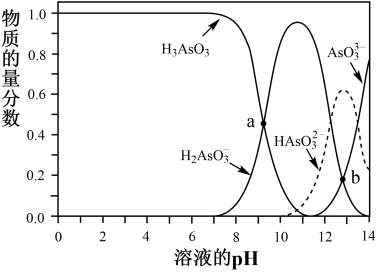
(4)人体血液的pH在7.35~7.45,患者用药后人体中含砷元素的主要微粒是_______ 。
(5)25°C,H2AsO 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是: _______ 。
(6)以酚酞为指示剂,将KOH溶液滴入H3AsO3溶液中,滴定终点的离子方程式是_______ 。
(7)b点溶液中:c(K+)_______ 2c(HAsO )+4c(AsO
)+4c(AsO ) (选填 “<”“>”或“=”)
) (选填 “<”“>”或“=”)
(1)写出砷原子核外最外层电子的电子排布式。
(2)1个砷的氢化物分子中含
(3)砷化镓(GaAs)和氮化镓(GaN)都是原子间以共价键结合而成的晶体。GaAs熔点为1238°C、GaN熔点为1500°C,GaAs熔点低于GaN的原因是
亚砷酸(H3AsO3) 可以用于治疗白血病。25°C,向0.1mol·L-1 H3AsO3溶液中滴加0.1mol·L-1KOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示。

(4)人体血液的pH在7.35~7.45,患者用药后人体中含砷元素的主要微粒是
(5)25°C,H2AsO
 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是: (6)以酚酞为指示剂,将KOH溶液滴入H3AsO3溶液中,滴定终点的离子方程式是
(7)b点溶液中:c(K+)
 )+4c(AsO
)+4c(AsO ) (选填 “<”“>”或“=”)
) (选填 “<”“>”或“=”)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】甲胺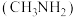 是一种一元弱碱。已知:
是一种一元弱碱。已知: 时,甲胺的电离常数
时,甲胺的电离常数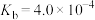 ,
, 。
。 时,向
时,向 溶液中滴加
溶液中滴加 的盐酸,混合溶液的
的盐酸,混合溶液的 、导电能力与加入盐酸体积
、导电能力与加入盐酸体积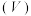 的关系如图所示。试回答下列问题:
的关系如图所示。试回答下列问题:

(1) 属于
属于_____ (填“强”或“弱”)电解质, 在水中的电离过程与
在水中的电离过程与 相似,写出
相似,写出 在水中的电离方程式:
在水中的电离方程式:_____ 。
(2) 时,
时, 点溶液呈
点溶液呈_____ (填“酸性”、“碱性”或“中性”)。
(3)已知:图中 点对应的溶液导电能力最强。则b、d、e三点对应的溶液中,水的电离程度由大到小的顺序为
点对应的溶液导电能力最强。则b、d、e三点对应的溶液中,水的电离程度由大到小的顺序为_____ , 的电离程度由大到小的顺序为
的电离程度由大到小的顺序为_____ 。
(4)图中
_____ (填“=”、“<”或“>”)20.00,b点对应的溶液中各离子浓度由大到小的顺序为_____ 。
(5) 点对应的溶液中
点对应的溶液中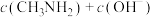
_____ (填“=”、“<”或“>”) 。
。
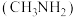 是一种一元弱碱。已知:
是一种一元弱碱。已知: 时,甲胺的电离常数
时,甲胺的电离常数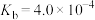 ,
, 。
。 时,向
时,向 溶液中滴加
溶液中滴加 的盐酸,混合溶液的
的盐酸,混合溶液的 、导电能力与加入盐酸体积
、导电能力与加入盐酸体积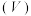 的关系如图所示。试回答下列问题:
的关系如图所示。试回答下列问题:
(1)
 属于
属于 在水中的电离过程与
在水中的电离过程与 相似,写出
相似,写出 在水中的电离方程式:
在水中的电离方程式:(2)
 时,
时, 点溶液呈
点溶液呈(3)已知:图中
 点对应的溶液导电能力最强。则b、d、e三点对应的溶液中,水的电离程度由大到小的顺序为
点对应的溶液导电能力最强。则b、d、e三点对应的溶液中,水的电离程度由大到小的顺序为 的电离程度由大到小的顺序为
的电离程度由大到小的顺序为(4)图中

(5)
 点对应的溶液中
点对应的溶液中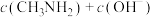
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】今有①CH3COOH、②HCl、③H2SO4 三种溶液,用序号 回答下列问题
(1)当它们pH相同时,其物质的量浓度的由大到小排列是__________________ 。
(2)当它们的物质的量浓度相同时,其pH的由大到小排列是_________________ 。
(1)当它们pH相同时,其物质的量浓度的由大到小排列是
(2)当它们的物质的量浓度相同时,其pH的由大到小排列是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】NH4Al(SO4)2是一种食品添加剂,用于焙烤食品;NH4HSO4在分析化学、制药工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是___________________________________________________ (用必要的化学用语和相关文字说明)。
(2)相同温度下,浓度均为0.1 mol/L 的下列溶液中的c( )由大到小
)由大到小_____ (填序号)。
①NH4Al(SO4)2 ②CH3COONH4 ③ NH4HSO4 ④NH3·H2O ⑤NH4Cl
(3)如图1是0.1 mol/L电解质溶液的pH随温度变化的图象。其中符合0.1 mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线是_____ (填写字母)。
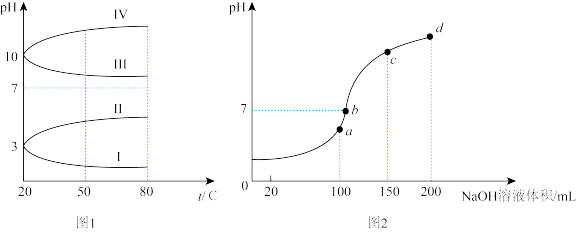
(4)室温时,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是_____ ;在b点,溶液中各离子浓度由大到小的排列顺序是______ ;在cd段发生反应的离子方程式________________ 。
(1)NH4Al(SO4)2可作净水剂,其理由是
(2)相同温度下,浓度均为0.1 mol/L 的下列溶液中的c(
 )由大到小
)由大到小①NH4Al(SO4)2 ②CH3COONH4 ③ NH4HSO4 ④NH3·H2O ⑤NH4Cl
(3)如图1是0.1 mol/L电解质溶液的pH随温度变化的图象。其中符合0.1 mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线是

(4)室温时,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知H2C2O4的电离平衡常数Ka1=5×10-2,Ka2=5×10-5,请回答下列问题:
(1)将10mL0.1mol/L的H2C2O4溶液加蒸馏水稀释到100mL后,下列变化中正确的有__ 。
①稀释前后溶液中c(H+)之比小于10
②溶液中所有离子浓度下降
③ 不变
不变
(2)下列溶液一定呈中性的是____
A.pH=7 B. =10-14 C.c(H+)=
=10-14 C.c(H+)=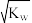
D.H2C2O4和K2C2O4的混合溶液中c(K+)=c(HC2O4-)+2c(C2O42-)
(3)草酸亚铁晶体(FeC2O4.xH2O)为淡黄色粉末,不溶于水,可作照相显影剂和用于制药工业。某化学兴趣小组称取yg样品,加入适量稀硫酸溶解,用0.1mol/L的酸性KMnO4溶液滴定测定x的值,发生的反应为Fe2++C2O42-+MnO4-→Fe3++CO2+Mn2+(未配平),滴定终点的现象为__ ,若滴定终点消耗20.00mLKMnO4溶液,则x=__ (用含y的式子表示)。
(4)已知:亚硝酸(HNO2)性质和硝酸类似,常温下亚硝酸的电离平衡常数Ka=5.1×10-4。在该温度下向含有1mol草酸钠的溶液中加入2mol的亚硝酸,溶液中所发生反应的离子反应方程式为___ 。
(5)T℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中三种微粒H2C2O4、HC2O4- 、C2O42-的物质的量分数(δ)与pH的关系如图所示:则A点对应的pH为__ 。

(1)将10mL0.1mol/L的H2C2O4溶液加蒸馏水稀释到100mL后,下列变化中正确的有
①稀释前后溶液中c(H+)之比小于10
②溶液中所有离子浓度下降
③
 不变
不变(2)下列溶液一定呈中性的是
A.pH=7 B.
 =10-14 C.c(H+)=
=10-14 C.c(H+)=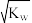
D.H2C2O4和K2C2O4的混合溶液中c(K+)=c(HC2O4-)+2c(C2O42-)
(3)草酸亚铁晶体(FeC2O4.xH2O)为淡黄色粉末,不溶于水,可作照相显影剂和用于制药工业。某化学兴趣小组称取yg样品,加入适量稀硫酸溶解,用0.1mol/L的酸性KMnO4溶液滴定测定x的值,发生的反应为Fe2++C2O42-+MnO4-→Fe3++CO2+Mn2+(未配平),滴定终点的现象为
(4)已知:亚硝酸(HNO2)性质和硝酸类似,常温下亚硝酸的电离平衡常数Ka=5.1×10-4。在该温度下向含有1mol草酸钠的溶液中加入2mol的亚硝酸,溶液中所发生反应的离子反应方程式为
(5)T℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中三种微粒H2C2O4、HC2O4- 、C2O42-的物质的量分数(δ)与pH的关系如图所示:则A点对应的pH为

您最近一年使用:0次


 、
、 、
、