以水钴矿(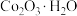 ,含
,含 、MgO、CaO)和辉铜矿(
、MgO、CaO)和辉铜矿( ,含
,含 、
、 )为原料制取胆矾和单质钴。
)为原料制取胆矾和单质钴。 ,
,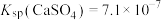 ,
,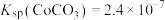 ;
;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
③萃取 的反应原理;
的反应原理; ;
;
④Mg、Ca、Fe、Co均能与强酸反应产生 。
。
回答下列问题:
(1)基态Co原子的简化电子排布式为___________ 。
(2)“酸浸”过程硫元素价态变为 价,写出“酸浸”过程中主要反应的化学方程式:
价,写出“酸浸”过程中主要反应的化学方程式:___________ 。
(3)“滤渣1”的主要成分为___________ 。
(4)常温下,若“滤液2”中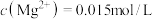 (忽略溶液中极少量的
(忽略溶液中极少量的 ),除去2L“滤液2”中的
),除去2L“滤液2”中的 ,至少需加入NaF固体的质量为
,至少需加入NaF固体的质量为___________ g(忽略溶液体积的变化)。
(5)“反萃取”步骤中加入的“试剂a”为___________ 。
(6)采用惰性电极电解 溶液﹑在无离子交换膜的条件下,不能用
溶液﹑在无离子交换膜的条件下,不能用 溶液代替
溶液代替 溶液的理由是
溶液的理由是___________ 。
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入 至弱酸性,生成白色沉淀和硫酸铵。经仪器分析:白色沉淀含H、N、O、S、Cu五种元素;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为一种三角锥形和一种正四面体形。则白色沉淀的化学式为
至弱酸性,生成白色沉淀和硫酸铵。经仪器分析:白色沉淀含H、N、O、S、Cu五种元素;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为一种三角锥形和一种正四面体形。则白色沉淀的化学式为___________ 。
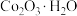 ,含
,含 、MgO、CaO)和辉铜矿(
、MgO、CaO)和辉铜矿( ,含
,含 、
、 )为原料制取胆矾和单质钴。
)为原料制取胆矾和单质钴。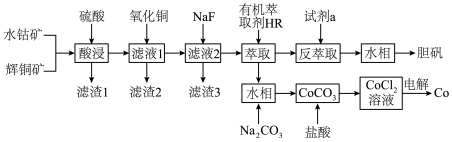
 ,
,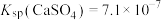 ,
,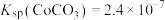 ;
;②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 |  |  |  |  |
开始沉淀时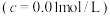 的pH 的pH | 2.7 | 7.5 | 7.6 | 4.7 |
完全沉淀时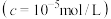 的pH 的pH | 3.7 | 9.0 | 9.1 | 6.2 |
 的反应原理;
的反应原理; ;
;④Mg、Ca、Fe、Co均能与强酸反应产生
 。
。回答下列问题:
(1)基态Co原子的简化电子排布式为
(2)“酸浸”过程硫元素价态变为
 价,写出“酸浸”过程中主要反应的化学方程式:
价,写出“酸浸”过程中主要反应的化学方程式:(3)“滤渣1”的主要成分为
(4)常温下,若“滤液2”中
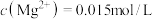 (忽略溶液中极少量的
(忽略溶液中极少量的 ),除去2L“滤液2”中的
),除去2L“滤液2”中的 ,至少需加入NaF固体的质量为
,至少需加入NaF固体的质量为(5)“反萃取”步骤中加入的“试剂a”为
(6)采用惰性电极电解
 溶液﹑在无离子交换膜的条件下,不能用
溶液﹑在无离子交换膜的条件下,不能用 溶液代替
溶液代替 溶液的理由是
溶液的理由是(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入
 至弱酸性,生成白色沉淀和硫酸铵。经仪器分析:白色沉淀含H、N、O、S、Cu五种元素;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为一种三角锥形和一种正四面体形。则白色沉淀的化学式为
至弱酸性,生成白色沉淀和硫酸铵。经仪器分析:白色沉淀含H、N、O、S、Cu五种元素;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为一种三角锥形和一种正四面体形。则白色沉淀的化学式为
更新时间:2024-05-25 15:46:54
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)元素⑧中质子数和中子数相等的同位素符号是:____________ ;
(2)④、⑤、⑥的离子半径由大到小的顺序为:________________ ;
(3)③的气态氢化物与其最高价氧化物对应水化物反应的化学方程式为:______________ ;
(4)④、⑤两种元素的原子按1:1组成的常见化合物,其阴、阳离子个数比为:__________ ;
(5)由表中两种元素形成的氢化物A和B都含有18个电子,A是一种6原子分子,可做火箭发动机燃料;B是一种常见强氧化剂。已知:液态A与液态B充分反应生成一种液态10电子分子和一种气态单质,写出A与B反应的化学方程式___________________________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)④、⑤、⑥的离子半径由大到小的顺序为:
(3)③的气态氢化物与其最高价氧化物对应水化物反应的化学方程式为:
(4)④、⑤两种元素的原子按1:1组成的常见化合物,其阴、阳离子个数比为:
(5)由表中两种元素形成的氢化物A和B都含有18个电子,A是一种6原子分子,可做火箭发动机燃料;B是一种常见强氧化剂。已知:液态A与液态B充分反应生成一种液态10电子分子和一种气态单质,写出A与B反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】水合氧化铁[ ]是一种重要的化工原料,用作磁性材料、颜料铁黄等。一种以硫铁矿烧渣(含Fe、FeO、
]是一种重要的化工原料,用作磁性材料、颜料铁黄等。一种以硫铁矿烧渣(含Fe、FeO、 和少量CuO)为原料生产
和少量CuO)为原料生产 的工艺流程如下:
的工艺流程如下:

回答下列问题:
(1)“酸浸”时CuO与硫酸发生反应的离子方程式为___________ 。
(2)“除杂”时滤渣②的成分有Fe和___________ 。
(3)“加热氧化”时 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(4)“过滤”后需洗涤 沉淀,请设计实验检验
沉淀,请设计实验检验 沉淀是否洗涤干净
沉淀是否洗涤干净_______ 。
 ]是一种重要的化工原料,用作磁性材料、颜料铁黄等。一种以硫铁矿烧渣(含Fe、FeO、
]是一种重要的化工原料,用作磁性材料、颜料铁黄等。一种以硫铁矿烧渣(含Fe、FeO、 和少量CuO)为原料生产
和少量CuO)为原料生产 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)“酸浸”时CuO与硫酸发生反应的离子方程式为
(2)“除杂”时滤渣②的成分有Fe和
(3)“加热氧化”时
 发生反应的化学方程式为
发生反应的化学方程式为(4)“过滤”后需洗涤
 沉淀,请设计实验检验
沉淀,请设计实验检验 沉淀是否洗涤干净
沉淀是否洗涤干净
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】化合物X由4种不同周期的元素组成,某实验小组按如下流程进行相关实验:
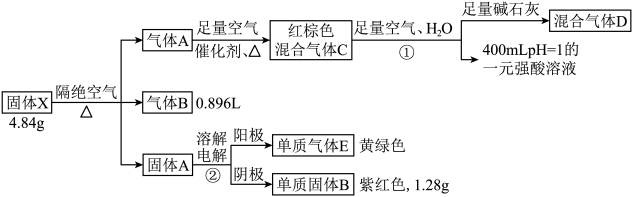
除C、D外其他未知物均为纯净物,其中气体A能使湿润的红色石蕊试纸变蓝,气体B的密度为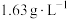 ,反应②将固体A充分溶解,电解至金属阳离子恰好反应完,所有数据均在标准状况下测得,流程中的反应均充分进行。请回答:
,反应②将固体A充分溶解,电解至金属阳离子恰好反应完,所有数据均在标准状况下测得,流程中的反应均充分进行。请回答:
(1)组成X的4种元素是______ (填元素符号),气体A的VSEPR模型为______ 。
(2)已知混合气体D为无色气体,其主要成分为______ (写化学式);写出反应①的化学方程式______ 。
(3)X属于配合物,其水溶液与足量NaF溶液反应可生成具有相同配位数的配合物,写出该反应的离子方程式______ 。
(4)用铁电极作为反应②的阴极时,电极上最终收集到的固体产物中会混有少量的 杂质,设计实验对其中的Fe元素进行检验
杂质,设计实验对其中的Fe元素进行检验______ 。

除C、D外其他未知物均为纯净物,其中气体A能使湿润的红色石蕊试纸变蓝,气体B的密度为
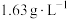 ,反应②将固体A充分溶解,电解至金属阳离子恰好反应完,所有数据均在标准状况下测得,流程中的反应均充分进行。请回答:
,反应②将固体A充分溶解,电解至金属阳离子恰好反应完,所有数据均在标准状况下测得,流程中的反应均充分进行。请回答:(1)组成X的4种元素是
(2)已知混合气体D为无色气体,其主要成分为
(3)X属于配合物,其水溶液与足量NaF溶液反应可生成具有相同配位数的配合物,写出该反应的离子方程式
(4)用铁电极作为反应②的阴极时,电极上最终收集到的固体产物中会混有少量的
 杂质,设计实验对其中的Fe元素进行检验
杂质,设计实验对其中的Fe元素进行检验
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】以废锌催化剂(主要成分为ZnO 及少量Fe2O3、CuO、MnO、SiO2)为原料制备锌的流程如下:

已知:①“浸取”时,ZnO、CuO转化为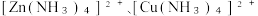 进入溶液;②25℃时, Ksp
进入溶液;②25℃时, Ksp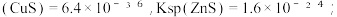 ③深度除杂标准:溶液中
③深度除杂标准:溶液中 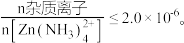
(1)“滤渣1”的主要成分为 Mn(OH)2、SiO2和_______ 。
(2)“深度除锰”是在碱性条件下将残留的Mn2+转化为MnO2,离子方程式为_______ 。
(3)“深度除铜”时,锌的最终回收率、[除铜效果以反应后溶液中铜锌比 表示]与“(NH4)2S 加入量”[以
表示]与“(NH4)2S 加入量”[以 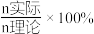 表示]的关系曲线如图所示。
表示]的关系曲线如图所示。
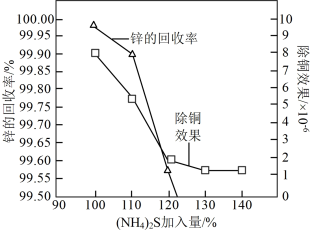
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是_______ (用离子方程式表示),该反应的平衡常数为_______ 。{已知 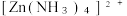 的
的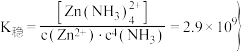
②“深度除铜”时(NH4)2S加入量最好应选_______ (填字母)。
A.100% B.110% C.120% D.130%
(4)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,如图结构。
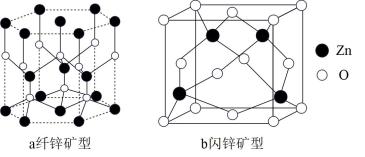
①图a纤锌矿型ZnO晶体中O2-的配位数为_______ 。
②图b闪锌矿型晶胞密度为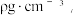 则Zn2+与(O2-的距离为
则Zn2+与(O2-的距离为_______ nm。(设NA为阿伏加德罗常数的值)

已知:①“浸取”时,ZnO、CuO转化为
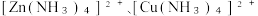 进入溶液;②25℃时, Ksp
进入溶液;②25℃时, Ksp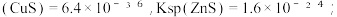 ③深度除杂标准:溶液中
③深度除杂标准:溶液中 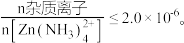
(1)“滤渣1”的主要成分为 Mn(OH)2、SiO2和
(2)“深度除锰”是在碱性条件下将残留的Mn2+转化为MnO2,离子方程式为
(3)“深度除铜”时,锌的最终回收率、[除铜效果以反应后溶液中铜锌比
 表示]与“(NH4)2S 加入量”[以
表示]与“(NH4)2S 加入量”[以 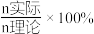 表示]的关系曲线如图所示。
表示]的关系曲线如图所示。
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是
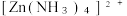 的
的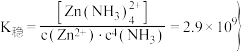
②“深度除铜”时(NH4)2S加入量最好应选
A.100% B.110% C.120% D.130%
(4)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,如图结构。

①图a纤锌矿型ZnO晶体中O2-的配位数为
②图b闪锌矿型晶胞密度为
 则Zn2+与(O2-的距离为
则Zn2+与(O2-的距离为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)盐酸滴定氢氧化钠溶液:滴定时应将盐酸溶液加入_______ (填“酸式”或“碱式”)滴定管中;在规格为50.00 的滴定管中,若NaOH溶液起始读数为15.00
的滴定管中,若NaOH溶液起始读数为15.00 ,此时滴定管中NaOH溶液的实际体积为
,此时滴定管中NaOH溶液的实际体积为_______ (填标号)。
a.15.00 B.35.00
B.35.00 C.大于35.00
C.大于35.00 D.小于15.00
D.小于15.00
(2)用KMnO4标准溶液在酸性条件下进行氧化还原滴定补血剂FeSO4·7H2O某同学设计的下列滴定方式中,最合理的是_______ (填字母)。

(3)下列操作能使结果偏大的是
(4)常温下,有关物质的溶度积如下:Ksp[Mg(OH)2]=3.2x10-11,Ksp[Cu(OH)2]=2.0x10-20。向含有 、Cu2+的溶液中滴加
、Cu2+的溶液中滴加 溶液,当两种沉淀共存时c(Mg2+):c(Cu2+)=
溶液,当两种沉淀共存时c(Mg2+):c(Cu2+)=_______ 。
(5)工业原料氯化铜中含杂质 ,使其溶于水,再加入适量
,使其溶于水,再加入适量__________________ (填“名称”),目的是消耗_______ 促进____________ (填“离子方程式”)平衡右移,使Fe3+完全沉淀。
(6)以 为原料制得的
为原料制得的 溶液中常含有
溶液中常含有 、
、 、
、 等金属离子,通过添加过量难溶电解质
等金属离子,通过添加过量难溶电解质 ,可使这些金属离子形成硫化物沉淀,经过滤除去包括
,可使这些金属离子形成硫化物沉淀,经过滤除去包括 在内的沉淀,再经蒸发、结晶,可得纯净的
在内的沉淀,再经蒸发、结晶,可得纯净的 。根据上述实验事实,可推知溶解度
。根据上述实验事实,可推知溶解度
_______ CdS(填“<”“>”或“=”),写出 生成硫化物沉淀的离子方程式
生成硫化物沉淀的离子方程式______________________________ 。
(1)盐酸滴定氢氧化钠溶液:滴定时应将盐酸溶液加入
 的滴定管中,若NaOH溶液起始读数为15.00
的滴定管中,若NaOH溶液起始读数为15.00 ,此时滴定管中NaOH溶液的实际体积为
,此时滴定管中NaOH溶液的实际体积为a.15.00
 B.35.00
B.35.00 C.大于35.00
C.大于35.00 D.小于15.00
D.小于15.00
(2)用KMnO4标准溶液在酸性条件下进行氧化还原滴定补血剂FeSO4·7H2O某同学设计的下列滴定方式中,最合理的是

(3)下列操作能使结果偏大的是
| A.滴定管未润洗即装入标准溶液 | B.滴定过程中开始仰视,后来俯视度数 |
| C.滴定过程中锥形瓶中不慎有液体溅出 | D.滴定开始时滴定管尖嘴处有气泡,滴定后气泡消失 |
 、Cu2+的溶液中滴加
、Cu2+的溶液中滴加 溶液,当两种沉淀共存时c(Mg2+):c(Cu2+)=
溶液,当两种沉淀共存时c(Mg2+):c(Cu2+)=(5)工业原料氯化铜中含杂质
 ,使其溶于水,再加入适量
,使其溶于水,再加入适量(6)以
 为原料制得的
为原料制得的 溶液中常含有
溶液中常含有 、
、 、
、 等金属离子,通过添加过量难溶电解质
等金属离子,通过添加过量难溶电解质 ,可使这些金属离子形成硫化物沉淀,经过滤除去包括
,可使这些金属离子形成硫化物沉淀,经过滤除去包括 在内的沉淀,再经蒸发、结晶,可得纯净的
在内的沉淀,再经蒸发、结晶,可得纯净的 。根据上述实验事实,可推知溶解度
。根据上述实验事实,可推知溶解度
 生成硫化物沉淀的离子方程式
生成硫化物沉淀的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】氮化镓(GaN)具有优异的光电性能。综合利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4]获得3种金属盐,并进一步利用镓盐制备氮化镓(GaN),部分工艺流程如下:
②常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表:
(1)为提高浸出率,可采用的方法是___________ (填一种方法即可)。
(2)基态镓原子的价层电子排布图为___________ 。GaN的熔点为1700℃,晶胞如图所示,GaN的晶体类型为___________ 。___________ (填化学式)。
(4)处理浸出液时,将溶液的pH调节至5.4,此时溶液中Fe3+的浓度为___________ 。
(5)“溶解还原”步骤中需要加入一定量的铁粉,进行该操作的主要目的是___________ 。
(6)“高温合成”操作中Ga(CH3)3与NH3反应生成GaN的化学方程式为___________ 。
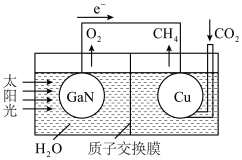
(7)下图可表示氮化镓与铜组装成的人工光合系统的工作原理。请写出铜电极上的电极反应式___________ 。
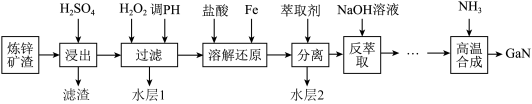
②常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表:
| 金属离子 | Fe2+ | Fe3+ | Zn2+ | Ga3+ |
| 开始沉淀pH | 8.0 | 1.7 | 5.5 | 3.0 |
| 沉淀完全pH | 9.6 | 3.2 | 8.0 | 4.9 |
| 萃取率(%) | 0 | 99 | 0 | 97~98.5 |
(1)为提高浸出率,可采用的方法是
(2)基态镓原子的价层电子排布图为
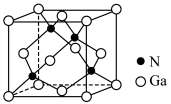
(4)处理浸出液时,将溶液的pH调节至5.4,此时溶液中Fe3+的浓度为
(5)“溶解还原”步骤中需要加入一定量的铁粉,进行该操作的主要目的是
(6)“高温合成”操作中Ga(CH3)3与NH3反应生成GaN的化学方程式为
(7)下图可表示氮化镓与铜组装成的人工光合系统的工作原理。请写出铜电极上的电极反应式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】金属锂及其化合物因独特的性质而具有重要的应用价值。例如:锰酸锂可用于电池; Li2O 可用于特种玻璃、陶瓷、医药等领域: LiH、LiBH4、LiNH2为常见的储氢材料等。回答下列问题:
(1)Mn2+最外层电子排布式___________
(2)LiH、LiBH4、 LiNH2中所含非金属元素的电负性由小到大的顺序为___________ (用元素符号表示); LiBH4中阴离子的空间构型为___________
(3)Li2O的熔点(1567℃)高于LiCl的熔点(605℃)的原因是___________ 。
(4)Li2O立方晶胞结构如图所示,晶胞边长为anm。Li+在晶胞中的配位数为___________ ;Li+和O2-的最短距离为___________ nm。

(1)Mn2+最外层电子排布式
(2)LiH、LiBH4、 LiNH2中所含非金属元素的电负性由小到大的顺序为
(3)Li2O的熔点(1567℃)高于LiCl的熔点(605℃)的原因是
(4)Li2O立方晶胞结构如图所示,晶胞边长为anm。Li+在晶胞中的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】镍是一种硬而有延展性并具有铁磁性的金属,且抗腐蚀,是重要的合金材料和催化剂。回答下列问题:
(1)基态镍原子的价电子排布式为___________ 。
(2) 可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见下图)等。
可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见下图)等。
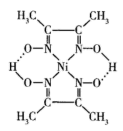
①CN-中碳原子的杂化方式为___________ ,1 mol[Ni(CN)4]2-中含有___________ molσ键。
②[Ni(NH3)4]2+中H-N-H键角比NH3分子中H-N-H键角___________ (填“大”或“小”),NH3极易溶于水的原因是___________ 。
③丁二酮肟镍分子内含有的作用力有___________ (填字母)。
a.配位键 b.离子键 c.氢键 d.范德华力
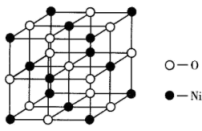
(3)NiO的晶胞结构如图所示,其密度是d g/cm3,距离最近的两个O2-之间的距离为___________  (用含d、NA的代数式表示,设NA表示阿伏加德罗常数的值)。
(用含d、NA的代数式表示,设NA表示阿伏加德罗常数的值)。
(1)基态镍原子的价电子排布式为
(2)
 可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见下图)等。
可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见下图)等。
①CN-中碳原子的杂化方式为
②[Ni(NH3)4]2+中H-N-H键角比NH3分子中H-N-H键角
③丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.范德华力
(3)NiO的晶胞结构如图所示,其密度是d g/cm3,距离最近的两个O2-之间的距离为
 (用含d、NA的代数式表示,设NA表示阿伏加德罗常数的值)。
(用含d、NA的代数式表示,设NA表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】N、P、 为第VA族元素,该族元素及其化合物在生产,生活中有广泛应用。回答下列问题:
为第VA族元素,该族元素及其化合物在生产,生活中有广泛应用。回答下列问题:
(1)基态砷原子核外有___________ 个未成对电子,位于元素周期表的___________ 区。
(2)已知: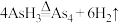 ,
, 的空间结构为
的空间结构为___________ , 原子的杂化类型为
原子的杂化类型为___________ ;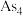 为正四面体结构,则1
为正四面体结构,则1
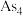 中含
中含___________ 
 键。
键。
(3)《本草纲目》中记载砒霜( )可入药,已知:
)可入药,已知: 的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力有
的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力有___________ ;
(4) 的键角为93.5°,
的键角为93.5°, 的键角为92.1°,
的键角为92.1°, 的键角大于
的键角大于 的键角的原因是
的键角的原因是______ ;
(5)由砷,铁,钙组成的某种新材料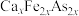 ,的晶胞结构如图所示。已知:
,的晶胞结构如图所示。已知: ,底边边长为a
,底边边长为a ,高为b
,高为b ,1号原子的高为
,1号原子的高为 。
。
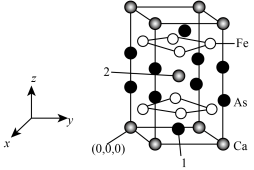
①1号原子的坐标为___________ ,距离2号原子最近的 原子有
原子有___________ 个。
②该晶体密度为___________  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 为第VA族元素,该族元素及其化合物在生产,生活中有广泛应用。回答下列问题:
为第VA族元素,该族元素及其化合物在生产,生活中有广泛应用。回答下列问题:(1)基态砷原子核外有
(2)已知:
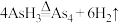 ,
, 的空间结构为
的空间结构为 原子的杂化类型为
原子的杂化类型为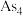 为正四面体结构,则1
为正四面体结构,则1
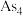 中含
中含
 键。
键。(3)《本草纲目》中记载砒霜(
 )可入药,已知:
)可入药,已知: 的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力有
的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力有(4)
 的键角为93.5°,
的键角为93.5°, 的键角为92.1°,
的键角为92.1°, 的键角大于
的键角大于 的键角的原因是
的键角的原因是(5)由砷,铁,钙组成的某种新材料
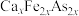 ,的晶胞结构如图所示。已知:
,的晶胞结构如图所示。已知: ,底边边长为a
,底边边长为a ,高为b
,高为b ,1号原子的高为
,1号原子的高为 。
。
①1号原子的坐标为
 原子有
原子有②该晶体密度为
 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硼是一种用途广泛的化工原料矿物,主要用于生产硼砂、硼酸和硼的各种化合物。回答下列问题:
Ⅰ.一种比率光声探针M与 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:________ ,B在元素周期表中位于________ 区,M中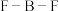 键角
键角________  中
中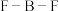 键角(填“>”、“<”或“=”)。
键角(填“>”、“<”或“=”)。
(2)均为平面结构的吡咯(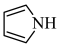 )和吡啶(
)和吡啶(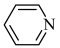 )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为________ ,原因是________ 。
Ⅱ.B的简单氢化物 不能游离存在,常倾向于形成较稳定的或与其他分子结合。
不能游离存在,常倾向于形成较稳定的或与其他分子结合。
(3) 分子结构如图,则B原子的杂化方式为
分子结构如图,则B原子的杂化方式为________ 。 )被认为是最具潜力的新型储氢材料之一,写出一种与氨硼烷互为等电子体的分子
)被认为是最具潜力的新型储氢材料之一,写出一种与氨硼烷互为等电子体的分子________ (填化学式)。
Ⅲ.硼砂是含结晶水的四硼酸钠,请根据模型回答有关问题: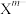 (含B、O、H三种元素)的球棍模型如图所示,则在
(含B、O、H三种元素)的球棍模型如图所示,则在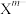 中的2号硼原子的价层电子对数为
中的2号硼原子的价层电子对数为________ ,
________ (填数字)。
(6) 和过量NaF作用可生成
和过量NaF作用可生成 ,
, 的空间结构为
的空间结构为________ , 的电子式为
的电子式为________ 。
Ⅰ.一种比率光声探针M与
 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
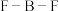 键角
键角 中
中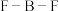 键角(填“>”、“<”或“=”)。
键角(填“>”、“<”或“=”)。(2)均为平面结构的吡咯(
 )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为Ⅱ.B的简单氢化物
 不能游离存在,常倾向于形成较稳定的或与其他分子结合。
不能游离存在,常倾向于形成较稳定的或与其他分子结合。(3)
 分子结构如图,则B原子的杂化方式为
分子结构如图,则B原子的杂化方式为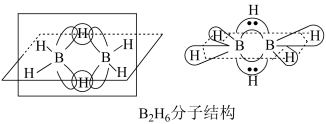
 )被认为是最具潜力的新型储氢材料之一,写出一种与氨硼烷互为等电子体的分子
)被认为是最具潜力的新型储氢材料之一,写出一种与氨硼烷互为等电子体的分子Ⅲ.硼砂是含结晶水的四硼酸钠,请根据模型回答有关问题:
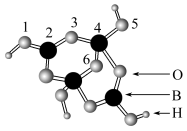
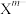 (含B、O、H三种元素)的球棍模型如图所示,则在
(含B、O、H三种元素)的球棍模型如图所示,则在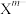 中的2号硼原子的价层电子对数为
中的2号硼原子的价层电子对数为
(6)
 和过量NaF作用可生成
和过量NaF作用可生成 ,
, 的空间结构为
的空间结构为 的电子式为
的电子式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铝及其化合物广泛应用于金属冶炼和有机合成等领域。
(1)铝热反应可以冶炼金属铬,基态铬原子的核外电子排布式为:_______________________ 。
(2)AlCl3可用作下列反应的催化剂

①乙酸酐分子中发生sp3杂化的原子共有______ 个
②CH3COOH和H2O可以以任意比例互溶,其原因是它们均是极性分子和_________________ 。
③单个AlCl3分子的空间构型为_______ 。
(3)在氧化铝的作用下,N4H4(SO4)2可同碱反应生成一种类似白磷的N4分子,1molN4分子中含有的共价键的物质的量为_____ mol
(4)某遮光剂的晶胞如图甲(黑球为Na+,白球为AlFn(n-3)-阴离子),由图可推算知,n=________ 。

(5)由Fe和Y形成的某化合物的晶胞如图乙所示,该晶胞中与亚铁离子距离相等并且最近的亚铁离子有_____ 个。 另有一种有缺陷的Fe和Y形成的化合物的晶体由Fe2+,Fe3+,Y2-及空隙组成,可表示为Fe0.98Y,则该晶体中,n(Fe2+) : n(Fe3+) =______________ 。
(1)铝热反应可以冶炼金属铬,基态铬原子的核外电子排布式为:
(2)AlCl3可用作下列反应的催化剂

①乙酸酐分子中发生sp3杂化的原子共有
②CH3COOH和H2O可以以任意比例互溶,其原因是它们均是极性分子和
③单个AlCl3分子的空间构型为
(3)在氧化铝的作用下,N4H4(SO4)2可同碱反应生成一种类似白磷的N4分子,1molN4分子中含有的共价键的物质的量为
(4)某遮光剂的晶胞如图甲(黑球为Na+,白球为AlFn(n-3)-阴离子),由图可推算知,n=

(5)由Fe和Y形成的某化合物的晶胞如图乙所示,该晶胞中与亚铁离子距离相等并且最近的亚铁离子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】 、
、 、
、 、
、 四种元素,
四种元素, 最高能级电子排布式为
最高能级电子排布式为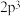 ,
, 元素的单质只能作氧化剂,
元素的单质只能作氧化剂, 是第三周期元素,其第1到第5电离能(
是第三周期元素,其第1到第5电离能( )数据如下:578、1817、2745、11575、14830,
)数据如下:578、1817、2745、11575、14830, 原子核外有14种不同的运动状态。回答下列问题:
原子核外有14种不同的运动状态。回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为_______ , 元素所在族第一电离能最大的前三种元素(按大→小顺序)分别是
元素所在族第一电离能最大的前三种元素(按大→小顺序)分别是_______ , 元素位于周期表中
元素位于周期表中_______ 区。
(2) 、
、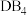 两种分子中,
两种分子中, 原子杂化轨道类型为
原子杂化轨道类型为_______ , 的分子构型为
的分子构型为_______ ;写出与 具有相同空间构型和键合形式的一种分子的化学式:
具有相同空间构型和键合形式的一种分子的化学式:_______ 。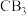 的熔点是1040℃,则该晶体中结构粒子间的相互作用类型为
的熔点是1040℃,则该晶体中结构粒子间的相互作用类型为_______ 。
(3) 、
、 两元素形成的常见氢化物的沸点
两元素形成的常见氢化物的沸点 ,其最主要的原因是
,其最主要的原因是_______ 。
(4) 与铜元素(黑球代表
与铜元素(黑球代表 )形成的某种化合物的晶胞结构如图所示,则该物质的化学式为
)形成的某种化合物的晶胞结构如图所示,则该物质的化学式为_______ ,若该晶体的密度为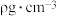 ,该晶体的晶胞参数
,该晶体的晶胞参数
_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 )。
)。

 、
、 、
、 、
、 四种元素,
四种元素, 最高能级电子排布式为
最高能级电子排布式为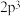 ,
, 元素的单质只能作氧化剂,
元素的单质只能作氧化剂, 是第三周期元素,其第1到第5电离能(
是第三周期元素,其第1到第5电离能( )数据如下:578、1817、2745、11575、14830,
)数据如下:578、1817、2745、11575、14830, 原子核外有14种不同的运动状态。回答下列问题:
原子核外有14种不同的运动状态。回答下列问题:(1)基态
 原子的电子排布式为
原子的电子排布式为 元素所在族第一电离能最大的前三种元素(按大→小顺序)分别是
元素所在族第一电离能最大的前三种元素(按大→小顺序)分别是 元素位于周期表中
元素位于周期表中(2)
 、
、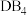 两种分子中,
两种分子中, 原子杂化轨道类型为
原子杂化轨道类型为 的分子构型为
的分子构型为 具有相同空间构型和键合形式的一种分子的化学式:
具有相同空间构型和键合形式的一种分子的化学式: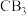 的熔点是1040℃,则该晶体中结构粒子间的相互作用类型为
的熔点是1040℃,则该晶体中结构粒子间的相互作用类型为(3)
 、
、 两元素形成的常见氢化物的沸点
两元素形成的常见氢化物的沸点 ,其最主要的原因是
,其最主要的原因是(4)
 与铜元素(黑球代表
与铜元素(黑球代表 )形成的某种化合物的晶胞结构如图所示,则该物质的化学式为
)形成的某种化合物的晶胞结构如图所示,则该物质的化学式为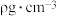 ,该晶体的晶胞参数
,该晶体的晶胞参数
 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次



