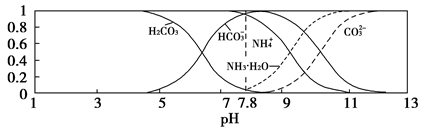
常温下,现有0.1 mol/L的NH4HCO3溶液,pH=7.8。已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如下图所示。下列说法不正确的是( )

A.NH4HCO3溶液中存在下列守恒关系:c(NH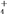 )+c(NH3·H2O)=c(HCO )+c(NH3·H2O)=c(HCO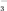 )+c(CO )+c(CO )+c(H2CO3) )+c(H2CO3) |
B.往该溶液中逐滴滴加氢氧化钠时NH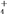 和HCO 和HCO 浓度逐渐减小 浓度逐渐减小 |
| C.通过分析可知常温下Kb(NH3·H2O)>Ka1(H2CO3) |
D.当溶液的pH=9时,溶液中存在下列关系:c(HCO )>c(NH )>c(NH )>c(NH3·H2O)>c(CO )>c(NH3·H2O)>c(CO ) ) |
15-16高三上·浙江·阶段练习 查看更多[4]
湖南师范大学附属中学2020届高三第五次月考化学试题(已下线)二轮复习 专题11 水溶液中的离子平衡 押题专练2015届四川省遂宁市高三第二次诊断考试化学试卷2015届浙江省严州中学高三1月份阶段测试化学试卷
更新时间:2016-12-09 07:10:01
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】电导率可用于衡量电解质溶液导电能力大小,且电导率越大溶液的导电能力越强。室温下,用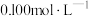 的
的 滴定
滴定 浓度均为
浓度均为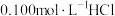 和
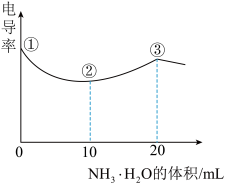
和 的混合液,电导率曲线如图所示。下列说法正确的是
的混合液,电导率曲线如图所示。下列说法正确的是
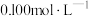 的
的 滴定
滴定 浓度均为
浓度均为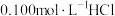 和
和 的混合液,电导率曲线如图所示。下列说法正确的是
的混合液,电导率曲线如图所示。下列说法正确的是
A. 溶液中 溶液中 为 为 |
| B.溶液温度高低为①>②>③ |
C. 点后因离子数目减少使电导率略降低 点后因离子数目减少使电导率略降低 |
D. 点时溶液中有 点时溶液中有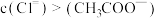 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】25oC时,浓度均为0.1 mol·L–1的几种溶液的pH如下:
下列说法正确 的是
| 溶液 | ①CH3COONa溶液 | ②NaHCO3溶液 | ③CH3COONH4溶液 |
| pH | 8.88 | 8.33 | 7.00 |
| A.①中, c(Na+) = c(CH3COO–) + c( OH–) |
B.由①②可知,CH3COO–的水解程度大于 的水解程度 的水解程度 |
| C.③中,由水电离出的c(OH–)水 = c(H+)水 = 1.0×10-7 mol·L–1 |
| D.推测25oC,0.1 mol·L–1 NH4HCO3溶液的pH <8.33 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】298 K 时,0.1 mol/L H2R溶液中H2R、HR‾、R2‾ 三种微粒的分布系数δ随 pH 变化的关系如图所示。已知:298 K时,HF的Ka=1.0×10‾3.4。下列表述正确的是
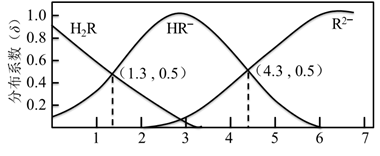

| A.H2R的Ka1 = 1.0×10‾1.3 |
| B.Na2R 溶液中离子存在关系:c(Na+) = c(HR‾ ) +2c(R2‾ ) |
| C.等物质的量的NaHR 和Na2R溶于水,所得溶液的pH 恰好为4.3 |
| D.在足量的NaF 溶液中加入少量 H2R 溶液:H2R + 2F‾ = 2HF + R2‾ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】室温下,将0.10 mol·L-1盐酸逐滴滴入20.00 mL 0.10 mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH= -lg c(OH-)。下列说法正确的是( )
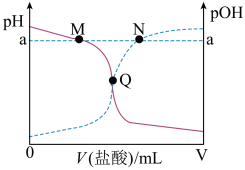
| A.M点所示溶液中:c(NH4+)+c(NH3·H2O)= c(Cl-) |
| B.N点所示溶液中:c(NH4+)>c(Cl-) |
| C.Q点所示消耗盐酸的体积等于氨水的体积 |
| D.M点和N点所示溶液中水的电离程度相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如图:

则下列分析都正确的组合是

则下列分析都正确的组合是
| 溶质的成分 | 对应图像 | 溶液中离子浓度关系 | |
| A | NaHCO3、Na2CO3 | Ⅱ | c(CO )<c(HCO )<c(HCO ) ) |
| B | NaOH、Na2CO3 | Ⅲ | c(OH-)>c(CO ) ) |
| C | Na2CO3 | Ⅳ | c(Na+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
| D | NaHCO3 | I | c(Na+)=c(HCO ) ) |
A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】室温下,通过下列实验探究某些碳酸盐溶液及碳酸氢盐溶液的性质。
已知: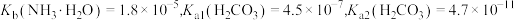 。
。
下列有关说法正确的是
已知:
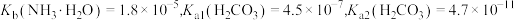 。
。| 实验 | 实验操作和现象 |
| 1 | 测量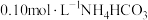 溶液的 溶液的 ,测得 ,测得 为 为 |
| 2 | 测量某浓度的 溶液的 溶液的 ,测得 ,测得 约为9.4 约为9.4 |
| 3 | 将两种浓度均为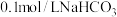 和 和 溶液等体积混合,测量其 溶液等体积混合,测量其 |
A.实验1溶液中: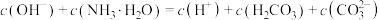 |
B.实验1测得的 值 值 |
C.实验2溶液中: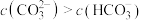 |
D.实验3所得溶液中: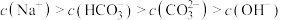 |
您最近一年使用:0次
【推荐3】已知MgF2难溶于水、可溶于酸。常温下,用HCl调节MgF2浊液的pH,测得在不同pH条件下,体系中−lgc(X)(X为Mg2+或F-)与lg[ ]的关系如图所示。下列说法正确的是
]的关系如图所示。下列说法正确的是
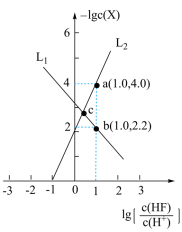
 ]的关系如图所示。下列说法正确的是
]的关系如图所示。下列说法正确的是
| A.Ksp(MgF2)的数量级为10-8 |
B.L1代表−lgc(Mg2+)与lg[ ]的变化曲线 ]的变化曲线 |
| C.a、c两点的溶液中均存在2c(Mg2+)=c(F-)+c(HF) |
| D.c点的溶液中存在c(Cl-)>c(Mg2+)>c(HF)>c(H+) |
您最近一年使用:0次

 )是二元弱酸,
)是二元弱酸,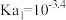 、
、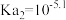 。20℃时,向
。20℃时,向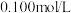 的
的 溶液中缓慢通入
溶液中缓慢通入 气体(忽略溶液体积的变化)。下列指定溶液中微粒关系正确的是
气体(忽略溶液体积的变化)。下列指定溶液中微粒关系正确的是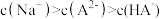
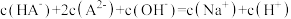
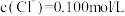 的溶液中:
的溶液中:

 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是

 水解形成
水解形成 胶体粒子数为
胶体粒子数为
 (分子结构如图)的共价键数目为
(分子结构如图)的共价键数目为
 溶液中
溶液中 与
与 离子数之和小于
离子数之和小于

